Primary analysis of a randomized, double-blind, phase II study of the anti-TIGIT antibody tiragolumab (tira) plus atezolizumab (atezo) versus placebo plus atezo as first-line (1L) treatment in patients with PD-L1-selected NSCLC (CITYSCAPE).
First Author : Rodriguez-Abreu D, st al.
PD-L1発現陽性非小細胞肺がんの一次治療において、アテゾリズマブ+抗TIGIT抗体tiragolumab併用療法をアテゾリズマブ+プラセボと比較する無作為化二重盲検比較第2相試験(CITYSCAPE試験)の初回解析結果
背景
TIGIT(T cell immunoreceptor with Ig and ITIM domains)はT細胞やナチュラルキラー細胞を含む複数の免疫細胞に発現する新規抑制性受容体であり、腫瘍細胞と抗原提示細胞上のPVR(CD155)がT細胞とNK細胞のTIGITに結合することによりT細胞とNK細胞の機能を阻害する。TIGITの発現はPD-1の発現と強く相関することが知られており、肺がんの腫瘍浸潤性T細胞においてもPD-1としばしば同時に発現する(Manieri NA et al. Trends Immunol. 2017;38:20-28)。
マウスを用いた前臨床モデルの検討においては、抗TIGIT抗体がTIGITとPVRの結合を阻害することによってT細胞を活性化し、抗PD-L1抗体との相乗効果により腫瘍を縮小させて(図1a、Johnston RJ et al. 2014;26:923-937)、結果的に生存期間を延長する効果が報告されている(図1b、Johnston RJ et al. 2014;26:923-937)。
図1a 抗TIGIT抗体と抗PD-L1抗体の相乗効果による奏効割合
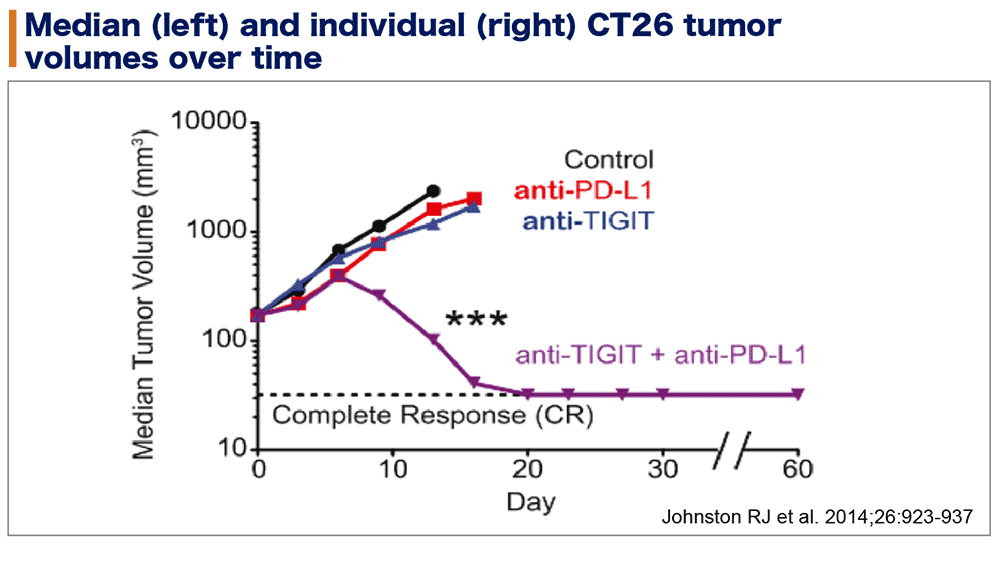
図1b 抗TIGIT抗体と抗PD-L1抗体の相乗効果による生存期間
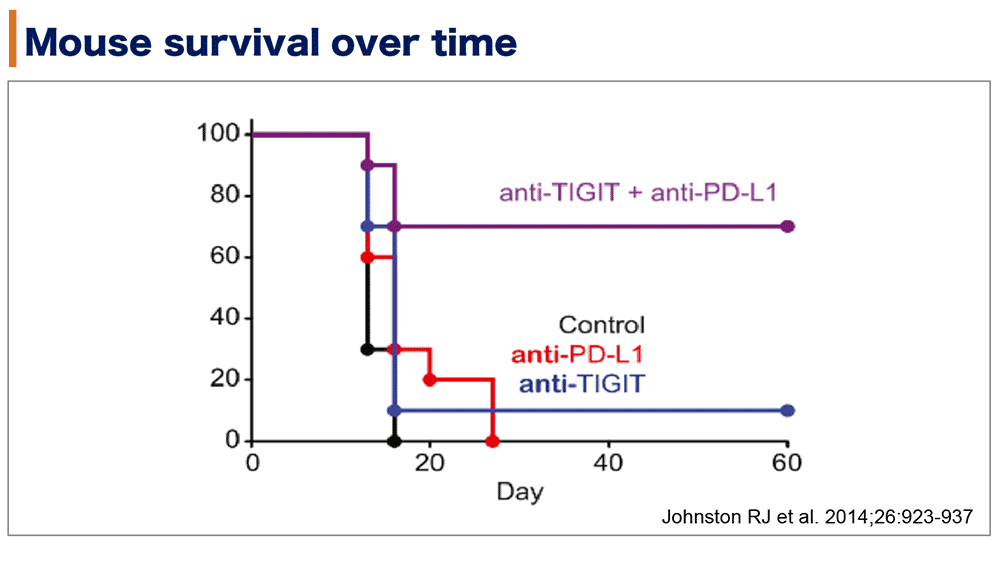
Tiragolumabは完全ヒトモノクローナルIgG1抗体の抗TIGIT抗体であり、TIGITとPVRの結合を阻害し、ヒトにおける抗PD-1/PD-L1抗体の抗腫瘍効果を補完することによって、その治療効果を発揮することが期待されている。
今回は、PD-L1陽性非小細胞肺がんの一次治療におけるアテゾリズマブと tiragolumabの併用療法の意義を検討するために行われた無作為化第2相試験であるCITYSCAPE試験の初回解析結果が報告された。
対象と方法
本試験はEGFR・ALK野生型かつPD-L1 TPS(22C3)1%以上の未治療非小細胞肺がん患者を対象として、アテゾリズマブ+tiragolumab併用療法群(試験治療群)とアテゾリズマブ+プラセボ群(標準治療群)に1:1の比率で無作為割付され、治療が実施された(図2)。割付層別化因子はPD-L1 TPS(1-49% vs 50%以上)、組織型(扁平上皮がん vs 非扁平上皮がん)および喫煙歴(あり vs なし)だった。アテゾリズマブは1,200mg点滴3週毎、tiragolumabは600mg点滴3週毎に投与された。Primary endpointは、客観的奏効割合(ORR)と無増悪生存期間(PFS)であり(Co-Primary endpoints)、Key secondary endpointsとして奏効期間、全生存期間、患者報告アウトカム、探索的解析としてPD-L1 TPSによる治療効果のサブグループ解析が設定された(今回はORRとPFS、それぞれのPD-L1 TPSによる治療効果のサブグループ解析結果、安全性が報告された)。
図2 試験デザイン

最終的に135例が登録され、出身国の内訳はアジア31%、米国27%、欧州42%だった。事前に規定された初回の主要解析は、最終登録例が2コース目の治療を終えた時点で実施され、結果として約80例の増悪イベントが確認された。データカットオフ日は2019年6月30日、フォローアップ期間中央値は5.9ヶ月だった。
