NEJ026:Final overall survival analysis of bevacizumab plus erlotinib treatment for NSCLC patients harboring activating EGFR-mutations.
First Author : Maemondo M, et al.
NEJ026試験:EGFR遺伝子変異陽性非小細胞肺癌に対するベバシズマブ+エルロチニブ併用療法の最終生存解析
背景
NEJ026試験(第3相試験)のOSの最終解析
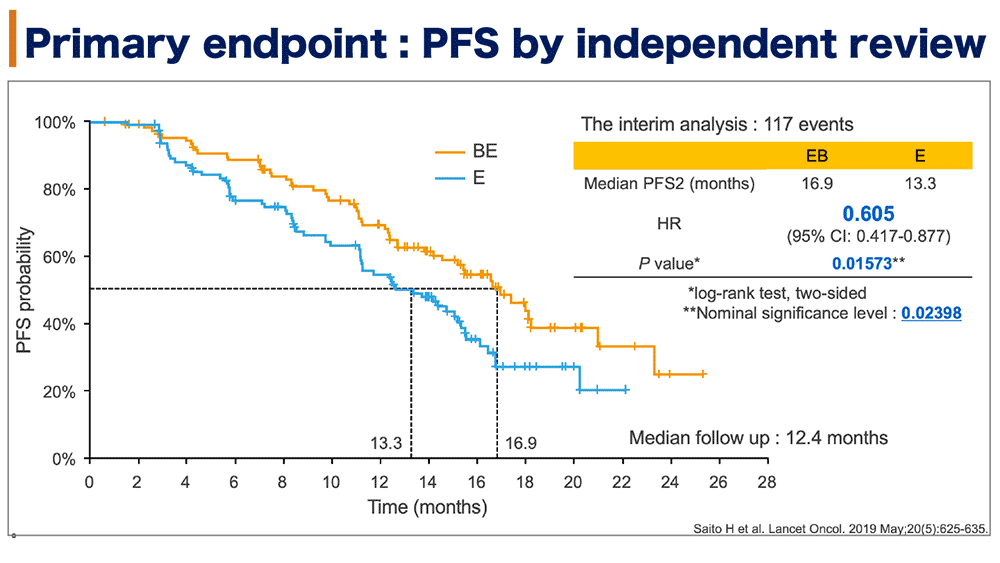
EGFR遺伝子変異陽性非小細胞肺癌に対する標準治療はEGFR-TKI単剤療法であるが、その治療効果は限定的で多くの症例は約1年前後で耐性化する。NEJ009試験では、ゲフィチニブ単剤に対してゲフィチニブ+カルボプラチン+ペメトレキセド併用療法でOSの優越性を示し、EGFR-TKI+αの併用療法により更なるOSの延長が期待されている。JO25567試験は、本邦で行われたエルロチニブ単剤(E群)に対してベバシズマブ+エルロチニブ併用療法(BE群)の有意なPFSを示した最初のランダム化第2相試験であったが、OSの延長を示すことはできなかった。一方、NEJ026はベバシズマブ+エルロチニブ併用療法の有効性を検討する第3相試験であり、プライマリー・エンドポイントの独立画像判定PFS中央値は、BE群:16.9ヶ月、E群:13.3ヶ月(HR:0.605、P=0.01573)と有意な延長を示し、事前規定された中間解析で有効性が確認された(図1参照)。今回はセカンダリー・エンドポイントのPFS2と全生存期間(OS)の最終解析が、本試験の研究代表者である岩手医科大学 前門戸任先生より発表された。
図1 NEJ026試験PFS結果
対象と方法
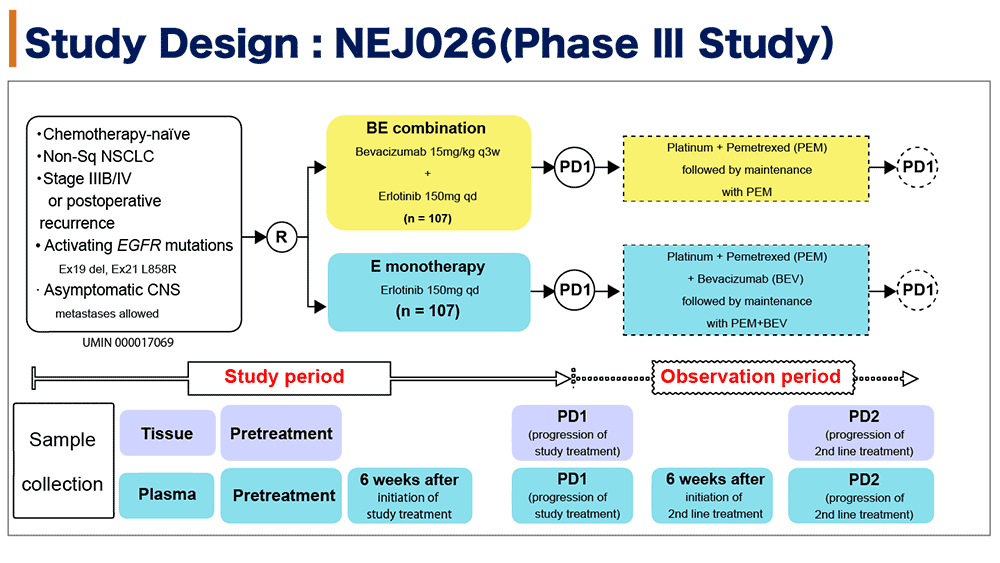
NEJ026試験は、未治療進行期(IIIB/IV期、術後再発)のEGFR遺伝子変異変異陽性(Ex19 delもしくはEx21 L858Rのいずれか)を対象に行われた。無症候性脳転移の症例は許容された。BE群とE群は1:1割付でBE群はベバシズマブ15mg/kgを3週毎投与とエルロチニブ150mg/Dayによる治療が、E群はエルロチニブ150mg/Dayによる治療がそれぞれ実施された。二次治療は、プラチナ製剤+ペメトレキセド併用療法が推奨され、E群においてはBEVのクロスオーバーを推奨していた。また試験期間中にオシメルチニブがT790M変異陽性例に二次治療以降として承認されたため、一次治療PD時にT790M陽性例に対しては実地臨床下でオシメルチニブが行われることが許容された。
さらに付随研究として組織および血漿のEGFR遺伝子変異検索がPNA-LNA Clamp法で行われた(図2参照)。
図2 NEJ026試験デザイン