First-line (1L) nivolumab (NIVO) plus chemotherapy (chemo) versus chemo in advanced gastric cancer/gastroesophageal junction cancer/esophageal adenocarcinoma (GC/GEJC/EAC): Expanded efficacy and safety data from CheckMate 649.
First Author : Markus H. Moehler, et al.
進行再発胃癌/食道胃接合部癌/食道腺癌患者の一次治療において、化学療法単独に対するニボルマブ+化学療法の有効性を検証した国際共同無作為化非盲検比較第3相試験(CheckMate649試験)の有効性・安全性に関する追加報告
背景
HER2陰性の進行再発胃癌(GC)または食道胃接合部癌(GEJC)の予後は不良であり、これまでに報告された一次治療例を対象とした臨床試験における全生存期間(OS)中央値は1年に満たないものがほとんどである。
GC/GEJC/食道腺癌(EAC)では、腫瘍細胞のみのPD-L1発現を評価するよりも、腫瘍と腫瘍環境における免疫細胞のPD-L1発現を反映したCPS(combined positive score)の方が、抗腫瘍効果が得られる対象を絞り込めることが報告されている1)。
CheckMate 649試験は進行再発GC/GEJC/EAC患者の一次治療において、抗PD-1抗体薬を併用した治療の有効性を検証する国際共同無作為化非盲検比較第3相試験であり、2020年の欧州臨床腫瘍学会(ESMO 2020)にてPD-L1 CPS≥5、≥1、および無作為化された全症例におけるニボルマブ+化学療法群の化学療法単独群に対するOSの有意な延長効果と無増悪生存期間(PFS)の延長効果、およびニボルマブ+化学療法の認容性が報告された2)3)。この結果を基に、2021年4月16日、米国食品医薬品局(FDA)はPD-L1発現を問わず、進行再発GC/GEJC/EACに対して化学療法との併用療法でニボルマブを承認した。
今回、CheckMate649試験に関しての有効性・安全性に関する追加報告が行われた。
対象と方法
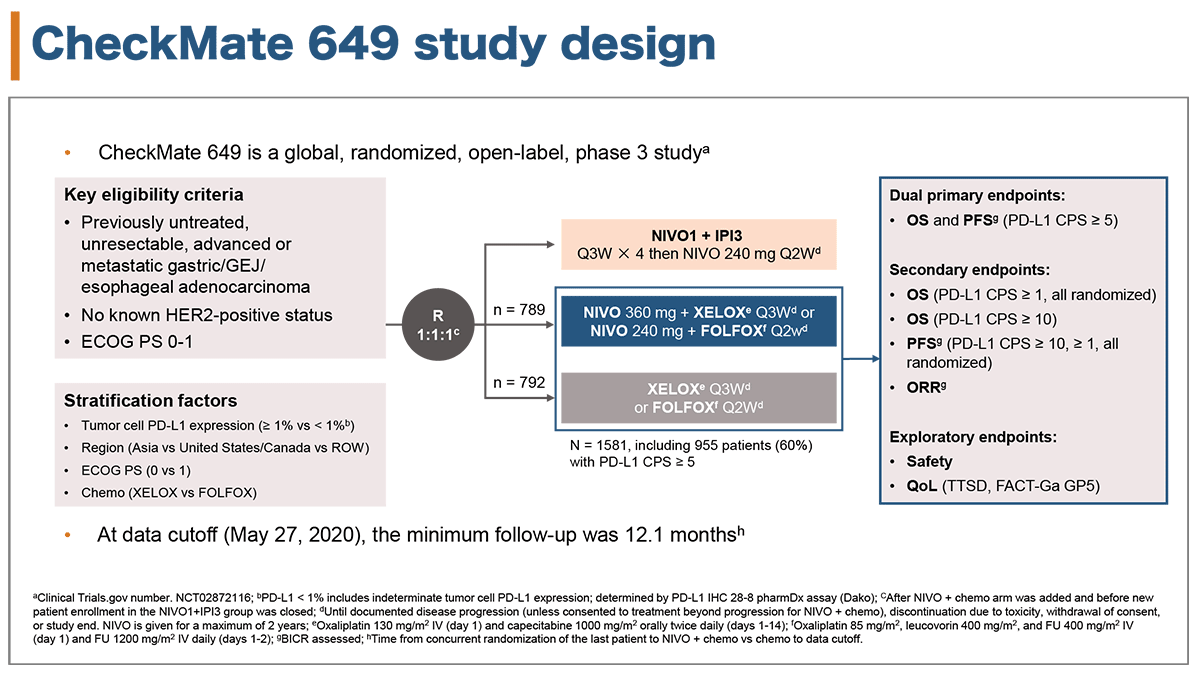
未治療のHER2陰性進行再発GC/GEJC/EACが対象とされた。患者はニボルマブ+イピリムマブ群、ニボルマブ+化学療法(FOLFOXもしくはXELOX)群、化学療法単独群(FOLFOXもしくはXELOX)の3群に1:1:1で割り付けられ、今回はニボルマブ+化学療法群(789例) vs 化学療法単独群(792例)に関する結果が報告された。
層別化因子は腫瘍細胞のPD-L1発現(≥1% vs <1%)、地域(アジア vs 北米 vs それ以外)、ECOG PS(0 vs 1)、化学療法(XELOX vs FOLFOX)とされた。
本試験の主要評価項目はPD-L1 CPS ≥ 5の対象におけるOS、PFSの2つが設定され、副次的評価項目はPD-L1 CPS ≥ 10、PD-L1 CPS ≥ 1、もしくは無作為化された全患者のOS、PFS、奏効割合だった。また、探索的な評価項目として安全性とQOL[臨床症状増悪までの期間(time to symptom deterioration:TTSD)、FACT-Ga GP5]に関する検討が実施された(図1)。
本解析のデータカットオフは2020年5月27日であり、最低観察期間は12.1ヶ月だった。
図1. CheckMate 649試験デザイン