Hepatic arterial infusion chemotherapy of oxaliplatin plus fluorouracil versus sorafenib in advanced hepatocellular carcinoma: A biomolecular exploratory, randomized, phase 3 trial (The FOHAIC-1 study).
First Author : Ning Lyu, et al.
進行肝細胞癌に対するオキサリプラチン+フルオロウラシル併用肝動注化学療法とソラフェニブ療法の比較:バイオマーカーの探索を含むランダム化第3相試験(The FOHAIC-1 study)
背景
進行肝細胞癌においては肝内巨大腫瘍や脈管侵襲を有する症例が77.5%、肝外転移を有する症例が37.9%と報告されている。しかし、IMbrave150, SHARP, Asia-Pacific SHARPなどの臨床試験では、肝外転移を有する症例はそれぞれ63%, 53%, 68.7%と多いのに対して、脈管侵襲を有する症例は38%, 36%, 36%しかなかった。FOLFOXによる肝動注化学療法(hepatic arterial infusion chemotherapy: HAIC)(HAIC-FO療法)の忍容性と有効性は以前に行われた第2相試験(the FOXAI study)で示された。今回計画されたFOHAIC-1試験は、進行肝細胞癌に対する一次薬物療法として、ソラフェニブに対するHAIC-FO療法の有効性を検証する最初のランダム化第3相試験である。本試験では特に肝内腫瘍量が多い症例が対象である。さらに、治療効果を予測するための遺伝的プロファイルを行った。
対象と方法
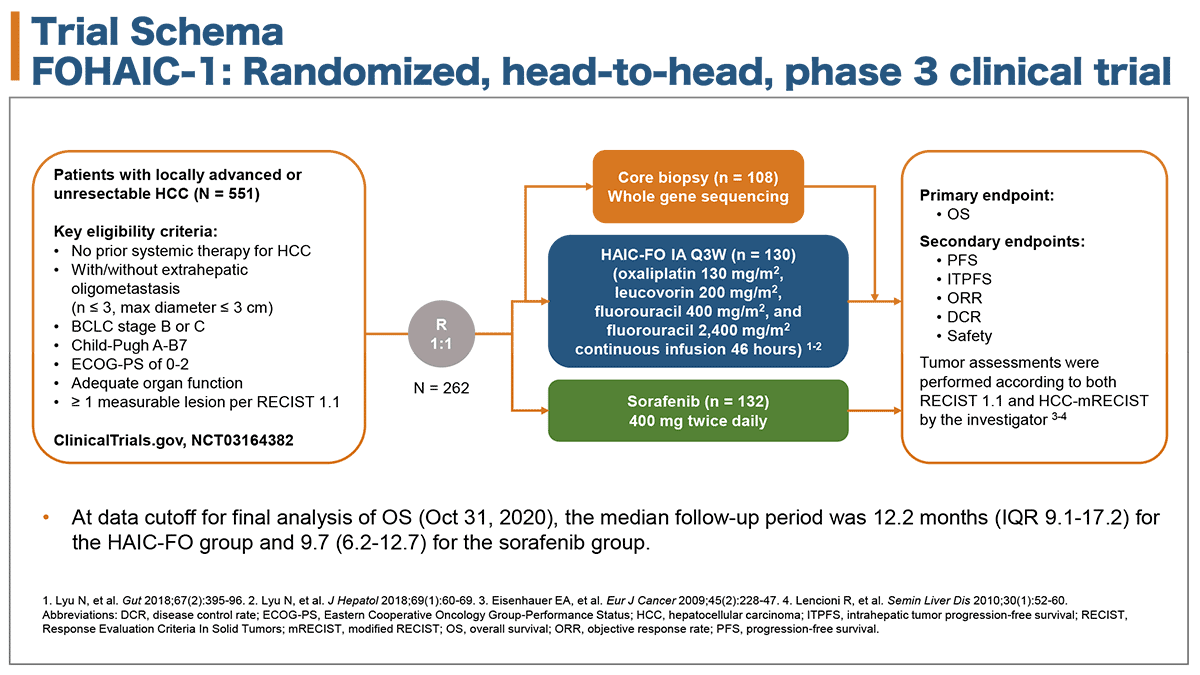
FOHAIC-1試験は全身薬物療法歴のない局所進行もしくは切除不能肝細胞癌患者を対象として、HAIC-FO療法の有効性及び安全性をソラフェニブと比較して検証する第3相試験である。主な適格基準はBCLC(Barcelona Clinic Liver Cancer) stage BまたはC、Child-Pugh分類A-B7、ECOG-PS(Eastern Cooperative Oncology Group-Performance Status) 0-2などである。患者はHAIC-FO療法を受ける群とソラフェニブ治療を受ける群に、1:1の割合で無作為に割り付けられた(図1)。HAIC-FO療法ではoxaliplatin 130 mg/m2, leucovorin 200 mg/m2, fluorouracil 400 mg/m2及びfluorouracil 2400 mg/m2 46時間持続投与を3週間毎に行い、ソラフェニブ群ではソラフェニブ1回400㎎を1日2回内服した。また、HAIC-FO群では治療効果を予測するため、腫瘍及び正常肝組織の生検によるゲノム解析が行われた。
図1. 試験デザイン