A randomized, controlled, multi-center, open-label study of adjuvant nab-paclitaxel plus S-1 (AS) versus capecitabine plus oxaliplatin (CapeOX) for stage III gastric cancer after D2 resection.
First Author : Yu Pengfei, et al.
D2郭清を伴う胃切除術後pStageIII胃癌に対する術後補助化学療法としてのナブパクリタキセル+S-1(AS)療法とカペシタビン+オキサリプラチン(CapeOX)療法の多施設共同前向き無作為化非盲検試験
背景と目的
現在、胃癌術後pStageIIIに対する術後補助化学療法は、日本で実施されたJACCRO GC-07(START-2)試験[ドセタキセル(DTX)+S-1(DS)療法とS-1単剤との比較]1)と、韓国および中国で実施されたCLASSIC試験[カペシタビン+オキサリプラチン(CapeOX)療法と手術単独療法との比較]2)、また、韓国で実施され2021年に報告されたARTIST 2試験[S-1+オキサリプラチン(SOX)療法+-RTとS-1単剤との比較]3)の結果からフッ化ピリミジン系薬剤+オキサリプラチン6ヶ月、あるいは、Docetaxel(DTX)+S-1(DS)療法1年が推奨されている。
しかしながらこれまでに、タキサン系薬剤+フッ化ピリミジン系薬剤とプラチナ製剤+フッ化ピリミジン系薬剤を比較した無作為化試験の報告はなく、このいずれを選択すべきかは明らかにされていない。
今回中国から、D2郭清を伴う胃切除術後pStageIII胃癌に対する術後補助化学療法として、フッ化ピリミジンにプラチナ併用とタキサン併用を比較検証する試験としてカペシタビン+オキサリプラチン(CapeOX)療法に対するナブパクリタキセル+S-1(AS)療法との安全性と有効性検証した多施設共同無作為化非盲検試験試験の中間解析結果が始めて報告された。
対象と⽅法
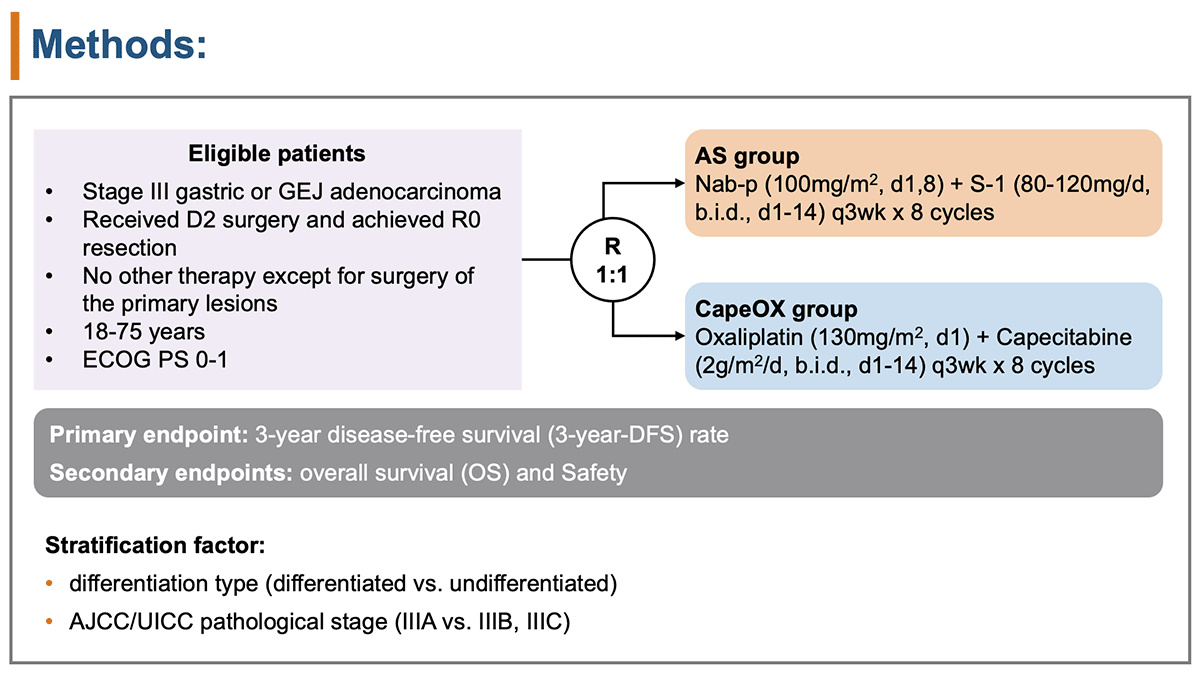
根治切除(胃切除+D2郭清)を行ったpStage IIIの胃または食道胃接合部の腺癌患者を対象とした。
AS療法群[(ナブパクリタキセル 100mg/m2、day 1、8)+(S-1 80-120 mg/day、day 1-14)、3週毎、8コース]とCapeOX療法群[(カペシタビン 2000mg/m2/day、day 1-14)+(オキサリプラチン 130mg/m2、day1)、3週毎、8コース]の2群に無作為に割り付けられた(図1)。層別因子は組織型(分化型 vs. 未分化型)、pStage(IIIA vs. IIIB、IIIC)だった。
図1 本試験の概要