Trastuzumab deruxtecan (T-DXd) versus treatment of physician’s choice (TPC) in patients (pts) with HER2-low unresectable and/or metastatic breast cancer (mBC): Results of DESTINY-Breast04, a randomized, phase 3 study.
First Author : Shanu Modi, et al.
HER2低発現の切除不能・転移乳がんに対するトラスツズマブ・デルクステカンと主治医選択治療を比較した第3相臨床試験(DESTINY-Breast04試験)。
背景と⽬的
HER2 IHC1+またはIHC2+/ISH-と定義されるHER2低発現の進行乳がんは、現在の抗HER2療法が有効でないため、HER2陰性乳がんとして治療される。ホルモン受容体(HR)陽性/HER2陰性乳がん治療においては、サイクリン依存性キナーゼ(CDK)4/6阻害薬に抵抗性となった場合、有効な治療は限られる。リアルワールド・データを用いた先行研究ではCDK4/6阻害薬抵抗性となったHR陽性HER2陰性乳がんの無増悪生存期間(PFS)は4か月未満と報告された。さらに、複数の化学療法に抵抗性となった患者に対して治療により得られる効果は乏しく、エリブリン・カペシタビンによるHER2陰性乳がんの治療では全生存期間(OS)が15か月未満との報告がある。
トラスツズマブ・デルクステカン(T-DXd)は細胞表面のHER2に結合し細胞内へ取り込まれると、リンカーが外れることでトポイソメラーゼI阻害薬であるデルクステカンが放出される。デルクステカンはT-DXdを取り込んだ細胞のアポトーシスをもたらすと同時に、近隣の細胞に対しても抗腫瘍効果を発揮する(バイスタンダー効果)。HER2低発現の進行乳がん患者(N=54)に対して、T-DXdを投与した第1b相試験では、無増悪生存期間(PFS)中央値が11.1か月、奏効割合は37.0%と報告された。本報告のDESTINY-Breast04試験は、HER2低発現の進行乳がんに対してT-DXdの効果を検証した初の第3相臨床試験である。
対象と⽅法
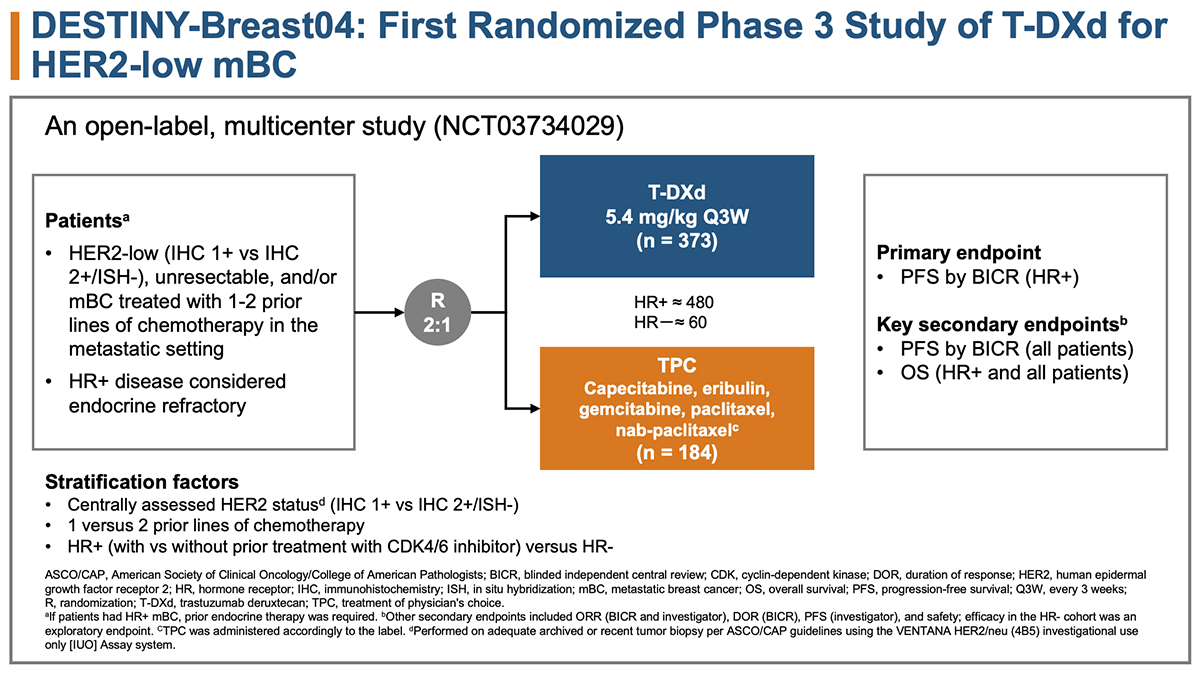
HER2低発現(IHC1+、IHC2+/ISH-)の切除不能・転移乳がんで1-2レジメン以上の化学療法投与歴があり、ホルモン療法抵抗性の患者が対象となった。2:1の割合でT-DXd投与群(5.4mg/kg、3週毎)と主治医選択治療(カペシタビン・エリブリン・ゲムシタビン・パクリタキセル・nab-パクリタキセルのいずれか)に無作為に割り付けられた。割り付けに際してHER2発現の程度、投与された化学療法のレジメン数、ホルモン受容体の発現によって層別化された。主要評価項目はHR陽性患者におけるPFS、副次評価項目は全患者のPFS・OSと設定された(図1)。
図1 試験デザイン