Final results from ClarIDHy, a global, phase 3, randomized, double-blind study of ivosidenib vs placebo in patients with previously treated cholangiocarcinoma and an isocitrate dehydrogenase 1(IDH1) mutation
First Author : Andrew X Zhu, et al.
IDH1 変異を有する既治療の胆道癌に対するivosidenibの有効性を検証する二重盲検グローバル第3相試験(ClarIDHy試験)の最終成績
背景
胆道癌は希少癌であり、有効な治療は限られている。肝内胆管癌において、IDH1 変異は最大20%に認めると報告されている。変異型IDH1 による癌代謝物のD-2-ヒドロキシグルタル酸(2-HG)の産生は、発がんを誘発する。ivosidenib(AG-120)は、IDH1 変異蛋白を阻害する初めての経口投与、低分子化合物であり、IDH1 変異を有する切除不能の進行胆道癌に対するivosidenibの有効性を検証するグローバル第3相試験(ClarIDHy試験)が行われた。ClarIDHy試験の結果は、すでに論文化(Abou-Alfa GK, et al. Lancet Oncol, 2020;21:796-807)されているが、今回、最終の追跡調査の結果が報告された。
対象と方法
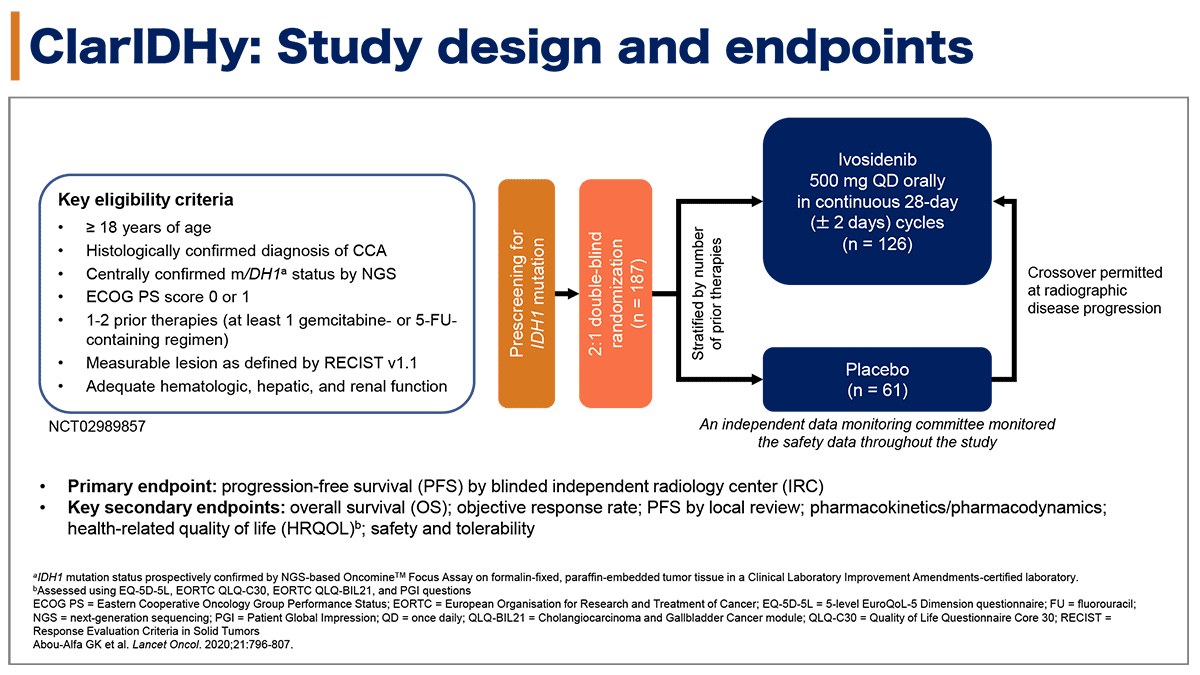
本試験の主な適格基準は、中央判定においてIDH1 変異が確認された進行胆道癌で、少なくともゲムシタビンもしくは5-FU含有レジメンによる治療歴を有する症例だった(図1)。登録患者は前治療で層別化され、ivosidenib群(500㎎/日)とプラセボ群に2:1に二重盲検で割りつけられた。病勢増悪時にはプラセボ群からivosidenib群へのクロスオーバーが許容された。187例が登録され、ivosidenib群に126例、プラセボ群に61例が割り付けられた。主要評価項目は無増悪生存期間(PFS)、副次評価項目は全生存期間(OS)、客観的奏効割合、主治医判定によるPFS、薬物動態学/薬力学、QOL、安全性と忍容性だった。
図1. 試験デザイン