Lefitolimod vs standard of care (SOC) for patients with metastatic colorectal cancer (mCRC) responding to first-line standard treatment: Results from the randomized phase III IMPALA trial.
First Author : Salazar R, et al.
背景
切除不能大腸がんの一次化学療法の治療戦略として、導入化学療法後にフッ化ピリミジン製剤±ベバシズマブによる維持療法を行うことがこれまでの臨床試験(OPTIMOX11)、AIO02072)、CAIRO33))の結果から推奨されてはいるものの、導入療法後の休薬(Treatment holiday)との比較に関しては、全生存期間の改善はこれまでに証明されておらず、維持療法がよいのか、休薬がよいのかについては、いまだに議論の余地がある。
近年、大腸がんにおける免疫チェックポイント阻害剤の治療効果についての検証がなされているが、有効性はMSI-Highの症例に限定的であり、MSS大腸がんを対象としたPD-(L)1阻害薬の治療効果を検証する試験(IMblaze3704)、MODULE5))が実施されてはいるものの、これまでには十分な有効性は確認できていない。
Lefitolimod (MGN1703)は、Toll-like receptor(TLR)-9に作用する皮下注射製剤で自然免疫や獲得免疫の活性化につながることが報告されている。これまでに、切除不能大腸がんの一次治療における維持療法として、Lefitolimodとプラセボを比較する無作為化比較第II相試験6)(IMPACT試験)が実施され、Lefitolimod群で無増悪生存期間の延長を認めた。IMPACT試験の結果を基に、一次治療における標準治療群(導入化学療法の継続:Continued first-line・維持療法の実施:De-escalation・休薬:Off treatment)をコントロール群として、Lefitolimodの維持療法の有効性と安全性を検証する無作為化第III相比較試験が実施されることになった。
対象と方法
本試験は、切除不能進行大腸がん、ECOG PS 0-1、標準的一次化学療法を12〜30週投与された時点でCR/PRが得られた患者とされた。試験治療群はLefitolimod(60mg皮下注射:週に2回/48時間以上の間隔をあけて)による維持療法を開始し、一方、コントロール群は、主治医の判断により、Continued first-line か、De-escalation、または、Off treatmentを選択する群(標準治療群)に無作為割付けされた。PDが確認された場合、Lefitolimod群は導入化学療法の併用を開始し、標準治療群のDe-escalation症例とOff treatment症例においては、導入化学療法の再導入が行われることが規定された。(図1)
図1
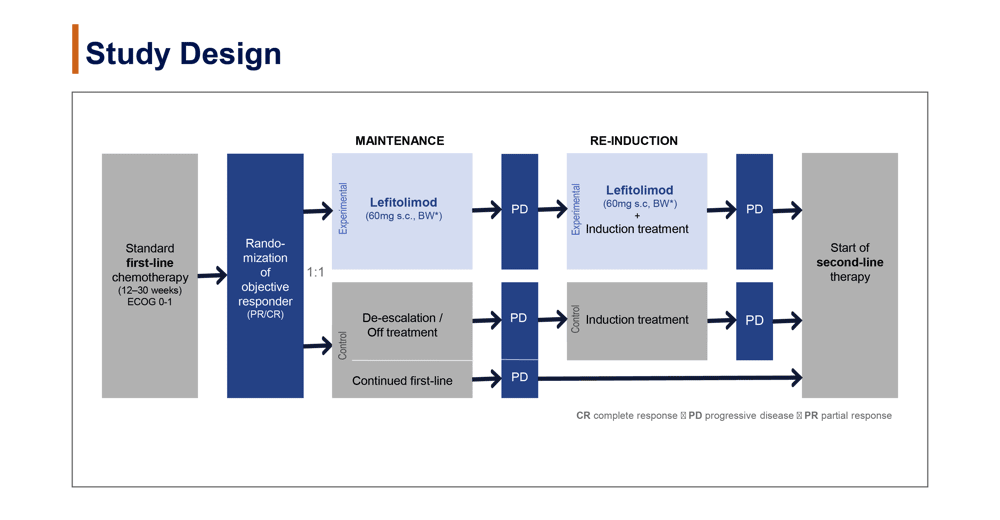
本試験の主要評価項目は全生存期間(OS)、副次的評価項目は無作為化からの無増悪生存期間(PFS)、奏効率(ORR)、安全性(CTCAE v4.03)、Lefitolimodの薬物動態解析とされた。また、治療開始時の患者背景や大腸がんに関連するバイオマーカー、免疫学的バイオマーカーによる探索的サブグループ解析が事前に設定された。
統計学的設定は標準治療群と比較しLefitolimod群の生存期間のハザード比を0.75と期待し、両側検定α= 0.05、検出力 80%で優越性を示す仮説で行われた。365イベント数が必要とされた。
