Abstract FIGHT-202
A phase 2 study of pemigatinib in patients with previously treated locally advanced or metastatic cholangiocarcinoma.
First Author : Vogel A, et al.
背景
局所進行もしくは遠隔転移を有する胆道癌に対する一次治療はGemcitabine+Cisplatin療法であるが1)、二次治療の効果は限定的である。胆道癌ではFGFR (線維芽細胞増殖因子受容体)2を含むいくつかの遺伝子変異が知られているが、FGFR2融合/再構成遺伝子は欧米の胆道癌患者の10~16%に認められる2)。ペミガチニブはFGFR1-3に対する選択的阻害剤であり3)、安全性、有効性を評価するための試験が実施された。
対象と方法
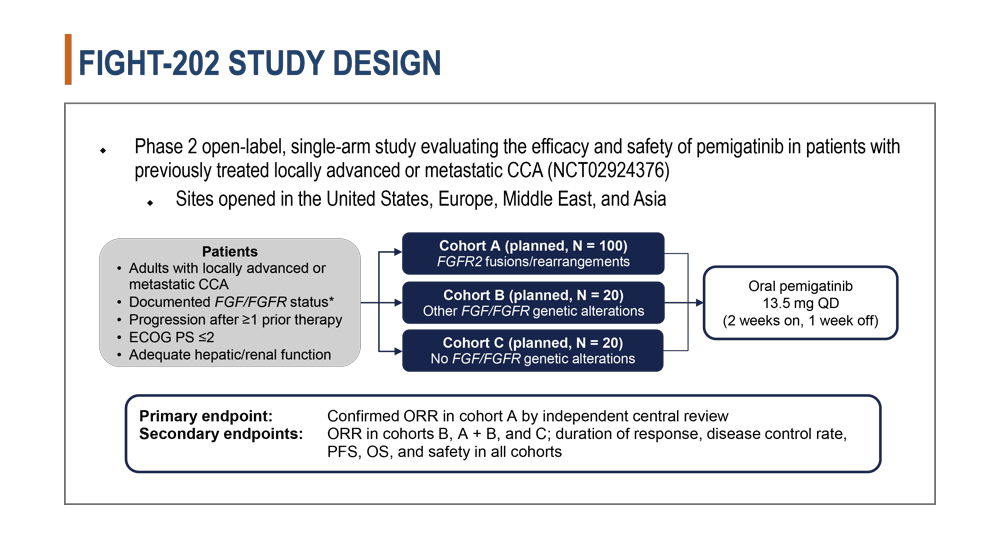
本試験はPhase2オープンラベル単相試験であり、治療歴を有する進行胆道癌に対するペミガチニブの効果、安全性を評価するために行われた。対象は局所進行もしくは遠隔転移を有する胆道癌であり、FGF/FGFR遺伝子異常が確認され、治療歴があり、ECOG PS2以下、肝腎機能が適切に保たれた症例である。
コホートAはFGFR2融合/再構成遺伝子を有する100例、コホートBは他のFGF/FGFR遺伝子変異を有する20例、コホートCはFGF/FGFR変異を有さない20例が設定され、いずれのコホートにもペミガチニブ13.5mgの経口投与を2週投与1週休薬で実施した。
主要評価項目はコホートAにおける独立評価委員会により評価された全奏功割合 (ORR)である。副次評価項目はコホートB、A+B、CにおけるORRと、全てのコホートにおける奏効期間 (DOR)、病勢コントロール割合 (DCR)、無増悪生存期間 (PFS)、全生存期間 (OS)、安全性である。(図1)
図1