Efficacy and safety of lanreotide autogel (LAN) 120 mg every 14 days in progressive pancreatic or midgut neuroendocrine tumours (NETs): CLARINET FORTE study results.
First Author : Marianne E. Pavel, et al.
進行膵・中腸神経内分泌腫瘍に対するランレオチド オートゲル(LAN)の120mg隔週投与の有効性と安全性についての第2相試験
背景
ランレオチドは、ソマトスタチンのアミノ酸の種類と個数を変化させて、体内での安定性をより高めた合成ソマトスタチンアナログであり、ランレオチド オードゲル(LAN)はその持続性をさらに高めた徐放性製剤である。既に本邦でも膵・消化管神経内分泌腫瘍に対して120mgを4週毎の投与にて承認が得られているが、隔週投与により投与頻度を増すことによる効果の改善が期待されている。今回、進行膵・中腸神経内分泌腫瘍を対象として、LAN120mg隔週投与の有効性と安全性を検討した第2相臨床試験(CLARINET FORTE試験)の解析結果が報告された。
対象と方法
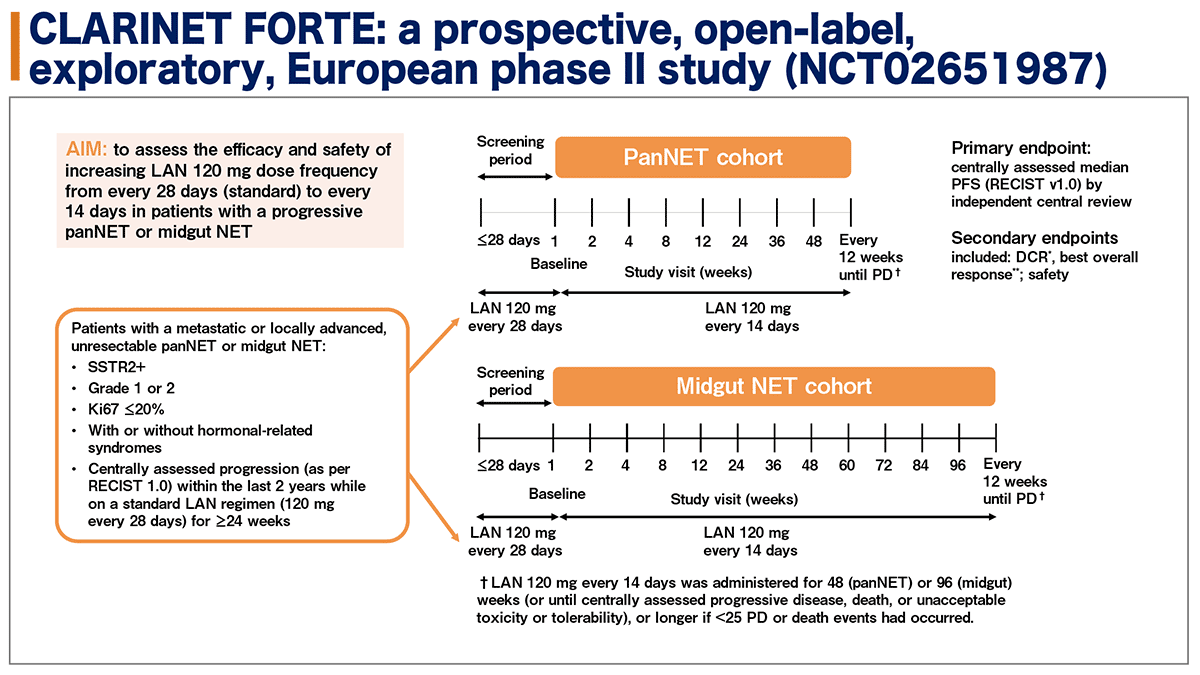
本試験の対象は、転移巣を有するか、局所進行により切除不能と診断された進行膵あるいは中腸(十二指腸・空腸・回腸・盲腸)NETであり、主な適格基準はNET Grade 1 or 2(Ki67 ≤20%)、SSTR2(ソマトスタチンレセプターtype2)陽性、過去2年以内に標準的なLANレジメン(120mg 4週毎投与)を24週以上継続した後に中央判定にて腫瘍進行を認めた治療歴を有する症例、でありホルモン症状を有する症例、有しない症例、両者が登録された。(図1)
膵・中腸NET症例は共に登録後、120mg投与、4週毎のスクリーニング期間を経て、LAN120mg隔週投与へ移行する。膵NETコホートでは48週、中腸NETコホートでは96週投与し、その後は、12週毎に投与した。中央判定による病勢進行(PD)、死亡、許容できない毒性の出現、あるいは不耐となるまで投与され、試験全体で死亡もしくはPDのイベントが25件以上発生するまで試験を継続する、とされた。
本試験の主要評価項目はRECISTv1.0による中央判定の無増悪生存期間中央値(mPFS)であり、副次評価項目は病勢制御割合(DCR)、最良総合効果(best overall response)、安全性とされた。(図1)
図1. 試験デザイン