Atezolizumab in combination with bevacizumab for patients with unresectable/metastatic anal cancer
First Author : Morris V, et al.
切除不能/転移性肛門管癌に対するアテゾリズマブ+ベバシズマブ併用療法の第2相試験
背景
肛門管扁平上皮癌の年間発生率は過去15年で着実に増加しており1)、症例の90%以上が過去のHPV感染に関連している2)。切除不能な既治療肛門管扁平上皮癌に対する抗PD-1/PD-L1抗体単剤療法の有効性は、ニボルマブ3)/ペムプロリズマブ4)で報告されており、奏効割合 11-24%、無増悪生存期間中央値 2.0-4.1ヶ月、生存期間中央値 11.5-11.9ヶ月と報告されている。
VEGFシグナル伝達は、進行がん患者の抗PD-1 / PD-L1療法に対する耐性の潜在的なメカニズムとして、免疫回避と免疫抑制を促進する可能性が示されている。
抗PD-L1抗体のアテゾリズマブと抗VEGF抗体のベバシズマブの併用療法が切除不能肝細胞癌において生存期間を延長することが示されている5)。今回、切除不能肛門管癌に対するアテゾリズマブ+ベバシズマブ併用療法の有効性と安全性が検討された。
対象と方法
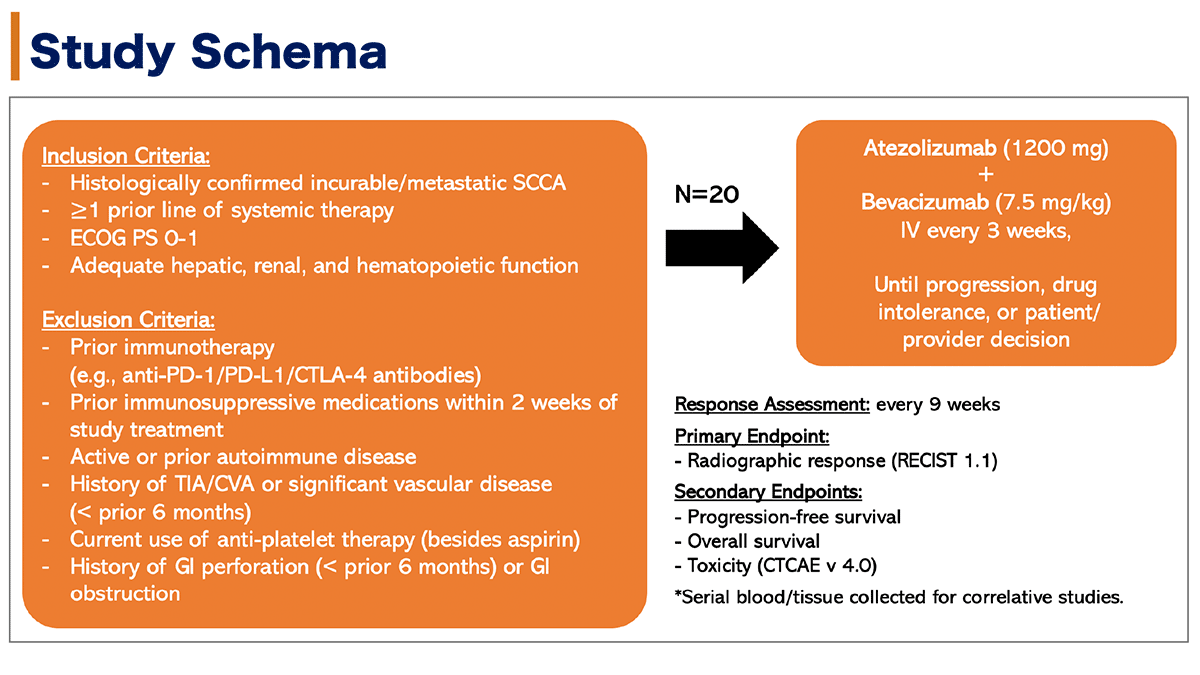
本試験の対象は、組織学的に扁平上皮癌と診断された切除不能/転移性肛門管癌で、1レジメン以上の治療歴を有する症例とされた。免疫チェックポイント阻害薬の既治療例や試験治療開始2週間前に免疫抑制療法を受けた症例、自己免疫性疾患の合併、または既往を有する症例は除外された。
目標症例数は20例と設定され、試験治療はアテゾリズマブ 1200mg/body、ベバシズマブ 7.5mg/kgを3週間毎に不応/不耐となるまでに投与された。本試験の主要評価項目は奏効割合であり、副次的評価項目は無増悪生存期間、全生存期間、有害事象(CTCAE v4.0)とされた。(図1)
図1. 試験デザイン