Randomized phase III trial of nivolumab in combination with carboplatin, paclitaxel, and bevacizumab as first-line treatment for patients with advanced or recurrent non-squamous NSCLC
First Author : Jong-Seok Lee
進行または再発非扁平上皮非小細胞性肺癌患者のファーストライン治療としてのカルボプラチン、パクリタキセル、ベバシズマブに対するニボルマブ併用療法のランダム化第III相試験
背景
細胞傷害性抗癌薬や血管新生阻害薬は、ニボルマブなどの免疫チェックポイント阻害薬の治療効果を高める可能性がある。ONO4538-52 / TASUKI-52試験は、非扁平上皮非小細性肺癌の一次治療において、カルボプラチン、パクリタキセル、ベバシズマブ併用療法にニボルマブの上乗せの有効性を検討した無作為化二重盲検第III相試験である。
対象と方法
未治療進行再発EGFR/ALK遺伝子変異陰性の非扁平上皮非小細胞性肺癌患者550例を、カルボプラチン(AUC 6)+パクリタキセル(200 mg / m2)、およびベバシズマブ(15 mg / kg)を3週間毎最大6サイクルに、ニボルマブ(360 mg/body 3週毎)またはプラセボを投与する群に1:1で無作為化割り付けされた。ニボルマブ/プラセボおよびベバシズマブは、疾患の進行または許容できない毒性が認められるまで維持療法として継続された。主要評価項目は中央判定による無増悪生存期間(PFS)で副次的評価項目は 全生存期間(OS)、奏効割合(ORR)、および安全性であった。また層別因子は28-8抗体を用いたPD-L1の発現(50%以上、1-49%、1%または評価不能)、PS 0-1、性別であった。
結果
日本、韓国、台湾の患者から550人が登録され、273人(ニボルマブ)と275人(プラセボ)に治療が実施された。306イベントが観察された第1回中間解析において、PFSが事前に規定された中間解析のαである0.0363を有意に下回る結果であり、早期発表となった。今回の発表における追跡調査の中央値は13.7ヶ月(追跡期間最小値7.4ヶ月)であった。
背景因子は両群ともに偏りはなかった。
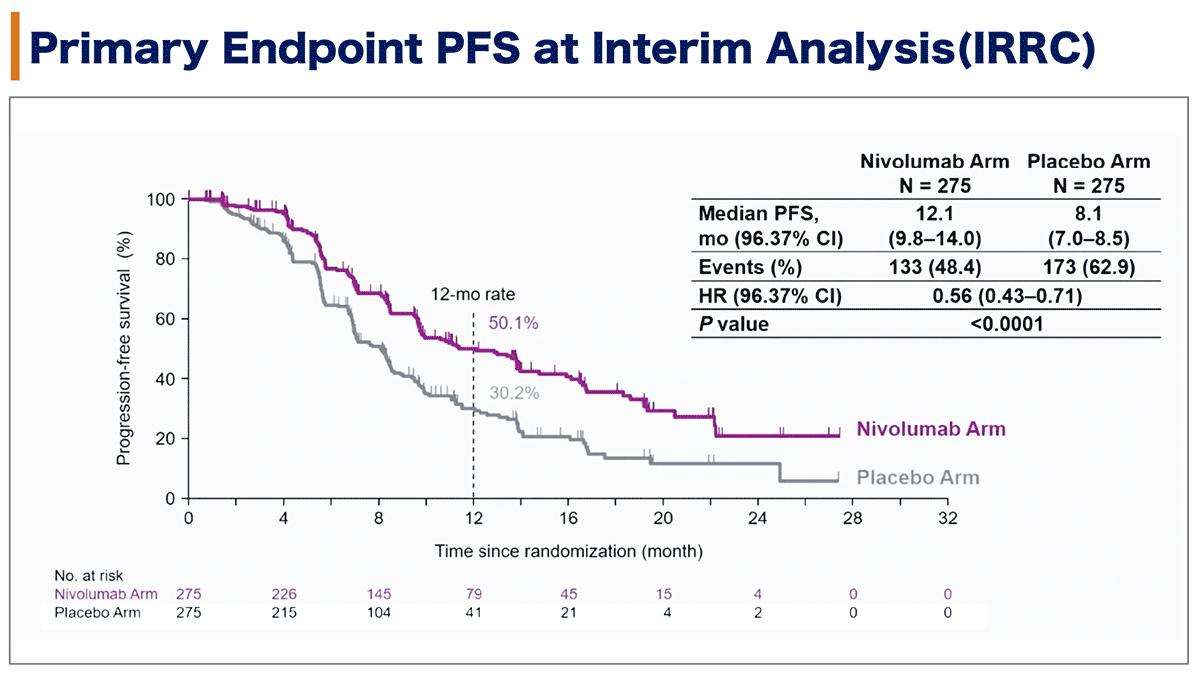
PFS中央値はニボルマブ群 12.1か月、プラセボ群 8.1か月でハザード比(HR] 0.56(96.37%CI; 0.43-0.71, p <0.0001)、1年PFS率はそれぞれ50.1%、30.2%であり、ニボルマブ群で有意なPFSの延長を認めた(図1)。
図1. 無増悪生存期間