Pembrolizumab Plus Chemotherapy Versus Chemotherapy as First-Line Therapy in Patients With Advanced Esophageal Cancer: The Phase 3 KEYNOTE-590 Study.
First Author : Kato K, et al.
進行食道がん患者に対する一次化学療法としてのペムブロリズマブ+化学療法と化学療法を比較する第3相試験:KETNOTE-590試験
背景
現在の進行食道がんに対する標準的一次化学療法はフッ化ピリミジン製剤と白金製剤の併用療法、標準的二次化学療法はドセタキセル、パクリタキセル、イリノテカンおよびパクリタキセル±ラムシルマブ(腺がんの場合)である。
ペムブロリズマブ単剤療法は進行/転移性食道がんに対する抗腫瘍効果と忍容可能な安全性を報告している。三次治療以降を対象としたKEYNOTE-180試験では、PD-L1 combined positive score (CPS) 10以上の扁平上皮がん症例においてペムブロリズマブ単剤療法は奏効割合 13%、奏効期間中央値 未到達という成績を示した1)1)2)。また、二次治療例を対象としたKEYNOTE-181試験では、CPS 10以上の扁平上皮がん症例において、ペムブロリズマブ単剤療法は標準治療(パクリタキセル/ドセタキセル/イリノテカン)と比較し、全生存期間(中央値:10.1ヶ月 vs 6.7ヶ月, HR 0.61)、奏効割合(22% vs 7%)、奏効期間(中央値:9.3ヶ月 vs 7.7ヶ月)を改善した3)。これらの結果を基に、米国FDAは1レジメン以上の治療を受け、増悪を認めたCPS 10以上の再発性局所進行もしくは転移性食道扁平上皮がんに対して、ペムブロリズマブ単剤療法を承認した。
以上を背景とし、進行食道がんの一次治療として化学療法+ペムブロリズマブ療法と化学療法+プラセボ療法を比較検討するプラセボコントロール二重盲検比較ランダム化第3相試験(KEYNOTE-590試験)が実施された。
対象と方法
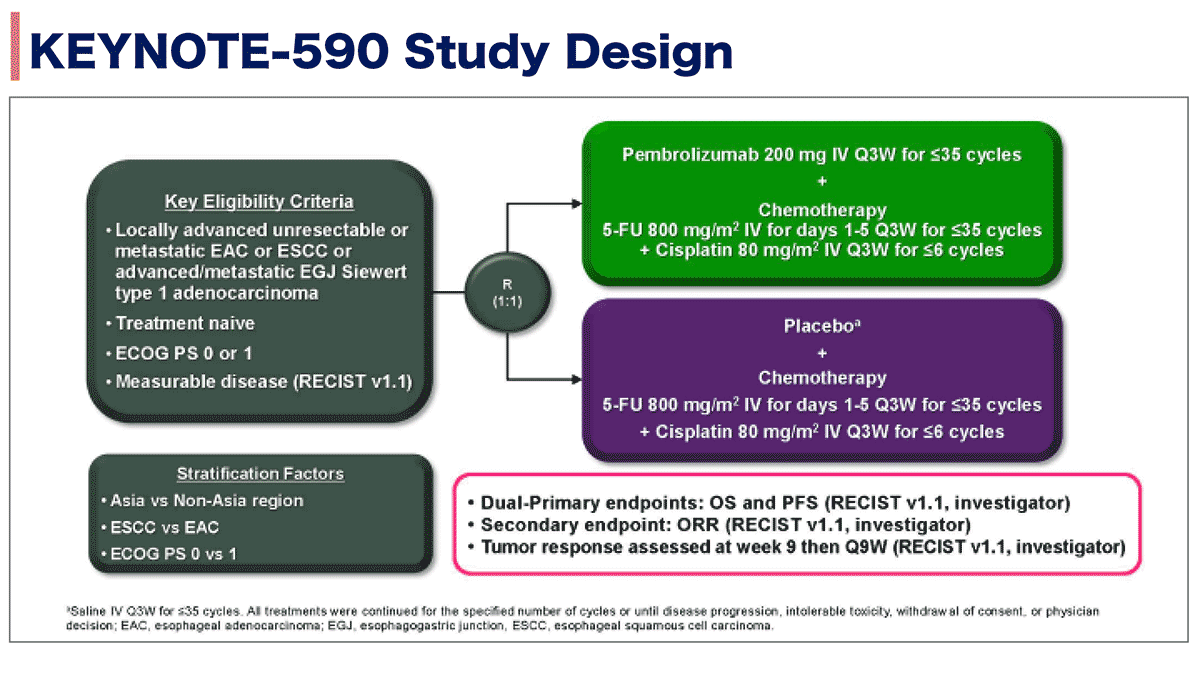
KEYNOTE-590試験は未治療の切除不能局所進行もしくは転移性食道がん(腺がん/扁平上皮がん)、食道胃接合部がん(Siewert 1型)を対象とし、ECOG PS 0-1、測定可能病変(RECIST v1.1)を有する症例が適格となった。症例は化学療法(5-FU 800mg/m2, Day 1-5, 最大35サイクル+シスプラチン 80mg/m2, Day 1, 最大6サイクル:3週毎)+ペムブロリズマブ(200mg/body, 最大35サイクル:3週毎)、もしくは化学療法(同スケジュール)+プラセボに1:1で無作為割付された。割付調整因子は参加国(アジア vs アジア以外)、組織診断(扁平上皮がん vs 腺がん)、ECOG PS(0 vs 1)であった。
主要評価項目は主治医評価による無増悪生存期間(RECIST v1.1)と全生存期間、副次的評価項目は主治医評価による奏効割合(RECIST v1.1)であった(画像評価は9週毎に実施された)。(図1)
図1. 試験デザイン