JUPITER-06: A Randomized, Double-blind, Phase 3 Study of Toripalimab versus Placebo In Combination with First-Line Chemotherapy for Treatment Naive Advanced or Metastatic Esophageal Squamous Cell Carcinoma (ESCC)
First Author : Ruihua Xu, et al.
無治療進行、もしくは転移を伴う食道扁平上皮癌に対する初回化学療法に、ToripalimabもしくはPlaceboを併用した無作為化二重盲検第3相試験
背景
食道扁平上皮癌において、シスプラチンを含む化学療法は標準的な初回治療として使用されている1)。食道扁平上皮癌に対する初回治療として、パクリタキセルとシスプラチンの併用療法(TP療法)にヒトモノクローナル抗PD-1抗体であるToripalimabを追加した第1b相試験では、良好な治療効果が示された。今回、進行もしくは転移を伴う食道扁平上皮癌に対してToripalimabを併用したTP療法、無作為化二重盲検第3相試験であるJUPITAR-06(NCT03829969)の結果を報告する。
目的
進行もしくは転移を伴う食道扁平上皮癌に対する初回治療として、TP療法に対するToripalimab+ TP療法の優越性につき検証する。
対象と方法
- 組織学的に診断された、進行もしくは転移を伴う食道扁平上皮癌
- 初回治療症例
- ECOG PS;0もしくは1
- RECIST ver. 1.1で測定可能病変を有する
層別化因子
- 放射線治療歴の有無
- ECOG PS;0もしくは1
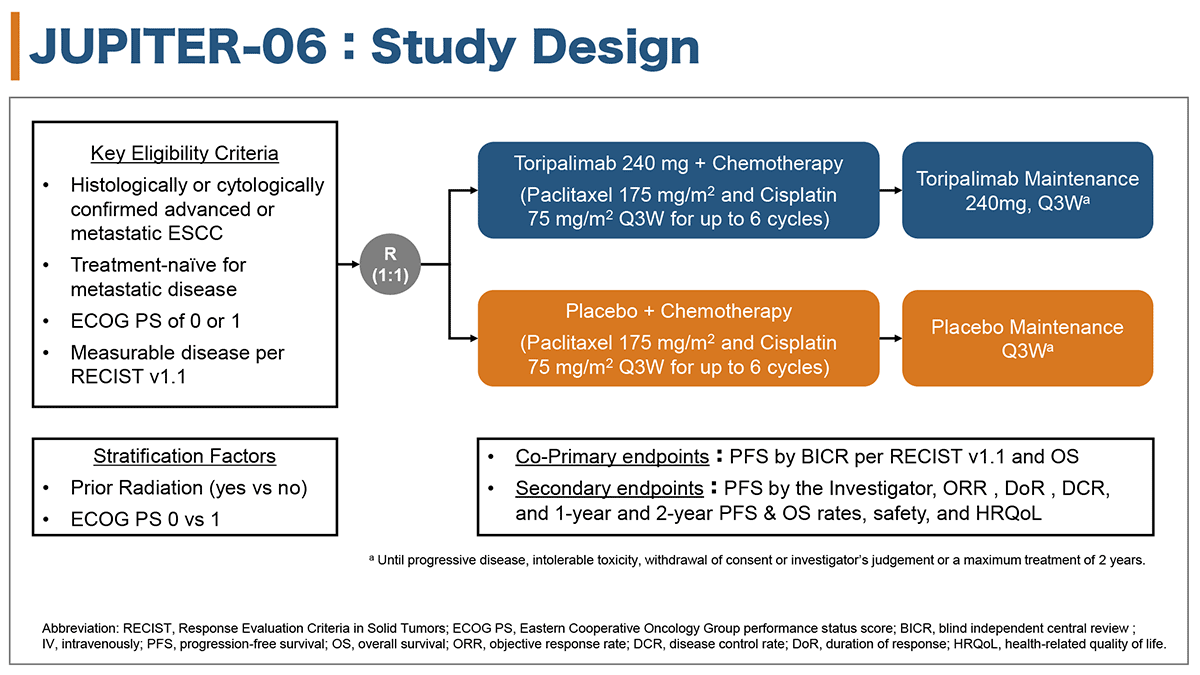
症例はToripalimab+TP療法群とPlacebo + TP療法群に、無作為に割り付けられた(図1)。Toripalimab+TP療法群ではToripalimab 240mg + パクリタキセル(PTX)175mg/m2+シスプラチン(CDDP)75mg/m2をTP療法群では、PTX175mg/m2+CDDP75mg/m2を1コース3週として6サイクルまで投与を行った。それ以降は、ToripalimabTP療法群ではToriparimab 240mg/bodyを、Placebo + TP療法群ではPlacebo薬を1コース3週として、病勢増悪または忍容できない毒性が認められるまで、最大で2年間投与を行った。
図1 研究デザインと、適格基準、主要評価項目