KRYSTAL-1: Adagrasib (MRTX849) as Monotherapy or Combined with Cetuximab (Cetux) in Patients (Pts) With Colorectal Cancer (CRC) Harboring a KRAS G12C Mutation.
First Author : Jared Weiss, et al.
KRYSTAL-1:KRAS G12C変異を有する切除不能進行大腸癌に対するAdagrasib (MRTX849) 単剤 もしくは Adagrasib+セツキシマブ併用療法の有効性を検討する第1/1b/2相試験
背景
KRAS G12C変異は切除不能進行再発大腸癌の約3-4%にみられるがん遺伝子であり、セツキシマブの負の効果予測因子であることが知られている1)-3)。KRAS蛋白はGDPが結合した不活性型とGTPが結合した活性型とが存在し、絶え間なく蛋白再合成が行われている (半減期:約24時間)4)5)。
KRAS G12C に対する共有結合阻害剤であるAdagrasibは、不活性型のGDP結合状態であるKRAS G12Cに不可逆的かつ選択的に結合する。その特徴は、半減期が24時間と長いこと、用量依存的な薬物動態、更には血液脳関門を通過することである6)。目標閾値を超える継続的なAdagrasib曝露を維持することにより、KRAS依存性のシグナル伝達の阻害が可能となり、抗腫瘍効果が最大化される。
更に、Adagrasibと抗EGFR抗体薬であるセツキシマブを併用することで、KRAS依存性シグナル伝達の阻害効果を高め、フィードバック機構による耐性化機構を克服し、治療効果を改善させる可能性が報告されている7)。
対象と方法
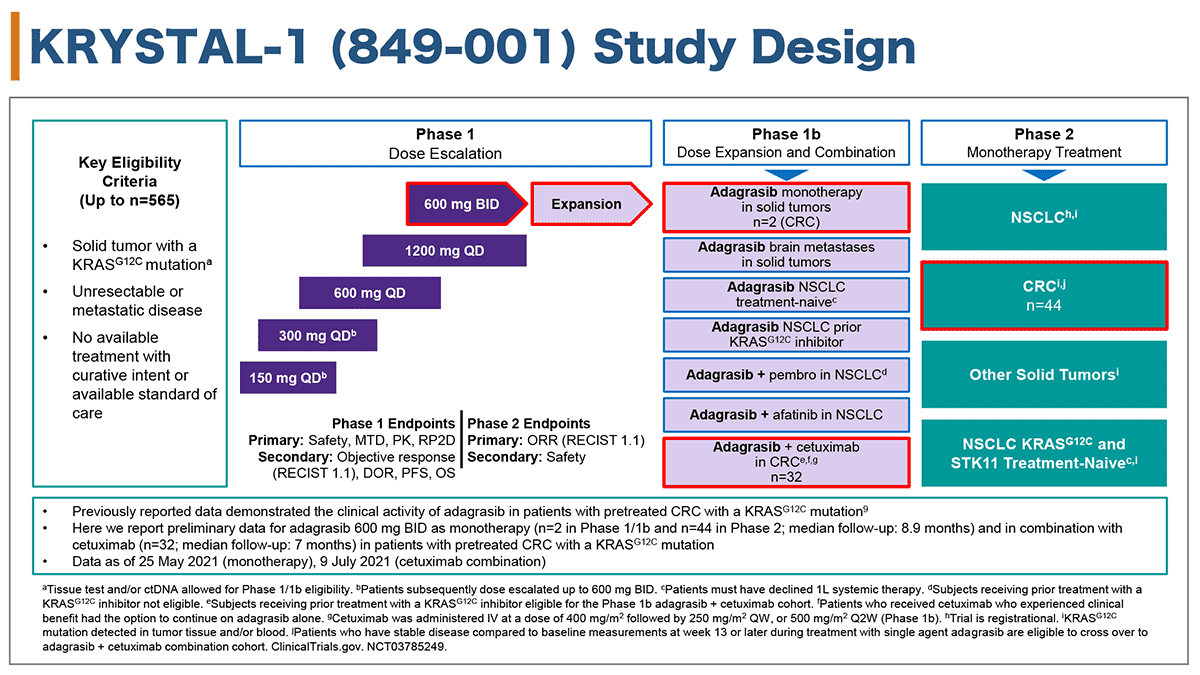
KRYSTAL-1試験は標準治療終了後のKRAS G12C 変異を有する切除不能進行・再発固形癌を対象とし、用量漸増パート(第1相)にてAdagrasibの投与量が600mg 1日2回内服と決定された (図1)。KRAS G12C 変異の確認は組織かつ/またはctDNAによる検査が許容され、第1b相におけるAdagrasib+セツキシマブ併用療法コホートではKRAS G12C 阻害剤の投与歴を有する症例も適格とされた。
今回の発表は、Adagrasib単剤療法が行われた大腸癌症例 46例 (第1/1b相 2例+第2相 44例:観察期間中央値 8.9ヶ月)、および、第1b相におけるAdagrasib+セツキシマブ併用療法コホートの大腸癌 32例(観察期間中央値 7ヶ月)について解析結果が報告された。
第1相部分の主要評価項目は安全性、最大耐用量、薬物動態および第2相部分における推奨用量の決定であり、副次的評価項目は客観的奏効割合 (RECIST v1.1)、奏効期間、無増悪生存期間、全生存期間であった。第2相部分の主要評価項目は客観的奏効割合 (RECIST v1.1)、副次的評価項目は安全性であった。
図1 KRYSTAL-1 試験デザイン