| 対象副作用 | 年, 月; 号: p-p. | 研究方法 (相) | 対象患者 | 対象薬剤 |
|---|---|---|---|---|
| 1型糖尿病 | 2019, 10:58–66. | 後ろ向き研究 | 抗PD-1抗体薬投与患者 |
背景
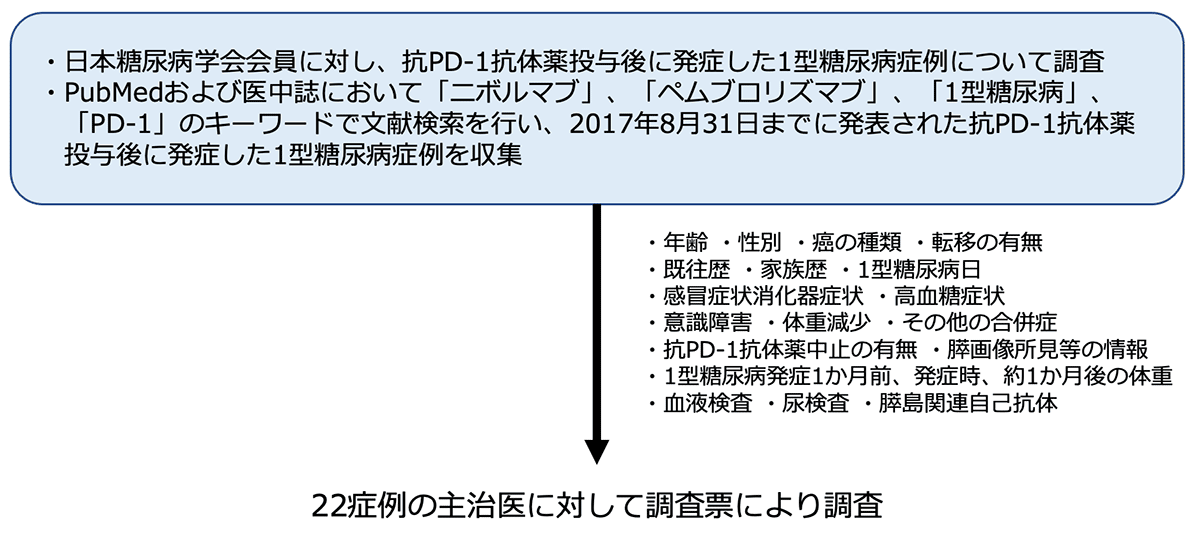
免疫チェックポイント阻害薬の投与により免疫学的機序に基づいた特有の副作用(免疫関連有害事象:irAE)を発症することがある。irAEの中でも1型糖尿病は劇症1型糖尿病の基準を満たすほど急速に進行する例が多く、治療開始の遅れや適切な治療が行われない場合は致命的となり得るため、迅速な診断と治療が必要不可欠である。抗PD-1 抗体薬投与後に発症する1型糖尿病の報告数はいまだ少なく、さらにその発症頻度や特徴には人種差があることからも、本邦における抗PD-1 抗体薬投与後に発症する1型糖尿病症例を集積し、その特徴および臨床病型を明らかにすることが求められている。そこで、文献検索および日本糖尿病学会会員に対する全国調査を行い、抗PD-1 抗体薬の投与後に発症した1型糖尿病症例の情報を収集・解析し、特徴および臨床病型の詳細を明らかにした。
シェーマ
統計学的事項
調査票による調査を行い、年齢、性別、癌の種類、転移の有無、既往歴、家族歴、1 型糖尿病発症日、感冒症状、消化器症状、高血糖症状、意識障害、体重減少、その他の合併症、抗PD-1 抗体中止の有無、膵画像所見等、1型糖尿病発症約1 ヶ月前、発症時、約1 ヶ月後の体重、血液検査、尿検査、膵島関連自己抗体について調査を実施した。
試験結果
抗PD-1抗体投与後に1型糖尿病を発症した日本人患者22症例について解析を行った結果、11例(50.0%)は劇症1型糖尿病の診断基準を満たし、その他11例(50.0%)は急性発症1型糖尿病の診断基準を満たした。本研究の22症例は全例がニボルマブ投与後に発症した症例であった。22例のうち8例(36.4%)が悪性黒色腫、10例(45.5%)が非小細胞肺癌、2例(9.1%)が腎細胞癌、1例(4.5%)がホジキンリンパ腫、1例(4.5%)が乳癌(適応外使用)であった。今回の調査結果では、先行調査の劇症1型糖尿病高齢発症群63症例と比較すると、抗PD-1抗体投与後に発症した1型糖尿病症例における自覚症状(感冒様症状、消化器症状、意識障害)の発症頻度はより低値であった。同様に、抗PD-1抗体投与後に発症した1型糖尿病では、劇症1型糖尿病高齢発症群と比較して血糖値が低く(617±248 vs. 853±362mg/dL)、HbA1cが高値を示し(8.1±1.3 vs. 7.0±0.7%)、動脈血pHも高値(7.26±0.15 vs. 7.12±0.20)であった。20例のうち17例(85.0%)がケトーシスを発症し、18例のうち7例(38.9%)が糖尿病性ケトアシドーシスを発症した。肝酵素の上昇を認めた症例はなかったが、19例のうち10例(52.6%)において発症時に1種類以上の膵外分泌酵素の上昇を認めた。初回の抗PD-1抗体投与から1型糖尿病を発症するまでの平均期間は155±123日(範囲:13日-504日)であり、多くの患者が抗PD-1抗体投与開始後7か月以内に1型糖尿病を発症していた(18/21例)。また、1型糖尿病の診断後、3例では血中C―ペプチド値はある程度維持されており、このうち1例の血中C―ペプチド値はニボルマブ中止1 週後に上昇傾向を示し、2例の血中C―ペプチド値はニボルマブ中止2-3週間後に上昇傾向を示した。しかし、その他多数の症例では、血中C―ペプチド値は1型糖尿病発症時すでに検出不可能、あるいは発症後2-3 週間で血中C―ペプチド値の減少を認め、その後に枯渇していた。
結語
抗PD-1抗体薬投与後に発症する1 型糖尿病は、劇症1型糖尿病の診断基準を満たすものから急性発症1型糖尿病の基準を満たすものまで多様な病型を呈した。発症時に糖尿病性ケトアシドーシスを発症する頻度も高く、適切な診断および治療が必要不可欠である。
論文の解釈
劇症1型糖尿病は治療が遅れると致命的となるため、早期に発見して適切な対処を行う必要がある。今回の調査により、日本人の抗PD-1抗体薬投与後に発症する1型糖尿病について、その臨床症状、膵島関連自己抗体についての情報、1型糖尿病の臨床病型が明らかとなったが、その臨床病型は劇症1型糖尿病に当てはまるものから急性発症1型糖尿病にあてはまるものまで幅広く、重症化および致死的となる原因はいまだ不明であり、更なる検討が必要である。
Cペプチド
血液検査(採血)、尿検査Cペプチドは、膵臓からインスリンが分泌されるときにインスリンにくっついて出てくるタンパク質です。その後、インスリンからは切り離されて、血液中を通った後に尿に出されます。(図:インスリンとCペプチドの関係)実際に血糖値を下げるのはインスリンであり、Cペプチドはそのかけらのようなものです。Cペプチドの量を測ると、自分の膵臓からでたインスリンの量を推測することができます。
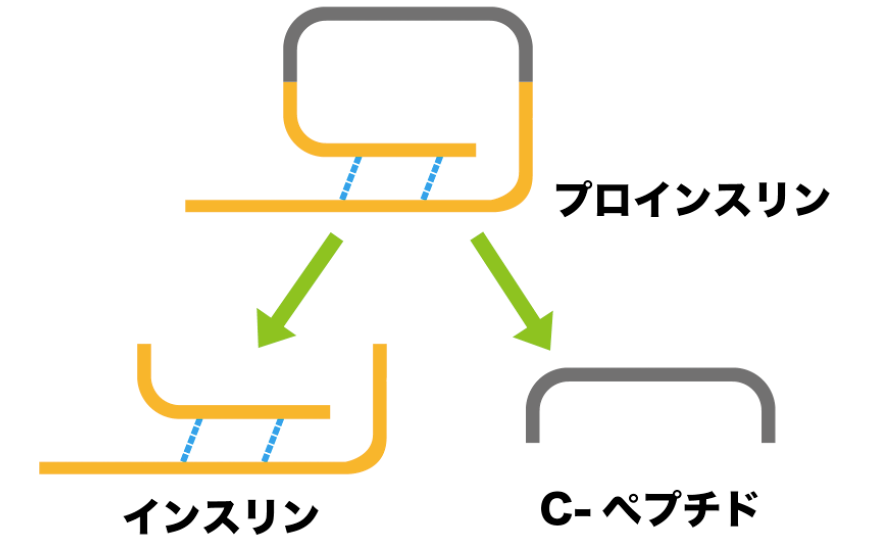
図:インスリンとCペプチドの関係
膵臓からははじめ、プロインスリンという蛋白質が出てきます。そこからCペプチドが切り離され、血糖値を下げるインスリンができます。Cペプチドはその後、尿中に捨てられてしまいます。
1型糖尿病や急性発症1型糖尿病の診断基準
表1 急性発症・緩徐進行・劇症1型糖尿病の診断基準([ ]内は参考所見)
急性発症緩徐進行(SPIDDM)劇症
| 1. 高血糖症状とケトーシ (注1) | 口渇・多飲・多尿など、高血糖症状の出現後、約3ヵ月以内にケトーシスあるいはケトアシドーシスに陥る | 糖尿病発症または診断時.ケトーシスおよびケトアシドーシスはなく、直ちにインスリン療法は必要とはならない | ロ渇・多飲・多尿など高血糖の出現後、約1週間以内にケトシスあるいはケトアシドーシスに陥る。初診時にケトーシスを認める。 |
| 2. 血糖値の状況・インス りん治療の必要性 | 糖尿病の診断早期に継続してインスリン治療を必要とする Honeymoon Period (注2) が一過性に存在する場合もある | 初期にはインスリン治療なしでも良好な血糖コントロールを得ることがしばしば可能であるが、インスリン依存状態への移行を遅延させるために、インス リン療法が有効であるといわれている | 初診時の随時血糖値が288mg/dL(16.0mmol/L)以上であり、かつHbA1cK8.7%である「インスリン治療は必須である] |
| 3. 膵島関連自己抗体 (注3) | GAD抗体、IA-2 抗体, IAA、ZnT8 抗体, ICA のうち、いずれかの陽性を経過中に確認.ただし、IAA はインスリン治療開始前に測定した場合に限る。 | 抗GAD 抗体, ICA のうち、いずれかの陽性を経過中に確認.[多くで経過中に陰性化する] | [原則陰性である] |
| 4.内因性インスリン分泌 | 膵島関連自己抗体が証明できないが、空腹時血清Cペプチド<0.6ng/mLであり、内因性インスリン分泌の欠乏が認められる。 | [自己抗体の値によらず、内因性インスリン分泌が低下しない例もある] | 発症時の尿中Cペプチド< 10 μg/日以g/日または空腹時血清Cペプチド<0.3ng/mL かつグルカゴン負荷後(または食後2時間)血清Cペプチド<0.5ng/mLである。 |
| 診断 | ・ 1.2.3を満たす場合、急性発症(自己免疫性)と診断 ・1.2.4を満たす場合.急性発症と診断 ・1.2を満たすが3.4を満た さない場合は、診断保留とし. 期間をおいて再評価 ・劇症の診断基準を満たす場合は劇症と診断 |
1.3をともに満たす場合に診断 | 1.2.4のすべてを満たすものを劇症と診断 |
| その他参考所見 | HNF-14 遺伝子異常. ミトコンドリア遺伝子異常,KCNJ11遺伝子異常などの単一遺伝子異常を除外する | インスリン依存状態に陥る前に、診断後早期からインスリン治療を開始することがある | ・1~2週間の例もある ・妊娠に関連して発症することがある ・98%で膵外分泌酵素のアミラーゼ、リパーゼ、エラスターゼ1などの上昇を認める ・70%以上で上気道症状,消化器症状を認める ・HLA DRB1 *04:05-DQB1* 04:01 との関連が認められ ている |
注1: ケトーシス:尿ケトン体陽性、血中ケトン体上昇のいずれかを認める場合に診断
注2: Honeymoon Period:診断当初、インスリン治療を施行したのち、数ヵ月間インスリン治療なしで血糖コントロールが可能な時期のこと
注3: 膵島関連自己抗体:GAD(glutamic acid decarboxylase) 抗体, IA-2(insulinoma-associated protein-2) 抗体,インスリン自己抗体(IAA).
ZnT8(zinc transporter 8) 抗体,膵島細胞抗体(ICA)を指す。
ZnT8(zinc transporter 8) 抗体,膵島細胞抗体(ICA)を指す。
日本糖尿病学会 糖尿病診療ガイドライン2019より