| 対象疾患 | 治療ライン | 研究の相 | 評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 進行消化管間質腫瘍(GIST) | 規定なし | 第3相 | 無増悪生存期間 | 欧州, 豪州, ニュージーランド, シンガポール |
なし |
試験名 :なし
レジメン:イマチニブ 400mg/日 vs イマチニブ 800mg/日
登録期間:2001年1月〜2002年1月
背景
消化管間質腫瘍 (GIST) は、軟部肉腫のサブグループであり、推定有病率は100万人あたり15〜20人である。これらの腫瘍は、腸管運動機能に重要な腸壁のカハール細胞から発生すると考えられている。GISTは、以前は平滑筋腫、または平滑筋肉腫として分類されていた。それらは従来の化学療法に抵抗性であり、一般に、KIT受容体の機能獲得変異、および場合によっては血小板由来成長因子受容体α (PDGFRα) の機能獲得変異を特徴とする。
イマチニブ (BCR-ABL、KIT、および血小板由来成長因子に対して活性を有する小分子チロシンキナーゼ阻害剤) のGISTに対する臨床的有効性は、EORTCが実施した第1相試験 (認容可能な最高用量が400mg×2回/日と決定) と第2相試験 (400〜800mg/日) で確認されている。イマチニブはGISTに対する治療薬として世界中で承認されており、推奨用量は通常400mg×1回/日とされている。しかし、認容可能な最高用量である400mg×2回/日(800mg/日)が推奨用量である400mg×1回/日よりも高い奏効割合や無増悪生存期間が得られるかどうかはわかっていない。そのため、進行再発GISTに対するイマチニブの用量、400mg×1回/日 (400mg/日) と400mg×2回/日 (800mg/日) とを比較する無作為化試験を実施した。
イマチニブ (BCR-ABL、KIT、および血小板由来成長因子に対して活性を有する小分子チロシンキナーゼ阻害剤) のGISTに対する臨床的有効性は、EORTCが実施した第1相試験 (認容可能な最高用量が400mg×2回/日と決定) と第2相試験 (400〜800mg/日) で確認されている。イマチニブはGISTに対する治療薬として世界中で承認されており、推奨用量は通常400mg×1回/日とされている。しかし、認容可能な最高用量である400mg×2回/日(800mg/日)が推奨用量である400mg×1回/日よりも高い奏効割合や無増悪生存期間が得られるかどうかはわかっていない。そのため、進行再発GISTに対するイマチニブの用量、400mg×1回/日 (400mg/日) と400mg×2回/日 (800mg/日) とを比較する無作為化試験を実施した。
シェーマ
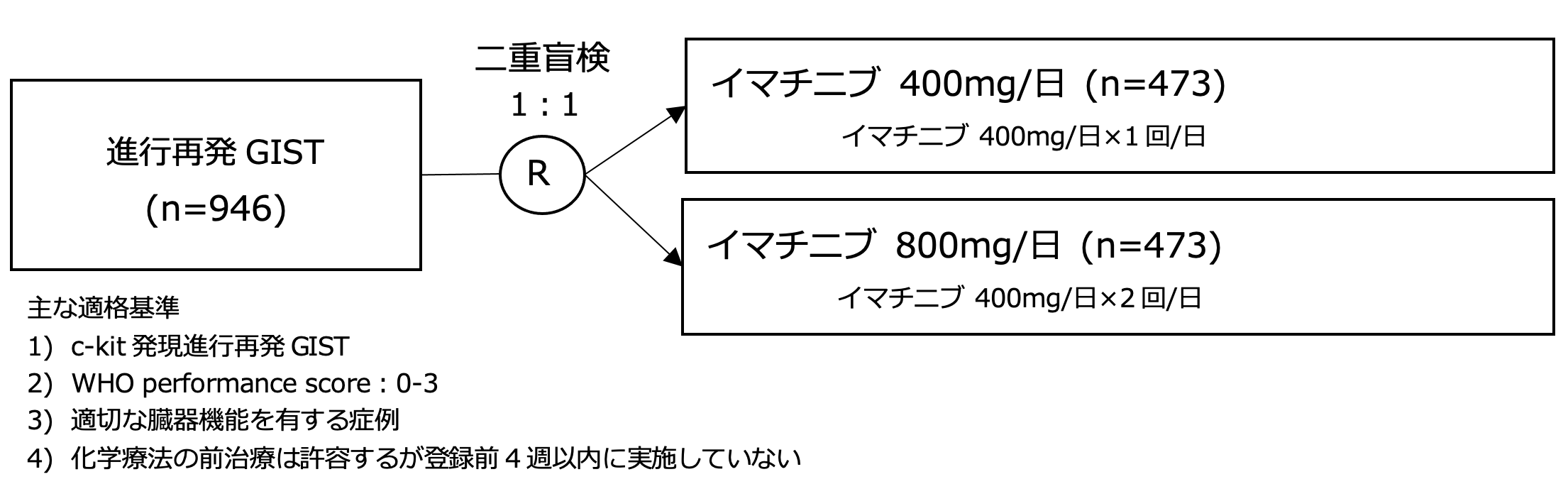
統計学的事項
主要評価項目:無増悪生存期間
副次的評価項目:全生存期間、奏効割合、安全性
400mg/日群と比較して800mg/日群の無増悪生存期間が10%改善されることを期待し (HR 0.737に対応)、α=0.05、β=0.2としたところ、レジメン間の差を検出するためには344イベントが必要と算出され、少なくとも600例の患者の登録が必要だった。試験結果:
- 2001年2月から2002年2月の間に13ヶ国56施設より946例が登録され、無作為割り付けされた (400mg/日群 n=473、800mg/日群 n=473)。
- 18例 (2%) は本研究に不適格だった (6例:重複がんあり、4例:プロトコールにて除外された合併症、8例:その他の理由)。ITT解析の方針に準じて、これらの症例も解析に含まれた。
- 本解析時点 (2004年5月) において、412例がプロトコール治療を終了していた。
1. 患者背景
| 400mg/日 (n=473) | 800mg/日 (n=473) | ||
|---|---|---|---|
| 年齢 | 中央値 (四分位範囲) | 59 (49-67) | 60 (49-68) |
| 性別 | 男性 | 283 (60%) | 290 (61%) |
| WHO performance score | 0 1 2 3 |
217 (46%) 191 (40%) 48 (10%) 17 (4%) |
219 (46%) 192 (41%) 44 (9%) 18 (4%) |
| 原発部位 | 消化管 胃 小腸 十二指腸 大網 直腸 結腸 その他の腹部 後腹膜 |
403 (85%) 159 (34%) 124 (26%) 53 (11%) 20 (4%) 21 (5%) 11 (2%) 58 (12%) 12 (2%) |
390 (82%) 157 (33%) 114 (24%) 36 (8%) 27 (6%) 23 (5%) 12 (3%) 71 (15%) 12 (3%) |
| 診断から治療に至るまでの期間 | <12ヶ月 12-24ヶ月 >24ヶ月 |
247 (52%) 83 (18%) 143 (30%) |
246 (52%) 74 (16%) 153 (32%) |
| 活動性病変 | 原発巣 肝 肺 腹水 胸水 骨 皮膚 |
149 (32%) 331 (70%) 41 (9%) 25 (6%) 13 (3%) 7 (1%) 7 (1%) |
167 (35%) 344 (73%) 39 (8%) 35 (8%) 12 (3%) 12 (3%) 4 (1%) |
| 前治療 | 手術 放射線治療 化学療法 |
410 (87%) 26 (6%) 156 (33%) |
392 (83%) 37 (8%) 155 (33%) |
- 無作為化された症例のうち、32例 (4%未満) は測定可能病変を有していなかった。
2. 投与状況
| 400mg/日(n=470) | 800mg/日(n=472) | ||
|---|---|---|---|
| 治療中断* | 189 (40%) | 302 (64%) | |
| 治療中断理由 | 血液毒性 非血液毒性 両者の重複 治療関連以外 不明 |
28 (6%) 107 (23%) 7 (1%) 38 (8%) 9 (2%) |
32 (7%) 203 (43%) 17 (4%) 42 (9%) 8 (2%) |
| 減量* | 77 (16%) | 282 (60%) | |
| 減量理由 | 血液毒性 非血液毒性 両者の重複 治療関連以外 不明 |
11 (2%) 49 (10%) 2 (1%) 7 (1%) 8 (2%) |
17 (4%) 196 (42%) 8 (2%) 27 (6%) 34 (7%) |
*p<0.0001 (カイ2乗検定)
| 400mg/日(n=470) | 800mg/日(n=472) | |
|---|---|---|
| 300mg/日以下への減量を要した症例 減量までの期間中央値 (四分位範囲) |
74 (16%) 64日 (40-172) |
41 (9%) 99日 (42-189) |
| 200mg/日以下への減量を要した症例 減量までの期間中央値 (四分位範囲) |
34 (7%) 99日 (42-189) |
21 (4%) 72日 (48-142) |
- プロトコール治療からの逸脱は155例 (16%) で報告され、その大部分はイマチニブ 800mg/日群に割り付けられた症例の不適切な減量に起因しており、155例中111例 (11%) は過少投与につながった。過小投与につながった111例の内訳は、400mg/日群が21例 (4%)、800mg/日群が90例 (19%) だった。
- プロトコール治療を中止した412例中、271例 (66%) は病勢進行によるものであり、28例 (7%) は毒性中止だった。
3. 有害事象
| 400mg/日 (n=470) | 800mg/日 (n=472) | |||||||
|---|---|---|---|---|---|---|---|---|
| Grade | 1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 |
| 全有害事象 | 98 | 215 | 123 | 29 | 41 | 190 | 201 | 36 |
| 貧血 | 257 | 128 | 26 | 7 | 195 | 187 | 55 | 24 |
| 白血球減少 | 128 | 59 | 13 | - | 138 | 77 | 10 | 2 |
| 顆粒球減少 | 96 | 63 | 20 | 13 | 89 | 81 | 22 | 11 |
| 血小板数減少 | 18 | 3 | 5 | 2 | 19 | 6 | 2 | 4 |
| 浮腫 | 236 | 86 | 13 | 1 | 200 | 169 | 41 | 2 |
| 疲労 | 201 | 90 | 28 | - | 177 | 146 | 50 | 1 |
| 発熱 | 39 | 13 | 4 | - | 60 | 15 | 6 | - |
| そう痒症 | 55 | 17 | 4 | - | 70 | 36 | 7 | - |
| 皮疹 | 80 | 34 | 11 | - | 121 | 74 | 24 | 1 |
| 食欲不振 | 76 | 37 | 8 | 1 | 119 | 63 | 8 | - |
| 便秘 | 52 | 18 | 4 | 1 | 61 | 19 | 7 | - |
| 下痢 | 160 | 58 | 7 | 1 | 170 | 73 | 25 | - |
| 悪心 | 170 | 47 | 12 | - | 170 | 101 | 15 | - |
| 嘔吐 | 86 | 25 | 12 | 1 | 107 | 60 | 13 | - |
| 出血 | 34 | 4 | 12 | 1 | 64 | 3 | 30 | 8 |
| 感染 | 34 | 34 | 12 | 1 | 41 | 36 | 21 | 1 |
| めまい | 44 | 7 | 1 | - | 50 | 9 | 2 | - |
| 関節痛 | 50 | 11 | - | - | 56 | 15 | 4 | - |
| 頭痛 | 59 | 15 | 1 | - | 54 | 8 | 4 | - |
| 筋肉痛 | 87 | 27 | 1 | - | 91 | 35 | 5 | - |
| 胸膜痛 | 159 | 60 | 19 | 2 | 143 | 83 | 33 | 1 |
| 咳嗽 | 52 | 8 | 1 | - | 53 | 13 | 1 | - |
| 呼吸困難 | - | 39 | 14 | 1 | - | 62 | 16 | 5 |
| 腎/泌尿器 | 43 | 16 | 2 | 1 | 48 | 22 | 10 | 3 |
- 有害事象は高頻度 (400mg/日群 465/470、800mg/日群 468/472) だったがほとんどが軽度だった。
- 高頻度に発生する血液学的有害事象は、貧血 (n=879, 93%)、顆粒球減少 (n=395, 42%) だった。ヘモグロビン数は400mg/日群で治療開始前と比較して8%減少し、800mg/日群では13%減少し、その後、安定した。
- 高頻度に発生する非血液学的有害事象は、浮腫 (n=748, 80%)、疲労 (n=693, 74%)、悪心 (n=515, 55%)、胸膜痛 (n=500, 53%)、下痢 (n=494, 52%)、および皮疹 (n=345, 37%) だった。
- 経時的な分析では、有害事象はほとんどが最初の8週間の間に発生していた。
- 有害事象を生じなかったのは9例 (1%) のみであり、389例 (41%) にはGrade 3-4の有害事象を生じた (400mg/日群 n=152 [32%], 800mg/日群 n=237 [50%], p<0.0001)。
- 重篤な有害事象:400mg/日群 n=174 (37%), 800mg/日群 n=180 (38%)
- 治療関連死亡は400mg/日群で2例、800mg/日群で3例認められ、肝障害と出血がその原因だった。
4. 治療群間の有害事象の違い
| Calculated p value | Adjusted p value* | |
|---|---|---|
| 浮腫 | <0.0001 | <0.0001 |
| 貧血 | <0.0001 | <0.0001 |
| 皮疹 | <0.0001 | <0.0001 |
| 疲労 | <0.0001 | <0.0001 |
| 悪心 | <0.0001 | <0.0001 |
| 出血 | <0.0001 | <0.0001 |
| 下痢 | 0.0005 | 0.0026 |
| 呼吸困難 | 0.009 | 0.036 |
| 胸膜痛 | 0.018 | 0.053 |
| 感染 | 0.12 | 0.24 |
| 顆粒球減少 | 0.42 | 0.42 |
- 浮腫、貧血、皮疹、疲労、悪心、出血、下痢、および呼吸困難は、800mg/日群で統計学的に有意に高頻度だった(*Hommel step-up法で調整)。
5. 最良腫瘍縮小
| 400mg/日(N=473) | 800mg/日(N=473) | |
|---|---|---|
| 完全奏効 | 24 (5%) | 28 (6%) |
| 部分奏効 | 213 (45%) | 229 (48%) |
| 病勢安定 | 150 (32%) | 150 (32%) |
| 病勢進行 | 61 (13%) | 42 (9%) |
| 評価不能 | 25 (5%) | 25 (5%) |
- 完全奏効までの時間中央値:210日 (四分位範囲:114-373)
- 奏効症例の最良奏効までの時間中央値:107日 (四分位範囲:58-172)
6. 無増悪生存期間
| 400mg/日(N=473) | 800mg/日(N=473) | |
|---|---|---|
| イベント | 263 (56%) | 235 (50%) |
HR 0.82 (95%信頼区間 0.69-0.98), p=0.026
- 観察期間中央値:760日 (四分位範囲:644-859)、1年追跡:n=927 (98%)、2年追跡:n=549 (58%)
- 死亡例:n=273、治療終了 (進行または死亡):n=498
- 死亡例273例のうち、215例 (79%) は現病死であり、9例 (3%) は有害事象に起因するもの、5例 (2%) は両者を判別できない死亡だった。
7. 全生存期間
| 400mg/日(N=473) | 800mg/日(N=473) | |
|---|---|---|
| 1年生存割合 | 85% | 86% |
| 2年生存割合 | 69% | 74% |
結語
奏効割合の向上のみが目的であればイマチニブ400mg/日の投与で十分であるが、イマチニブ800mg/日の方が有意に無増悪生存期間は延長する。
執筆:香川大学医学部附属病院 がんセンター/腫瘍内科 病院講師 大北 仁裕 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生