| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| ホルモン受容体陽性・HER2陰性、 腋窩リンパ節転移陰性の早期乳癌患者 |
術後 | 第3相 | 無浸潤疾患生存期間 | 国際 | なし |
試験名 :TAILORx
レジメン:(Recurrent Score: 11-25)内分泌療法単独 vs. 内分泌療法+化学療法
登録期間:2006年4月7日〜2010年10月6日
背景
Oncotype DX(Genomic Health社)は、ホルモン受容体陽性乳癌の予後を予測する多遺伝子検査の一つである。21遺伝子に基づく再発スコア(RS)は0-100で示され、31以上または26以上では化学療法の有用性が高く、0-10では内分泌療法単独の10年遠隔再発率が2%と、化学療法が不要である可能性が高い。しかし、患者の多くを占める再発スコア11-25である中程度リスクにおいて化学療法が有用であるかどうかは不明である。
以上のことから、TAILORx(Trial Assigning Individualized Options for Treatment)試験では、RS 11-25の中程度リスクを有する患者において、現在使用されている化学療法+内分泌療法に対する内分泌療法単独の有用性を検証した前向き試験である。
シェーマ
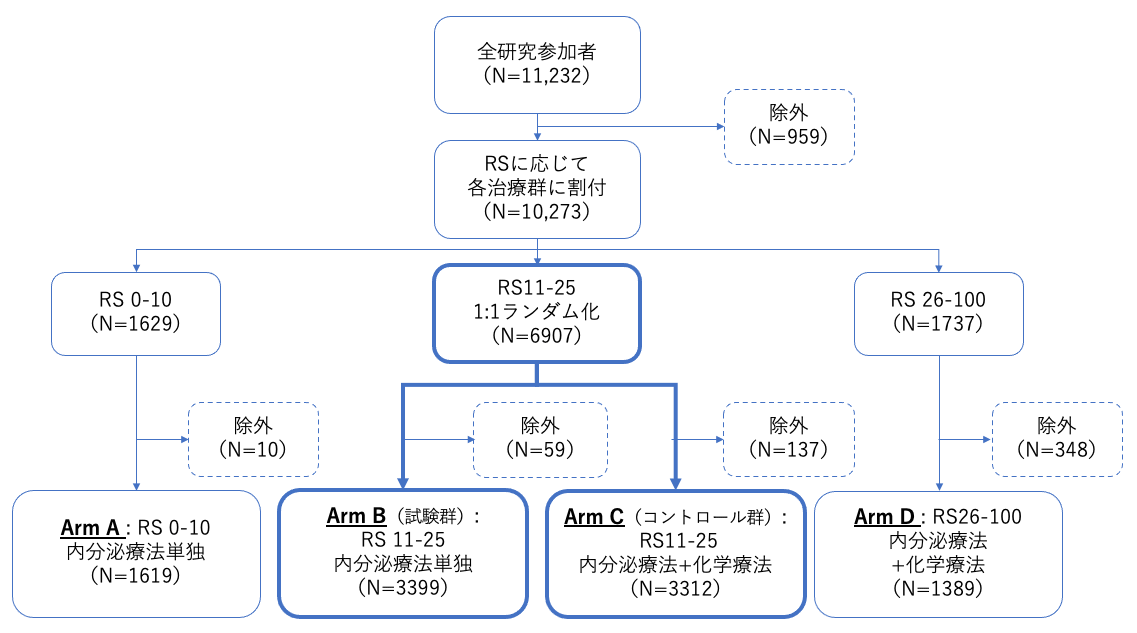
主な適格条件
- 18-75歳
- ホルモン受容体陽性、HER2陰性浸潤性乳癌
- 腋窩リンパ節転移陰性
- 根治的な手術後12週間以内
- 腫瘍径1.1-5.0 cm(T1c-T2)または、腫瘍径0.6-1.0 cm(T1b)かつ中程度以上の核グレードかつ/または組織学的グレート、または脈管侵襲あり
統計設定:
本試験は、RS 11-25の患者において、化学療法併用(標準治療)に対する内分泌療法単独(試験治療)の非劣性を検証する帰無仮説に基づいた試験で、タイプⅠエラーを片側10%、タイプⅡエラーを5%と設定した。5年無浸潤疾患生存率が化学療法併用で90%、内分泌療法単独で87%以下の場合、化学療法を行わないと、浸潤性病変の再発・二次原発がん・死亡のリスクが32.2%高くなる(ハザード比1.322)ことから、これらは許容できない値として事前に規定された。なお、初回解析で治療の非遵守率が12%と、予測の5%よりも多かったため、RS 11-25の症例数が6517例まで増加された。最終解析は必要イベント数の835例が発生した2018年3月2日に実施され、治療の非遵守率の影響を考慮し、実際に行われた治療に応じた(as-treated)解析も行われた。
試験結果:
主要評価項目:無浸潤疾患生存率(浸潤性病変の再発、二次原発がん、死亡を対象とする)
副次評価項目:無遠隔転移生存率、無遠隔転移・無局所再発生存率、全生存率
2006年4月7日から2010年10月6日に、National Comprehensive Cancer Network(NCCN)ガイドラインにおいて術後化学療法が適応となる、上記適格基準を満たす10,273例が最終的に登録され、RS 0-10の患者は内分泌療法単独(N=1619; 17%)、26以上の患者は内分泌療法+化学療法(化学療法併用、N=1389; 14%)に割付され、11-25の患者(N=6711; 69%)は内分泌療法単独(N=3399)と化学療法併用(N=3312)にランダム化割付された。RS 11-25の患者群における追跡期間中央値は、無浸潤疾患生存率で90か月、全生存率で96か月だった。
RS 11-25の患者群において、内分泌療法の期間の中央値は5.4年、5年を超えた割合は約35%で、内分泌療法単独と化学療法併用群で概ね同様だった。最も多かった化学療法は、ドセタキセル・シクロホスファミド(56%)とアントラサイクリン含有レジメン(36%)だった。また、閉経後の内分泌療法では、アロマターゼ阻害薬が最多(91%)で、閉経前ではタモキシフェンまたはタモキシフェン→アロマターゼ阻害薬が最も多く(78%)、閉経前患者のうち13%で卵巣機能抑制が併用された。治療非遵守率は、全体で11.8%、内分泌療法単独群では5.4%、化学療法併用群では18.4%だった。
主要評価項目:
RS 11-25の患者では、intention-to-treat(ITT)集団での無浸潤疾患生存率において、内分泌療法単独は化学療法併用に対して非劣性であり(ハザード比 1.08;95%信頼区間,0.94-1.24;P=0.26)、9年後の無浸潤疾患生存率は内分泌療法単独と化学療法併用でそれぞれ83.3%、84.3%だった。また、As-treated解析はITT解析と一致した結果で(無浸潤疾患生存率,ハザード比1.14;95%CI,0.99-1.31;P=0.06)、9年後の無浸潤疾患生存率は内分泌療法単独と化学療法併用でそれぞれ83.1%、84.7%だった。
副次評価項目:
RS 11-25の患者のITT集団で、内分泌療法単独は化学療法併用に対して、無遠隔転移生存率(ハザード比 1.10;95%信頼区間;P=0.48)、無遠隔転移・無局所再発生存率(ハザード比 1.11;P=0.33)、全生存率(ハザード比 0.99;P=0.89)のいずれにおいても非劣性だった。また、内分泌療法単独と化学療法併用において、9年後の無遠隔転移生存率はそれぞれ94.5%、95.0%、無遠隔転移・無局所再発生存率は92.2%、92.9%、全生存率は93.9%、93.8%だった。副次評価項目についてもAs-treated解析はITT解析と一致した結果だった(無遠隔転移生存率;ハザード比 1.03;P=0.81,無遠隔転移・無局所再発生存率;ハザード比 1.12;P=0.28,全生存率;ハザード比 0.97;P=0.78)
探索的解析:
ITT集団におけるサブグループ解析では、化学療法と予後もしくは治療効果に関わる共変量について検討された。化学療法と予後に関わる共変量(再発スコア、腫瘍径、組織学的グレード、臨床的リスク、閉経状態)との間には、有意な相互作用は認められなかった。なお、化学療法と年齢(50歳以下 vs. 51-65歳 vs. 66歳以上)では、無浸潤疾患生存率(P=0.03)、無遠隔転移・無局所再発生存率(P=0.02)において、有意な相互作用が認められた。また、治療効果については、閉経状態(前・後)と再発スコア(11-15 vs. 16-20 vs. 21-25)の6つの組み合わせと(P=0.02)、年齢と再発スコアの9つの組み合わせ(P=0.004)が検討され、無浸潤疾患生存率においては有意に異なった。さらに、50歳以下の女性では、再発スコアが16-25の場合、内分泌療法単独に対し化学療法併用では無遠隔転移再発率が低いことが示された。
21遺伝子アッセイの臨床的有用性に関するこれまでの情報に基づき、ホルモン受容体陽性、HER2陰性、腋窩リンパ節転移陰性の乳癌では、術後化学療法の使用が大幅に減少している。本試験では、21遺伝子アッセイにより、術後化学療法を省略可能な50歳以上でRS 25以下、および50歳以下でRS 15以下の患者を最大で85%特定できる可能性が示唆された。腋窩リンパ節転移陽性のホルモン受容体陽性乳癌においては、RxPONDER試験で21遺伝子アッセイの臨床的有用性が検討されている。
監修:虎の門病院 臨床腫瘍科 医長 田辺 裕子 先生