| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 大腸癌 | 二次治療以降 | 第3相試験 | 全生存期間 | 欧州、アジアなど | なし |
試験名 :20100007
レジメン:パニツムマブ単剤
登録期間:2011年11月〜2013年8月
背景
パニツムマブ(PANI)はIgG2完全ヒト型抗EGFR抗体薬であり、RAS野生型切除不能大腸癌において単剤もしくは他薬剤との併用で有効性が示されている。20100007試験はKRAS exon2野生型切除不能大腸癌を対象とし、PANI療法とbest supportive care(BSC)を比較する第3相試験である。フッ化ピリミジン系薬剤、イリノテカンおよびオキサリプラチンを含むレジメンに不応・不耐となった大腸癌を対象として行われ、PANIはBSCと比較し有意な全生存期間の延長を認めた1)。また、KRAS exon2野生型と比較しRAS野生型において全生存期間、無増悪生存期間および奏効割合が、良好な傾向を認めたが、RAS変異型では全生存期間の延長を示さなかった。
近年BRAF遺伝子は切除不能大腸癌におけるバイオマーカーとして注目されているが、PANIの効果予測因子としてのデータは少ない。また抗EGFR抗体薬のバイオマーカーを同定するための新たな臨床的な評価項目として、early tumor shrinkage(ETS)およびDepth of response(DpR)が検討されている2)-4)。しかし、抗EGFR抗体薬単剤におけるETSやDpRのデータは少ない。
そのため本論文では20100007試験の最終解析結果を報告すると共に、RAS/BRAF遺伝子型による解析およびRAS野生型におけるETSとDpRの解析を行った。
近年BRAF遺伝子は切除不能大腸癌におけるバイオマーカーとして注目されているが、PANIの効果予測因子としてのデータは少ない。また抗EGFR抗体薬のバイオマーカーを同定するための新たな臨床的な評価項目として、early tumor shrinkage(ETS)およびDepth of response(DpR)が検討されている2)-4)。しかし、抗EGFR抗体薬単剤におけるETSやDpRのデータは少ない。
そのため本論文では20100007試験の最終解析結果を報告すると共に、RAS/BRAF遺伝子型による解析およびRAS野生型におけるETSとDpRの解析を行った。
シェーマ
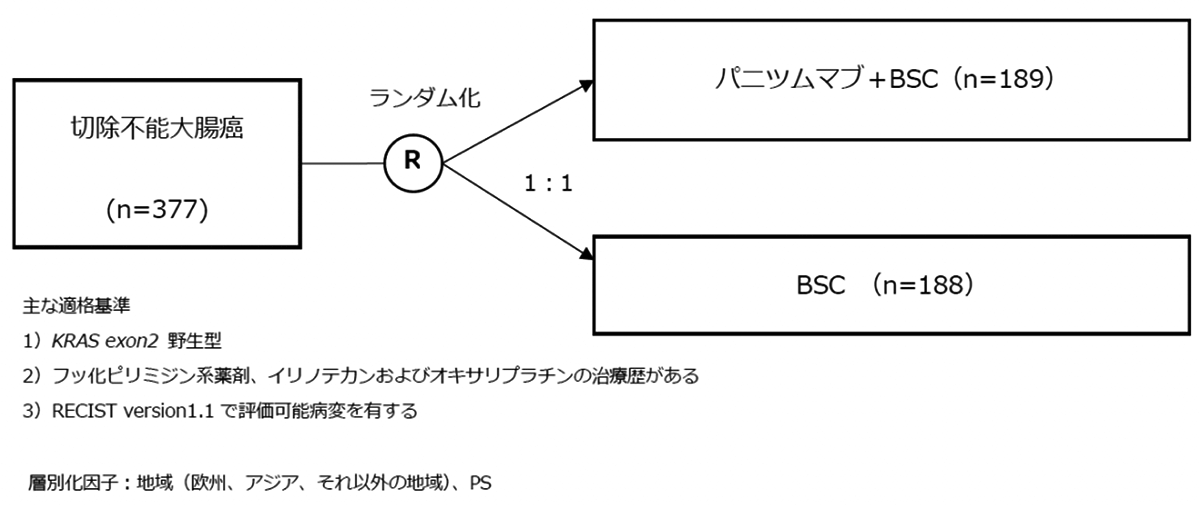
統計学的事項
主要評価項目:全生存期間
主要評価項目はKRAS exon2 野生型切除不能大腸癌における全生存期間、副次的評価項目は無増悪生存期間、奏効割合および安全性であった。RAS野生型における全生存期間、無増悪生存期間および奏効割合は副次的評価項目とした。主解析は全生存期間のイベント数が250となった時点で行われた。本最終解析は最終患者登録から2年後に行われた。解析はKRAS exon2 野生型、RAS野生型(KRAS exon2,3、NRAS exon 2,3,4)およびRAS/BRAF野生型(KRAS exon2,3、NRAS exon 2,3,4、BRAF exon15)、BRAF変異型を対象に行われた。
ETSはベースラインと8週目の画像を比較し評価を行った。DpRはベースラインから最も腫瘍が縮小した時点の腫瘍径の減少割合を評価した。ETSのカットオフ値は0%と20%とし、OSとPFSとの関連を評価した。
試験結果:
- RAS野生型およびRAS/BRAF野生型において、PANI群はBSC群と比較し有意に全生存期間および無増悪生存期間を延長した。BRAF変異型ではいずれもPANI群で良好な傾向を認めたが、有意差は認めなかった。
1. RAS野生型、RAS/BRAF野生型、BRAF変異型における全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR (95% CI)p= | ||
|---|---|---|---|---|
| RAS野生型 | PANI群(n=142) | 10ヶ月 | 8.7-11.6 | HR:0.721 (0.553-0.940) p=0.015 |
| BSC群(n=128) | 6.9ヶ月 | 5.2-7.9 | ||
| RAS/BRAF野生型 | PANI群(n=128) | 10.2ヶ月 | 8.7-11.7 | HR:0.749 (0.566-0.993) p=0.0436 |
| BSC群(n=114) | 7.4ヶ月 | 5.7-10.0 | ||
| BRAF変異型 | PANI群(n=9) | 4.1ヶ月 | 3.8-Not evaluable | HR:0.390 (0.010-1.513) p=0.1597 |
| BSC群(n=11) | 3.0ヶ月 | 1.3-4.1 |
2. RAS野生型、RAS/BRAF野生型、BRAF変異型における無増悪生存期間
| 中央値 | 95%信頼区間 | HR (95% CI)p= | ||
|---|---|---|---|---|
| RAS野生型 | PANI群(n=142) | 5.2ヶ月 | 3.5-5.3 | HR:0.452 (0.348-0.588) P<0.0001 |
| BSC群(n=128) | 1.7ヶ月 | 1.6-2.2 | ||
| RAS/BRAF野生型 | PANI群(n=128) | 5.3ヶ月 | 3.6-5.4 | HR:0.452 (0.343-0.596) P<0.0001 |
| BSC群(n=114) | 1.8ヶ月 | 1.6-2.6 | ||
| BRAF変異型 | PANI群(n=9) | 1.5ヶ月 | 0.8-3.7 | HR:0.277 (0.071-1.080) p=0.0502 |
| BSC群(n=11) | 1.3ヶ月 | 0.9-1.8 |
3. RAS野生型PANI群におけるETSと治療効果の相関
PANI群の131例でETSが評価された。ETS≧0は69.5%(n=91)の症例で、ETS≧20は38.2%(n=50)の症例で認められた。ETS≧0、ETS≧20のいずれにおいても、全生存期間および無増悪生存期間の有意な延長を認めた。またPANI群の130例でDpRが検討され、97例(75%)で腫瘍縮小を認め、DpRの中央値は16.9%であった。
・全生存期間
| 中央値 | 95%信頼区間 | HR :0.582 (0.398-0.852) p=0.005 |
|
| ETS≧20(n=50) | 13.6ヶ月 | 10.5-16.9 | |
| ETS<20(n=81) | 8.5ヶ月 | 7.1-10.6 |
| 中央値 | 95%信頼区間 | HR :0.624 (0.420-0.926) p=0.0192 |
|
| ETS≧0(n=91) | 11.5ヶ月 | 10.0-13.7 | |
| ETS<0(n=40) | 6.1ヶ月 | 4.0-10.6 |
・無増悪生存期間
| 中央値 | 95%信頼区間 | HR :0.568 (0.395-0.817) p=0.0023 |
|
| ETS≧20(n=50) | 5.4ヶ月 | 5.3-7.1 | |
| ETS<20(n=81) | 3.5ヶ月 | 2.7-5.3 |
| 中央値 | 95%信頼区間 | HR :0.389 (0.265-0.571) P<0.0001 |
|
| ETS≧0(n=91) | 5.4ヶ月 | 5.3-5.7 | |
| ETS<0(n=40) | 1.7ヶ月 | 0.9-2.8 |
4. RAS野生型における安全性
PANI群の主な有害事象は皮膚毒性と低マグネシウム血症であった。
| PANI群 (n =142) | BSC群 (n=128) | |
|---|---|---|
| 全毒性 n(%) | 138 (97.2) | 79 (61.7) |
| Grade3以上の毒性 | 56 (39.4) | 20 (15.6) |
| 皮疹 | 56 (39.4) | 1 (0.8) |
| 低マグネシウム血症 | 44 (31.0) | 1 (0.8) |
| ざ瘡様皮疹 | 40 (28.2) | 0 (0) |
| 掻痒 | 35 (24.6) | 0 (0) |
| 皮膚乾燥 | 24 (16.9) | 1 (0.8) |
| ざ瘡 | 23 (16.2) | 0 (0) |
| 爪囲炎 | 22 (15.5) | 0 (0) |
| 紅斑 | 21 (14.8) | 0 (0) |
| 腹痛 | 20 (14.1) | 18 (14.1) |
| 下痢 | 20 (14.1) | 4 (3.1) |
| 倦怠感 | 20 (14.1) | 11 (8.6) |
| 手足症候群 | 15 (10.6) | 0 (0) |
| 食欲不振 | 12 (8.5) | 16 (12.5) |
結語
PANIはRAS野生型大腸癌の治療成績を改善した。また、ETSとDpRはPANIの効果予測因子となり得る。
関連論文
1) Kim TW, Elme A, Kusic Z, et al. A phase 3 trial evaluating panitumumab plus best supportive care vs best supportive care in chemorefractory wild type KRAS or RAS metastatic colorectal cancer. Br J Cancer 2016; 115:1206-14. [Pubmed]
2) Heinemann V, Stintzing S, Modest DP, et al. Early tumour shrinkage (ETS) and depth of response (DpR) in the treatment of patients with metastatic colorectal cancer (mCRC). Eur J Cancer 2015; 51:1927-36. [Pubmed]
3) Douillard JY, Siena S, Peeters M, et al. Impact of early tumour shrinkage and resection on outcomes in patients with wild type RAS metastatic colorectal cancer. Eur J Cancer 2015; 51:1231-42. [Pubmed]
4) Cremolini C, Loupakis F, Antoniotti C, et al. Early tumor shrinkage and depth of response predict long-term outcome in metastatic colorectal cancer patients treated with first-line chemotherapy plus bevacizumab: results from phase III TRIBE trial by the Gruppo Oncologico del Nord Ovest. Ann Oncol 2015; 26:1188-94. [Pubmed]
執筆:神戸市立医療センター中央市民病院腫瘍内科 医長 松本 俊彦 先生
監修:愛知県がんセンター病院 薬物療法部 医長 舛石 俊樹 先生
監修:愛知県がんセンター病院 薬物療法部 医長 舛石 俊樹 先生