| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 大腸癌 | 一次治療 | 第3相 | 奏効割合 | 国際 | なし |
試験名 :なし
レジメン:FOLFOXIRI vs FOLFIRI
登録期間:2001年11月〜2005年4月
背景
切除不能大腸癌では5-FU/l-LVに対するイリノテカン(IRI)やオキサリプラチン(OX)の上乗せ効果が証明されており、このことは一次治療においてIntensiveな治療は無増悪生存期間(PFS)や全生存期間(OS)の延長に寄与する可能性があることを示唆している。FOLFIRI → FOLFOXもしくはFOLFIRI → FOLFOXのどちらの逐次治療を行っても5-FU、IRI、OXの3剤が投与できればOSは良好となることがGERCORから報告されており、また7つの第3相試験のpooled analysisでも同様に前述の3剤が投与できた患者のOSは良好であったが、このpooled analysisでは全体の50-80%の患者しか二次治療へ移行できなかった。
以上ことから5-FU、IRI、OXの3剤を含むレジメンを一次治療で投与可能であれば治療成績がより向上する可能性が考えられたため、FOLFOXIRIレジメンが開発された。FOLFOXIRIレジメンの第2相試験からは、FOLFOXIRIの認容性が確認されており、奏効割合(RR)は72%、OSは28.4ヶ月、PFSは10.8ヶ月と有望な結果であった。
この結果をもとにFOLFOXIRIとFOLFIRIとを比較する第3相試験が行われた。
以上ことから5-FU、IRI、OXの3剤を含むレジメンを一次治療で投与可能であれば治療成績がより向上する可能性が考えられたため、FOLFOXIRIレジメンが開発された。FOLFOXIRIレジメンの第2相試験からは、FOLFOXIRIの認容性が確認されており、奏効割合(RR)は72%、OSは28.4ヶ月、PFSは10.8ヶ月と有望な結果であった。
この結果をもとにFOLFOXIRIとFOLFIRIとを比較する第3相試験が行われた。
シェーマ
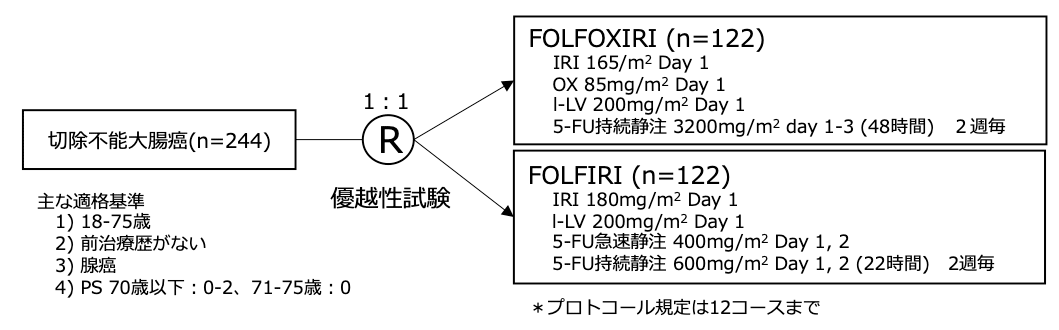
統計学的事項
主要評価項目:奏効割合
本試験の主要評価項目は奏効割合(RR)とした。FOLFIRIのRRを40%、FOLFOXIRIのRRを60%、検出力80%、両側α=0.05、10%の症例でRRが評価困難と仮定し、240例の登録が必要とされた。試験結果:
- 2001年11月〜2005年4月の期間に15施設より244例が登録された(各群122例)。
- 両群の患者背景には偏りはなかった。
- 観察期間中央値は18.4ヶ月であった。
1. 奏効割合(主要評価項目)
| 奏効割合 (各担当医判定) |
P値 | 奏効割合 (中央判定) |
P値 | |
|---|---|---|---|---|
| FOLFOXIRI(n=122) | 66% | 0.002 | 60% | <0.001 |
| FOLFIRI(n=122) | 41% | 34% |
2. 投与コース数
| 中央値 | Range | |
|---|---|---|
| FOLFOXIRI(n=122) | 11 | 1-16 |
| FOLFIRI(n=122) | 10 | 1-16 |
3. Relative Dose Intensity
| OX | IRI | 5-FU | |
|---|---|---|---|
| FOLFOXIRI(n=122) | 83% | 82% | 82% |
| FOLFIRI(n=122) | - | 87% | 86% |
4. 化学療法後に根治手術が可能となった割合
| 全体 | P値 | 肝転移限局例 | P値 | |
|---|---|---|---|---|
| FOLFOXIRI(n=122) | 15% | 0.033 | 36% | 0.017 |
| FOLFIRI(n=122) | 6% | 12% |
5. 無増悪生存期間
| 中央値 | HR 0.63 (95%C.I. 0.47-0.81) p=0.0006 |
|
| FOLFOXIRI (n=122) | 9.8ヶ月 | |
| FOLFIRI (n=122) | 6.9ヶ月 |
6. 全生存期間
| 中央値 | HR 0.70 (95%C.I. 0.50-0.96) p=0.032 |
|
| FOLFOXIRI (n=122) | 22.6ヶ月 | |
| FOLFIRI (n=122) | 16.7ヶ月 |
7. 有害事象(NCI-CTCAE Grade)
| FOLFOXIRI(n=122) | FOLFIRI(n=122) | P値 | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Grade | 1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 | 3/4 |
| 悪心 | 49(40%) | 34(28%) | 7(6%) | 0(0%) | 48(39%) | 20(16%) | 1(1%) | 0(0%) | NS |
| 嘔吐 | 24(20%) | 31(25%) | 8(7%) | 0(0%) | 28(23%) | 22(18%) | 1(1%) | 1(1%) | NS |
| 下痢 | 40(33%) | 30(25%) | 21(17%) | 4(3%) | 30(25%) | 27(22%) | 13(11%) | 1(1%) | NS |
| 口内炎 | 32(26%) | 17(14%) | 5(4%) | 1(1%) | 28(23%) | 7(6%) | 4(3%) | 0(0%) | NS |
| 神経障害 | 45(37%) | 21(17%) | 3(2%) | 0(0%) | 0(0%) | 0(0%) | 0(0%) | 0(0%) | <0.0001 |
| 無力 | 27(22%) | 19(16%) | 7(6%) | 0(0%) | 29(24%) | 12(10%) | 4(3%) | 0(0%) | NS |
| 血小板数減少 | 22(18%) | 7(6%) | 2(2%) | 0(0%) | 5(4%) | 3(2%) | 1(1%) | 0(0%) | NS |
| 貧血 | 53 (43%) | 23(19%) | 4(3%) | 0(0%) | 50(41%) | 11(9%) | 1(1%) | 0(0%) | NS |
| 好中球数減少 | 16(13%) | 24(20%) | 40(33%) | 21(17%) | 22(18%) | 16(13%) | 21(17%) | 13(11%) | 0.0006 |
| 発熱性好中球減少 | 6(5%) | 4(3%) | NS | ||||||
結語
FOLFOXIRIは切除不能大腸癌に対する一次治療においてFOLFIRIよりも高い奏効割合を示し認容性も保たれていた。
執筆:静岡県立静岡がんセンター 消化器内科 レジデント 古田 光寛 先生
監修:静岡県立静岡がんセンター 治験管理室 部長、消化器内科 医長 山﨑 健太郎 先生
監修:静岡県立静岡がんセンター 治験管理室 部長、消化器内科 医長 山﨑 健太郎 先生