| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| MSI-H/dMMR大腸癌 | 二次治療以降 | 第2相 | 奏効割合 | 国際 | あり |
試験名 :KEYNOTE-164
レジメン:ペムブロリズマブ
登録期間:2015年9月14日〜2017年9月12日
背景
DNAミスマッチ修復機能の欠損(deficiencies in DNA mismatch repair: dMMR)に起因する高頻度マイクロサテライト不安定性(MSI-H)の遺伝的特徴を有するステージIV大腸癌の頻度は約5%である。ミスマッチ修復機能が正常な(proficient mismatch repair: pMMR)大腸癌やマイクロサテライト不安定性のない(Microsatellite stable: MSS)大腸癌に比較して、MSI-H/dMMR大腸癌は従来の化学療法に抵抗性であり、治療成績は不良である。
78例のMSI-H/dMMR固形癌を対象にした初期の臨床試験において、ペムブロリズマブ(Pembro)の有効性が報告されている(奏効割合は大腸癌で52%、非大腸癌で54%)1)。また、CheckMate142試験ではMSI-H/dMMR大腸癌に対するニボルマブ単独およびニボルマブ/イピリムマブ併用療法の有効性が示された(奏効割合は31%と55%、12カ月全生存割合は73%と85%)2)。本試験では2レジメン以上(コホートA)または1レジメン以上(コホートB)の前治療歴を有するMSI-H/dMMR大腸癌を対象として、Pembroの抗腫瘍効果を検討した。
78例のMSI-H/dMMR固形癌を対象にした初期の臨床試験において、ペムブロリズマブ(Pembro)の有効性が報告されている(奏効割合は大腸癌で52%、非大腸癌で54%)1)。また、CheckMate142試験ではMSI-H/dMMR大腸癌に対するニボルマブ単独およびニボルマブ/イピリムマブ併用療法の有効性が示された(奏効割合は31%と55%、12カ月全生存割合は73%と85%)2)。本試験では2レジメン以上(コホートA)または1レジメン以上(コホートB)の前治療歴を有するMSI-H/dMMR大腸癌を対象として、Pembroの抗腫瘍効果を検討した。
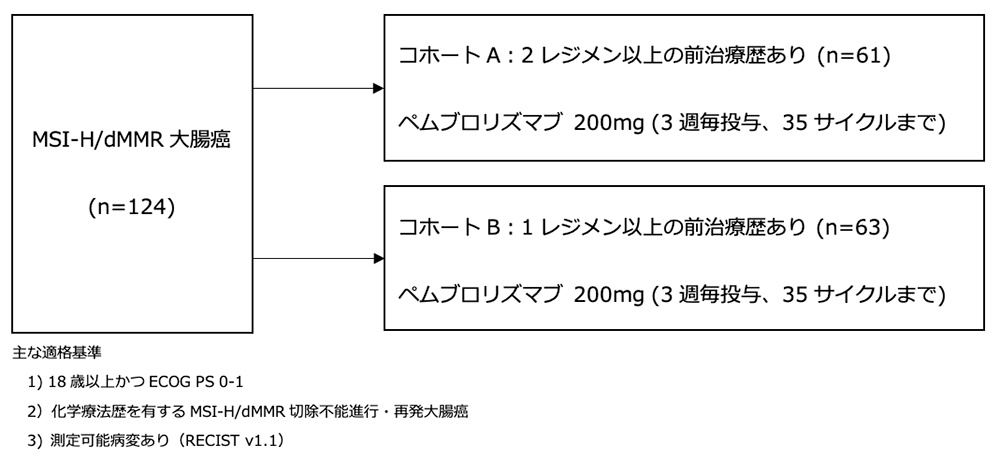
シェーマ
統計学的事項
主要評価項目:奏効割合 (中央判定:RECIST v1.1)
コホートAとBは独立して評価された。コホートAでは、客観的奏効割合(中央判定:RECIST v1.1)において、60例のサンプルサイズでPembroによる真の奏効割合を35%と想定し、Pembroの奏効割合を15%とする帰無仮説を検出力93%、片側α=0.025で棄却するように算出し、観察される奏効割合の下限が26.7%以上で統計学的に有意とした。
コホートBでは、60例のサンプルサイズで少なくとも19例の奏効例が観察されることを想定し、95%信頼区間の下限を20%と設定した。
試験結果:
- 2015年9月14日から2017年9月12日にかけて7か国、128施設からコホートA(2レジメン以上の前治療歴あり)に61症例、コホートB(1レジメン以上の前治療歴あり)に63症例が登録された。
- 観察期間中央値はコホートAで31.3ヶ月(範囲:0.2-35.6か月)、コホートBで24.2ヶ月(範囲:0.1-27.1か月)だった。
- 各コホートの患者背景はStageIV MSI-H/dMMR患者の特徴と一致していた。
- 遠隔臓器転移を有する症例は、コホートAで61例(全例)、コホートBで59例(94%)。
- 3レジメン以上の前治療歴を有する症例は、コホートAで27例(44%)、コホートBで19例(30%)。
- 2018年9月4日のデータカットオフ時点で、コホートAは全例で治療中止となっており、コホートBでは10例(16%)が治療継続中であった。
1. 客観的奏効割合(主要評価項目)
| コホートA (n=61) | コホートB (n=63) | |||
|---|---|---|---|---|
| No. (%) | [95%信頼区間] | No. (%) | [95%信頼区間] | |
| 奏効割合 | 20 (33) | [21-46] | 21 (33) | [22-46] |
| CR | 2 (3) | [0-11] | 5 (8) | [3-18] |
| PR | 18 (30) | [19-43] | 16 (25) | [15-38] |
| SD | 11 (18) | [9-30] | 15 (24) | [14-36] |
| PD | 28 (46) | [33-59] | 25 (40) | [28-53] |
| NE | 2 (3) | [0-11] | 2 (3) | [0-11] |
| 病勢制御割合 | 31 (51) | [38-64] | 36 (57) | [44-70] |
| 奏効までの期間中央値;ヶ月(範囲) | 4.3 (1.8-24.9) | 3.9 (1.8-12.5) | ||
| 奏効期間中央値;ヶ月(範囲) | 未到達 (6.2-31.3+) | 未到達 (4.4-23.6+) | ||
(+, 最終解析にてPDが観察されなかった症例)
- コホートAでは、奏効が確認された85%の症例は解析時点で奏効状態が維持されており、95%の症例は奏効期間が12ヶ月以上だった。
- コホートBでは、奏効が観察された76%の症例は解析時点でも奏効状態が維持されており、95%の症例は奏効期間が12ヶ月以上だった。
- コホートAの34例(56%)とコホートBの39例(62%)は標的病変の腫瘍径がベースラインよりも縮小した。
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | 12ヶ月生存割合 | 24ヶ月生存割合 | |
|---|---|---|---|---|
| コホートA | 2.3ヶ月 | 2.1-8.1 | 34% | 31% |
| コホートB | 4.1ヶ月 | 2.1-18.9 | 41% | 37% |
3. 全生存期間
| 中央値 | 95%信頼区間 | 12ヶ月生存割合 | 24ヶ月生存割合 | |
|---|---|---|---|---|
| コホートA | 31.4ヶ月 | 21.4-未到達 | 72% | 55% |
| コホートB | 未到達 | 19.2-未到達 | 76% | 63% |
4. 前治療レジメン数毎の奏効割合
| 前治療レジメン数 | コホートA (n=61) No./total (%) | コホートB (n=63) No./total (%) |
|---|---|---|
| 1注) | 2/6 (33) | 7/24 (29) |
| 2 | 11/28 (39) | 9/20 (45) |
| ≥3 | 7/27 (26) | 5/19 (26) |
注)術後補助化学療法歴を有する進行癌症例は前治療レジメン数1と定義した。
- 先行する前治療レジメン数に関わらずベースラインからの標的病変の縮小効果が確認された。
5. 遺伝子変異毎の奏効割合
| BRAF/RAS遺伝子のstatus | コホートA (n=61) No./total No. (%) | コホートB (n=63) No. /total No. (%) |
|---|---|---|
| BRAF野生型 | 9/28 (32) | 13/29 (45) |
| BRAF変異 | 5/9 (55) | 1/5 (20) |
| BRA未確定 | 6/24 (25) | 7/29 (24) |
| RAS野生型 | 8/19 (42) | 7/16 (44) |
| RAS変異型 | 7/19 (37) | 9/25 (36) |
| RAS未確定 | 5/23 (22) | 5/22 (23) |
- BRAF変異またはRAS変異を有する症例をコホートAで46%、コホートBで49%に認めた。
6. 有害事象
| コホートA (n=61) No. (%) | コホートB (n=63) No. (%) | |||
|---|---|---|---|---|
| 治療関連有害事象 | ||||
| 全Grade | 38 (62) | 44 (70) | ||
| Grade 3-4 | 10 (16) | 8 (13) | ||
| 治療中止に至った症例注1) | 2 (3) | 2 (3) | ||
| 治療関連死 | 0 (0) | 0 (0) | ||
| 10%以上の頻度の有害事象 | 全Grade | Grade 3-4 | 全Grade | Grade 3-4 |
| 関節痛 | 10 (16) | 1 (2) | 7 (11) | 0 (0) |
| 悪心 | 10 (16) | 0 (0) | 5 (8) | 0 (0) |
| 下痢 | 8 (13) | 0 (0) | 7 (11) | 0 (0) |
| 無力症 | 8 (13) | 1 (2) | 2 (3) | 0 (0) |
| 掻痒感 | 8 (13) | 0 (0) | 5 (8) | 0 (0) |
| 倦怠感 | 6 (10) | 2 (3) | 11 (17) | 0 (0) |
| 甲状腺機能低下 | 3 (5) | 0 (0) | 11 (17) | 0 (0) |
| 甲状腺機能亢進 | 2 (3) | 0 (0) | 7 (11) | 0 (0) |
| 免疫関連有害事象とinfusion reaction | ||||
| 全Grade | 13 (21) | 23 (37) | ||
| Grade 3-4 | 4 (7) | 2 (3) | ||
| 治療中止に至った症例注2) | 1 (2) | 2 (3) | ||
| 治療関連死 | 0 (0) | 0 (0) | ||
| 全事象 | 全Grade | Grade 3-4 | 全Grade | Grade 3-4 |
| 甲状腺機能低下 | 6 (10) | 0 (0) | 13 (21) | 0 (0) |
| 甲状腺機能亢進 | 3 (5) | 0 (0) | 7 (11) | 0 (0) |
| 膵炎 | 3 (5) | 2 (3) | 0 (0) | 0 (0) |
| 大腸炎 | 1 (2) | 0 (0) | 1 (2) | 1 (2) |
| 肝炎 | 1 (2) | 1 (2) | 0 (0) | 0 (0) |
| 筋炎 | 1 (2) | 0 (0) | 1 (2) | 0 (0) |
| 肺炎 | 3 (5) | 1 (2) | 3 (5) | 1 (2) |
| 重篤な皮膚毒性 | 1 (2) | 1 (2) | 0 (0) | 0 (0) |
| Infusion reaction | 1 (2) | 0 (0) | 1 (2) | 0 (0) |
注1)コホートAでALT高値の1例と肺炎の1例、コホートBで肺炎の2例
注2)コホートAで肺炎の1例、コホートBで肺炎の2例
結語
前治療歴を有するMSI-H/dMMR切除不能大腸癌に対するPembro単剤療法は、持続的な臨床効果を示した。Pembro単剤療法は同症例に対する重要な治療選択肢となる。
関連論文
1) Le DT, et al, Mismatch repair deficiency predicts response of solid tumors to PD-1 blockade, Science 2017;357:409-413. [Pubmed]
2) Overman MJ, et al, Nivolumab in patients with metastatic DNA mismatch repair-deficient or microsatellite instability-high colorectal cancer (CheckMate 142): An open-label, multicentre, phase 2 study, Lancet Oncol 2017;18:1182-1191. [Pubmed]
執筆:九州がんセンター 消化管外科 中島 雄一郎 先生
監修:関西医科大学付属病院 がんセンター 学長特命准教授 佐竹 悠良 先生
監修:関西医科大学付属病院 がんセンター 学長特命准教授 佐竹 悠良 先生