| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 大腸癌 | 一次治療 | 第2相試験と第3相試験の統合解析 | 最良奏効割合 無増悪生存期間 |
欧州 | なし |
試験名 :(KRAS野生型切除不能大腸癌に対する一次治療としてのセツキシマブ併用化学療法の統合解析)
レジメン:FOLFIRI+セツキシマブ、FOLFOX+セツキシマブ
登録期間:CRYSTRAL試験:2006年7月27日〜2009年8月28日
OPUS試験:2007年3月1日〜2009年8月12日
背景
切除不能大腸癌における抗EGFR抗体薬は、KRAS codon12、13に遺伝子変異のない大腸癌においてのみ、効果が認められる薬剤であることが、これまでのCRYSTAL試験、OPUS試験などの後方視的検討により、明らかになっている。更にそれら試験のアップデート解析においても、KRAS変異と治療効果における関連性が確認され、KRAS野生型大腸癌では、一次化学療法にセツキシマブ(CET)を上乗せすることで良好な治療効果が得られることが報告された。一方、BRAF変異が切除不能大腸癌の予後不良因子として注目されているものの、CET療法の効果との関連性については、明らかになっていない。今回、KRAS/BRAF変異と一次治療としてのCET併用化学療法の治療効果との関連性を明らかにするために、CRYSTAL試験およびOPUS試験の統合解析を実施するに至った。
シェーマ
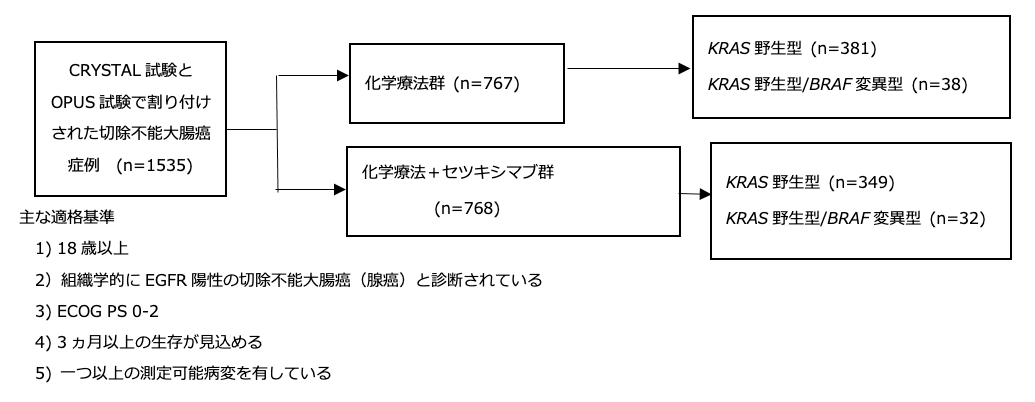
統計学的事項
主要評価項目:独立した評価委員会によるmodified WHO基準に基づく無増悪生存期間(PFS)と最良奏効割合(ORR)
本試験はCRYSTAL試験とOPUS試験の患者データを収集して実施された。Cox比例ハザードモデルにより、層別因子で調整した治療効果について検討した。生存曲線の検定には、ログランク 検定を用い、奏効割合についてはMantel-Haenszel 検定を用いた。Cox比例ハザードモデルにおける治療相互作用に関する試験間の異質性については、尤度比検定を用いて評価された。感度分析については、固定効果モデル(fixed effect)と変量効果モデル(random effects)が用いられた。試験結果:
- CRYSTAL試験とOPUS試験において1535例中1378例(90%)の症例でKRAS変異についての評価が可能であった。BRAF変異については、KRAS野生型症例845例中800例(95%)で評価可能であり、70例(9%)にBRAF変異が認められた。
- KRAS野生型/BRAF野生型症例とKRAS野生型/BRAF変異型症例の両群間の患者背景については、概ねバランスがとれていた。
- 845人の統合解析の結果では、解析法の違いに関わらず、KRAS野生型症例において、ORR、PFS、全生存期間(OS) のいずれも、化学療法(CTX)群と比較し、CTX+CET併用療法群の方が有意に良好な結果であった。
1. KRAS /BRAF変異別の治療効果
| KRASwt | KRASwt/BRAFwt | KRASwt/BRAFmt | ||||
|---|---|---|---|---|---|---|
| CTX群(n=447) | CTX+CET群(n=398) | CTX群(n=381) | CTX+CET群(n=349) | CTX群(n=38) | CTX+CET群(n=32) | |
| ORR ORR オッズ比 (95%CI) P値 Heterogeneity p値 |
38.5% 2.16 (1.6-2.86) <0.0001 0.56 |
57.3% |
40.9% 2.27 (1.08-3.07) <0.0001 0.59 |
60.7% |
13.2% 1.60 (0.45-5.67) 0.46 0.17 |
21.9% |
| PFS Median PFS (95%CI) ハザード比 (95%CI) P値 Heterogeneity p値 |
7.6ヶ月 (7.4-8.4) 0.66 (0.55-0.80) <0.0001 0.33 |
9.6ヶ月 (8.9-11.3) |
7.7ヶ月 (7.4-9.0) 0.64 (0.52-0.79) <0.0001 0.34 |
10.9ヶ月 |
3.7ヶ月 (2.1-7.9) 0.67 (0.34-1.29) 0.23 0.38 |
7.1ヶ月 (3.7-9.1) |
| OS Median OS (95%CI) ハザード比 (95%CI) P値 Heterogeneity p値 |
19.5ヶ月 (17.8-21.1) 0.81 (0.69-0.94) 0.0062 0.70 |
23.5ヶ月 (20.7-25.7) |
21.1ヶ月 (19.5-23.6) 0.84 (0.71-1.00) 0.048 0.70 |
24.8ヶ月 (22.1-27.0) |
9.9ヶ月 (5.7-13.6) 0.62 (0.36-1.06) 0.076 0.048 |
14.1ヶ月 (8.8-18.5) |
- 2つの試験間において、治療効果についての有意な異質性は認められなかった(Heterogeneity p値)。
2. 治療効果(KRAS野生型症例における統合解析)
ORR (Control: CTX+CET群)
| 試験 | 対象 | 解析法 | オッズ比 (95%CI) |
|---|---|---|---|
| 統合解析 | KRAS野生型 (n=845) KRAS野生型 (n=845) |
層別解析 非層別解析 固定効果法 変量効果法 |
2.16 (1.64-2.86) 2.14 (1.63-2.82) 2.16 (1.64-2.85) 2.16 (1.64-2.85) |
| CRYSTAL試験 | KRAS野生型 (n=666) | 層別解析 | 2.07 (1.52-2.83) |
| OPUS試験 | KRAS野生型 (n=179) | 層別解析 | 2.55 (1.38-4.72) |
PFS (Control: CTX群)
| 試験 | 対象 | 解析法 | オッズ比 (95%CI) |
|---|---|---|---|
| 統合解析 | KRAS野生型 (n=845) KRAS野生型 (n=845) |
層別解析 非層別解析 固定効果法 変量効果法 |
0.66 (0.55-0.80) 0.65 (0.54-0.79) 0.67 (0.55-0.81) 0.67 (0.55-0.81) |
| CRYSTAL試験 | KRAS野生型 (n=666) | 層別解析 | 0.70 (0.56-0.87) |
| OPUS試験 | KRAS野生型 (n=179) | 層別解析 | 0.57 (0.38-0.86) |
OS (Control: CTX群)
| 試験 | 対象 | 解析法 | オッズ比 (95%CI) |
|---|---|---|---|
| 統合解析 | KRAS野生型 (n=845) KRAS野生型 (n=845) |
層別解析 非層別解析 固定効果法 変量効果法 |
0.81 (0.69-0.94) 0.80 (0.69-0.93) 0.81 (0.69-0.94) 0.81 (0.69-0.94) |
| CRYSTAL試験 | KRAS野生型 (n=666) | 層別解析 | 0.80 (0.67-0.95) |
| OPUS試験 | KRAS野生型 (n=179) | 層別解析 | 0.85 (0.60-1.22) |
- 層別解析では、層別化因子としてECOG PSが用いられた。
- 治療効果に関する感度解析結果においては、どの分析手法を用いても、これまでに示されていたKRAS野生型に対するCETの良好な上乗せ効果が再確認される結果であった。
3. 無増悪生存期間(KRAS野生型症例におけるレジメン別の統合解析)
| イベント数 | 中央値 | 95%信頼区間 | |
|---|---|---|---|
| CTX群 (n=447) | 251 | 7.6ヶ月 | 7.4-8.4 |
| CTX+CET群 (n=398) | 184 | 9.6ヶ月 | 8.9-11.3 |
BRAF変異別の無増悪生存期間
| BRAF mt CTX群(n=38) | BRAF mt CTX+CET群(n=32) | BRAF wt CTX群(n=381) | BRAF wt CTX+CET群(n=349) | |
|---|---|---|---|---|
| イベント数 | 24 | 17 | 211 | 155 |
| 無増悪生存期間中央値(95%CI) | 3.7ヶ月(2.1-7.9) | 7.1ヶ月(3.7-9.1) | 7.7ヶ月(7.4-9.0) | 10.9ヶ月(9.2-11.9) |
4. 全生存期間 (KRAS野生型症例におけるレジメン別の統合解析)
| イベント数 | 中央値 | 95%信頼区間 | |
|---|---|---|---|
| CTX群 (n=447) | 359 | 19.5ヶ月 | 17.8-21.1 |
| CTX+CET群 (n=398) | 297 | 23.5ヶ月 | 20.7-25.7 |
BRAF遺伝子変異別の全生存期間
| BRAF mt CTX群(n=38) | BRAF mt CTX+CET群(n=32) | BRAF wt CTX群(n=381) | BRAF wt CTX+CET群(n=349) | |
|---|---|---|---|---|
| イベント数 | 38 | 26 | 295 | 255 |
| 無増悪生存期間中央値(95%CI) | 9.9ヶ月(5.7-13.6) | 14.1ヶ月(8.8-18.5) | 21.1ヶ月(19.5-23.6) | 24.8ヶ月(22.1-27.0) |
- KRAS野生型症例(n=845)に関しては、CTX+CET群において、PFSとOSの統計学的に有意な延長効果が認められた(PFS: HR=0.66, p=0.001、OS: HR=0.81, p=0.0062)。
- BRAF変異型症例(n=70)に関しては、CTX+CET群において、PFSとOSは、CTX群と比較し、延長傾向を認めたものの、統計学的有意差は認められない結果であった (PFS: HR=0.67、OS: HR=0.62)。
結語
今回の統合解析によって、KRAS 野生型切除不能大腸癌に対する一次治療としてのCTX+CET併用療法群の治療効果(PFS、ORR、OS)は、CTX群と比較し、有意に良好な結果であった。過去に実施されたCRYSTALおよびOPUS試験の解析結果において、既に示されていたCTX+CET併用化学療法の良好な治療効果が、本統合解析で再確認された。また、BRAF 変異症例におけるCTX+CET併用療法群の治療効果に関しては、CTX群と比較し良好な傾向を認めるものの統計学的な差は認められず、本解析結果においては、BRAF 変異は、予後不良因子ではあるものの、効果予測因子ではないことが結論付けられた。
関連論文
・ Bokemeyer C, Bondarenko I, Hartmann JT, et al. Efficacy according to biomarker status of cetuximab plus FOLFOX-4 as first-line treatment for metastatic colorectal cancer: the OPUS study. Ann Oncol. 2011 ;22:1535-1546.[Pubmed]
・ Van Cutsem E, Lenz HJ, Köhne CH, et al. Fluorouracil, leucovorin, and irinotecan plus cetuximab treatment and RAS mutations in colorectal cancer. J Clin Oncol. 2015;33:692-700. [Pubmed]
執筆:大阪医療センター 消化器内科 医師 長谷川 裕子 先生
監修:愛知県がんセンター病院 薬物療法部 医長 坂東 英明 先生
監修:愛知県がんセンター病院 薬物療法部 医長 坂東 英明 先生