| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 大腸癌 | 一次治療 | 第3相 | 無増悪生存期間 | 国内 | あり |
試験名 :TRICOLORE
レジメン:S-1+IRI+Bev vs mFOLFOX6/CapeOX+Bev
登録期間:2012年6月〜2014年9月
背景
切除不能大腸癌初回治療において、S-1+IRI+Bevの3週レジメン、4週レジメンそれぞれで第2相試験で有望な結果を示した。これらの結果をもとにmFOLFOX6/CapeOX+Bevに対するS-1+IRI+Bevの第3相試験(TRICOLORE試験)が行われた。 [UMIN-CTR (http://www.umin.ac.jp/ctr/) (000007834)]
シェーマ
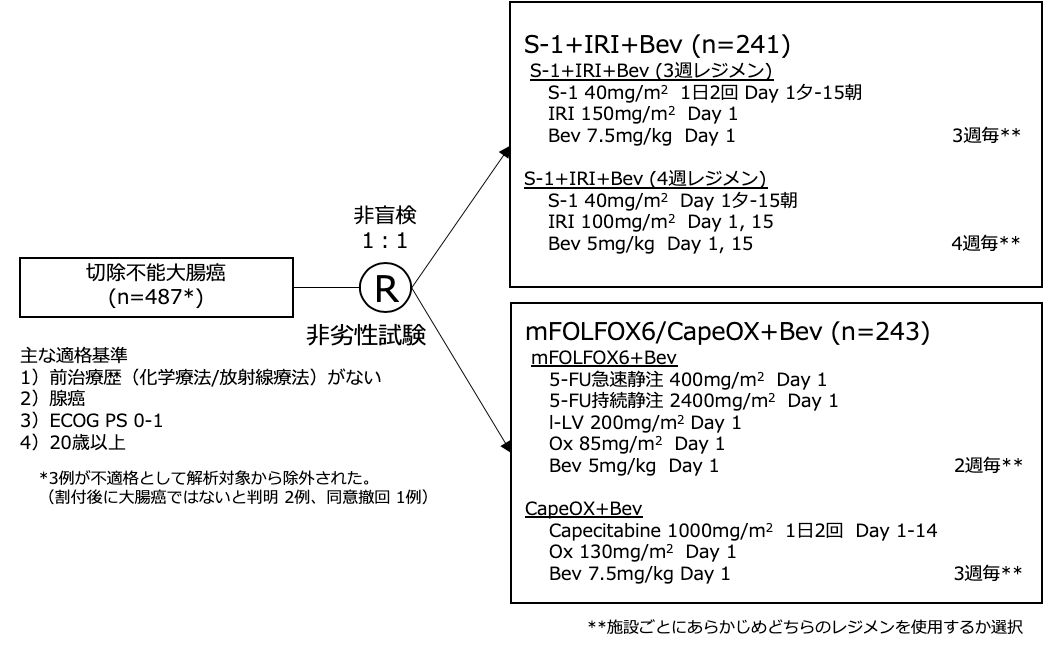
統計学的事項
主要評価項目:無増悪生存期間
本試験は主要評価項目を無増悪生存期間(PFS)とした非劣性試験である。PFSの中央値をS-1+IRI+Bev群 12ヶ月、 mFOLFOX6/CapeOX+Bev群 11ヶ月(HR=0.917)、非劣性マージンを1.25、検出力85%、片側α=0.025と設定すると、450例の登録・374イベントが必要とされた。試験結果:
- 2012年6月〜2014年9月の間に487例が国内53施設から登録され、除外された3例を除く484例(S-1+IRI+Bev群241例、 mFOLFOX6/CapeOX+Bev群243例)が解析対象となった。
- 両群の患者背景には偏りはなかった。
- データカットオフ日は2016年4月30日。フォローアップ期間中央値は32.4ヶ月(range 1.5-46.6ヶ月)であった。
1. 無増悪生存期間(主要評価項目)
| 中央値 | 95%CI | HR 0.84 (95%C.I. 0.70-1.02) p<0.0001:非劣性 p=0.0815:優越性 |
|
| S-1+IRI+Bev(n=241) | 14.0ヶ月 | 12.4-15.5 | |
| mFOLFOX6/CapeOX+Bev(n=243) | 10.8ヶ月 | 9.6-11.6 |
2. 増悪までの期間
| 中央値 | 95%CI | HR 0.71 (95%C.I. 0.59-0.85) p=0.0002 |
|
| S-1+IRI+Bev(n=241) | 9.6ヶ月 | 8.2-11.0 | |
| mFOLFOX6/CapeOX+Bev(n=243) | 7.7ヶ月 | 7.1-8.2 |
3. 奏効割合
| 奏効割合 | p=0.34 | |
| S-1+IRI+Bev | 66.4% | |
| mFOLFOX6/CapeOX+Bev | 70.6% |
4. 全生存期間
| 中央値 | 95%信頼区間 | HR 0.86 (95%C.I. 0.66-1.13) p=0.2841 |
|
| S-1+IRI+Bev | 34.9ヶ月 | 31.9-42.4 | |
| mFOLFOX6/CapeOX+Bev | 33.6ヶ月 | 29.8-40.1 |
5. QOL評価
治療開始前にQOL質問票の回答を得ていた436例(90.6%)で治療前後のQOLスコアの比較を行った。
FACT-C TOI score では、S-1+IRI+Bev群とmFOLFOX6/CapeOX+Bev群との間で有意差は認められなかったが、FACCT/GOG-Ntx scoreではS-1+IRI+Bev群の方が有意に良好であった(p<0.01)。
6. 有害事象(CTCAE ver.4.0)
| S-1+IRI+Bev(n=239) | mFOLFOX6/CapeOX+Bev(n=242) | P値 (Grade 3以上の比較) |
|||
|---|---|---|---|---|---|
| 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | ||
| 白血球数減少 | 157 (65.7%) | 21 (8.8%) | 154 (63.6%) | 6 (2.5%) | <0.01 |
| 好中球数減少 | 150 (62.8%) | 58 (24.3%) | 139 (57.4%) | 33 (13.6%) | <0.01 |
| 血小板数減少 | 74 (31.0%) | 2 (0.8%) | 151 (62.4%) | 4 (1.7%) | 0.69 |
| 貧血 | 121 (50.6%) | 12 (5.0%) | 92 (38.0%) | 5 (2.1%) | 0.09 |
| 発熱性好中球減少 | 8 (3.3%) | 8 (3.3%) | 0 (0.0%) | 0 (0.0%) | <0.01 |
| 口内炎/粘膜炎 | 128 (53.6%) | 7 (2.9%) | 104 (43.0%) | 4 (1.7%) | 0.38 |
| 食欲不振 | 143 (59.8%) | 16 (6.7%) | 149 (61.6%) | 16 (6.6%) | 1.00 |
| 悪心 | 136 (56.9%) | 8 (3.3%) | 119 (49.2%) | 9 (3.7%) | 1.00 |
| 嘔吐 | 59 (24.7%) | 5 (2.1%) | 37 (15.3%) | 4 (1.7%) | 0.75 |
| 下痢 | 149 (62.3%) | 32 (13.4%) | 109 (45.0%) | 16 (6.6%) | 0.02 |
| 手足症候群 | 59 (24.7%) | 2 (0.8) | 125 (51.7%) | 15 (6.2%) | <0.01 |
| 末梢神経障感覚 ニューロパチー |
47 (19.7%) | 0 (0.0%) | 223 (92.1%) | 53 (21.9%) | <0.01 |
Post hoc analysisでは、S-1+IRI+Bev群におけるGr≧3の下痢の頻度がCCr ≧70ml/minの患者で11.5%であったのに対しCCr<70ml/minでは19.6%に認められた。
監修:静岡県立静岡がんセンター 治験管理室 部長、消化器内科 医長 山﨑 健太郎 先生