| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 食道扁平上皮癌 | 二次治療 | 第3相 | 全生存期間 | 国際 | あり |
試験名 :ATTRACTION-3
レジメン:ニボルマブ vs 化学療法 (ドセタキセル or パクリタキセル)
登録期間:2016年1月〜2017年5月
背景
進行食道扁平上皮がんに対する緩和的化学療法の有用性は十分に確立していない。
フッ化ピリミジンと白金製剤の併用療法は切除不能進行/再発食道扁平上皮がんに対する一次化学療法として広く受け入れられている。パクリタキセル/ドセタキセルは一次化学療法で不応となった症例に対する二次治療として用いられているが、血液毒性/消化器毒性/神経障害が問題となり、長期生存例も乏しい。
PD-1阻害薬の抗腫瘍活性は食道がん、頭頚部がん、非小細胞肺がん、肛門管がんといった扁平上皮癌を含むいくつかの試験で報告されており、米国FDAでは2019年、PD-L1発現を認める局所進行/転移性食道扁平上皮がんの二次治療以降に抗PD-1抗体薬であるペムブロリズマブを承認した。
同じく抗PD-1抗体薬であるニボルマブはフッ化ピリミジン、白金製剤、タキサン系抗がん剤に不応/不耐となった食道扁平上皮がん症例を対象として、第2相試験(ATTRACTION-1試験)を実施し、良好な有効性と安全性を示している。この結果を受け、フッ化ピリミジン/白金製剤に不応/不耐となった食道扁平上皮癌症例を対象として、二次治療におけるニボルマブと化学療法の有効性、安全性を比較検討する国際共同非盲検比較第3相試験(ATTRACTION-3試験)が実施された。
フッ化ピリミジンと白金製剤の併用療法は切除不能進行/再発食道扁平上皮がんに対する一次化学療法として広く受け入れられている。パクリタキセル/ドセタキセルは一次化学療法で不応となった症例に対する二次治療として用いられているが、血液毒性/消化器毒性/神経障害が問題となり、長期生存例も乏しい。
PD-1阻害薬の抗腫瘍活性は食道がん、頭頚部がん、非小細胞肺がん、肛門管がんといった扁平上皮癌を含むいくつかの試験で報告されており、米国FDAでは2019年、PD-L1発現を認める局所進行/転移性食道扁平上皮がんの二次治療以降に抗PD-1抗体薬であるペムブロリズマブを承認した。
同じく抗PD-1抗体薬であるニボルマブはフッ化ピリミジン、白金製剤、タキサン系抗がん剤に不応/不耐となった食道扁平上皮がん症例を対象として、第2相試験(ATTRACTION-1試験)を実施し、良好な有効性と安全性を示している。この結果を受け、フッ化ピリミジン/白金製剤に不応/不耐となった食道扁平上皮癌症例を対象として、二次治療におけるニボルマブと化学療法の有効性、安全性を比較検討する国際共同非盲検比較第3相試験(ATTRACTION-3試験)が実施された。
シェーマ
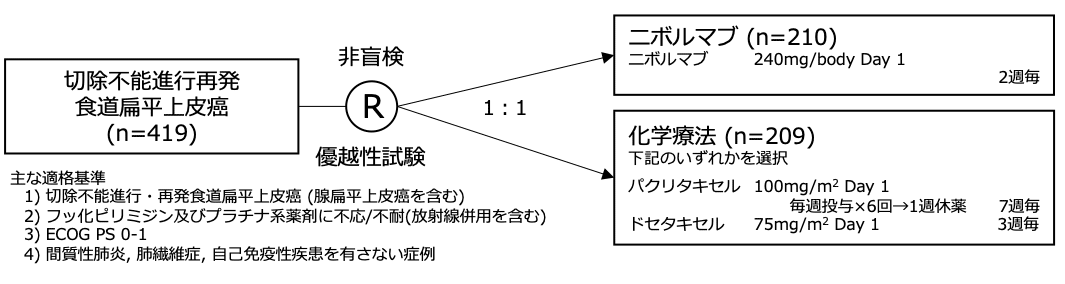
統計学的事項
主要評価項目:全生存期間
本試験は地域(日本 vs それ以外)、転移臓器個数(≤1 vs ≥2)、PD-L1発現(<1% vs ≥1%)を割付調整因子として1:1に無作為割付された。本試験は化学療法群を対照としてニボルマブ群の全生存期間のハザード比が0.70となることを検証する優越性試験として設計され、検出力90%、両側α=0.05として390例の登録、331の死亡イベントが必要とされた。
本試験の登録期間は16ヶ月、最終症例登録後18ヶ月の追跡を行うこととして計画された。
試験結果:
- 2016年1月から2017年5月の間に590例が適格性評価を受け、419例がランダム化された(210例 ニボルマブ群、209例 化学療法群)。
- ニボルマブ群の1例(死亡)、化学療法群の1例(同意撤回)が実際の治療を受けなかった。
- データカットオフは2018年11月12日で、全生存期間に関する観察期間中央値はニボルマブ群で10.5ヶ月(四分位範囲 4.5-19.0)、化学療法群で8.0ヶ月(四分位範囲 4.6-15.2)であった。
- 患者背景は両群間で偏りがなかった。
- 全症例が扁平上皮がんで、アジア人が96%(401/419)であった。
- 49%(205/419)が手術歴、70%(295/419)が放射線照射歴を有していた。
- ほぼ半数の症例(ニボルマブ群 48%/化学療法群 49%)で腫瘍部のPD-L1発現(≥1%)を認めた
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.77 (95%C.I. 0.62-0.96) p=0.019 |
|
| ニボルマブ | 10.9ヶ月 | 9.2-13.3 | |
| 化学療法 | 8.4ヶ月 | 7.2-9.9 |
2. 12ヶ月/18ヶ月生存割合
| 12ヶ月生存割合 | 95%信頼区間 | 18ヶ月生存割合 | 95%信頼区間 | |
|---|---|---|---|---|
| ニボルマブ | 47% | 40-54 | 31% | 24-37 |
| 化学療法 | 34% | 28-41 | 21% | 15-27 |
3. 奏効割合 (ニボルマブ n=171 / 化学療法 n=158)
| CR | PR | SD | PD | NE | 奏効割合 | 95%信頼区間 | |
|---|---|---|---|---|---|---|---|
| ニボルマブ | 1 | 32 | 31 | 94 | 13 | 19% | 14-26 |
| 化学療法 | 2 | 32 | 65 | 51 | 8 | 22% | 15-29 |
4. 病勢制御割合/奏効期間 (ニボルマブ n=171/ 化学療法 n=158)
| 病勢制御割合 | 95%信頼区間 | 奏効期間 中央値 | 95%信頼区間 | |
|---|---|---|---|---|
| ニボルマブ | 37% | 30-45 | 6.9ヶ月 | 5.4-11.1 |
| 化学療法 | 63% | 55-70 | 3.9ヶ月 | 2.8-4.2 |
- データカットオフの時点でニボルマブ群の7名、化学療法群の2例は治療効果が継続していた。
- 奏効までの期間中央値(四分位範囲)は、ニボルマブ群 2.6ヶ月(1.5-2.8)、化学療法群 1.5ヶ月(1.4-1.7)、治療期間中央値(四分位範囲)は、ニボルマブ群 2.6ヶ月(1.0-6.1)、化学療法群 2.6ヶ月(1.2-4.2)であった。
- 相対用量強度 中央値(四分位範囲)は、ニボルマブ群 100%(92-100)、化学療法群 81%(68-96)であった。
5. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 1.08 (95%C.I. 0.87-1.34) | |
| ニボルマブ | 1.7ヶ月 | 1.5-2.7 | |
| 化学療法 | 3.4ヶ月 | 3.0-4.2 |
6. 6ヶ月/12ヶ月無増悪生存割合(PFS割合)
| 6ヶ月PFS割合 | 95%信頼区間 | 12ヶ月PFS割合 | 95%信頼区間 | |
|---|---|---|---|---|
| ニボルマブ | 24% | 19-30 | 12% | 8-17 |
| 化学療法 | 17% | 12-23 | 7% | 4-12 |
7. 治療関連有害事象 (CTCAE ver.4.0)
| N(%) | ニボルマブ (n=209) | 化学療法 (n=208) | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Grade | 1-2 | 3 | 4 | 5 | 1-2 | 3 | 4 | 5 | |
| 全事象 | 99 (47) | 33 (16) | 5 (2) | 0 | 65 (31) | 85 (41) | 46 (22) | 2 (1) | |
| 重篤な有害事象 | 13 (6) | 16 (8) | 4 (2) | 0 | 6 (3) | 31 (15) | 8 (4) | 2 (1) | |
| 治療中止に至った事象 | 10 (5) | 8 (4) | 0 | 0 | 6 (3) | 9 (4) | 3 (1) | 1 (<1) | |
| 死亡に至った事象 | 0 | 2 (1) | 0 | 0 | 0 | 1 (<1) | 0 | 2 (1) | |
| 皮疹 | 22 (11) | 1 (1<) | 0 | 0 | 29 (14) | 2 (1) | 0 | 0 | |
| 下痢 | 20 (10) | 2 (1) | 0 | 0 | 18 (9) | 2 (1) | 0 | 0 | |
| 食欲不振 | 14 (7) | 2 (1) | 0 | 0 | 46 (22) | 10 (5) | 0 | 0 | |
| 疲労 | 14 (7) | 1 (<1) | 0 | 0 | 34 (16) | 9 (4) | 0 | 0 | |
| 倦怠感 | 9 (4) | 0 | 0 | 0 | 45 (22) | 0 | 0 | 0 | |
| 口腔粘膜炎 | 4 (2) | 1(<1) | 0 | 0 | 24 (12) | 1(<1) | 0 | 0 | |
| 悪心 | 4 (2) | 0 | 0 | 0 | 33 (16) | 1(<1) | 0 | 0 | |
| 脱毛 | 3 (1) | 0 | 0 | 0 | 98 (47) | 0 | 0 | 0 | |
| 関節痛 | 3 (1) | 0 | 0 | 0 | 20 (10) | 1 (<1) | 0 | 0 | |
| 好中球数減少 * | 3 (1) | 1 (<1) | 0 | 0 | 28 (13) | 47 (23) | 41 (20) | 0 | |
| 貧血 | 1 (<1) | 4 (2) | 0 | 0 | 30 (14) | 19 (9) | 0 | 0 | |
| 白血球減少 | 1 (<1) | 1 (<1) | 0 | 0 | 26 (13) | 32 (15) | 14 (7) | 0 | |
| 末梢性感覚ニューロパチー ** | 1 (<1) | 0 | 0 | 0 | 67 (32) | 2 (1) | 0 | 0 | |
| 発熱性好中球減少症 | 0 | 0 | 0 | 0 | 0 | 18 (9) | 4 (2) | 0 | |
* 好中球数減少:「Neutrophil count decreased」と「Neutropenia」の合算、** 末梢性感覚ニューロパチー:「Peripheral sensory neuropathy」と「Neuropathy peripheral」の合算
- 重篤な有害事象(全Grade)で高頻度の事象・・・ニボルマブ群:発熱(5例, 2%)・間質性肺疾患(4例, 2%)、化学療法群:発熱性好中球減少症(16例, 8%)・食欲不振(6例, 3%)。
- 治療中止に至った治療関連有害事象(全Grade)で高頻度の事象・・・両群とも間質性肺疾患(ニボルマブ群 5例/2%、化学療法群 3例/1%)と肺炎(ニボルマブ群 4例/2%、化学療法群 2例/1%)が高頻度
- 治療関連有害事象による投与延期はニボルマブ群(全Grade 34例/16%, Grade 3-4 15例/7%)より化学療法群(全Grade 104例/50%, Grade 3-4 81例/39%)で高頻度であった。
- 5例の治療関連死亡が報告されたが、2例がニボルマブ群(間質性肺疾患 1例、肺炎 1例)、3例が化学療法群(肺炎 1例、脊髄膿瘍 1例、間質性肺疾患 1例)であった。
8. PD-L1発現別の全生存期間 (事前に規定されたサブ解析)
| PD-L1<1% | 中央値 | 95%信頼区間 | HR 0.84 (95%C.I. 0.62-1.14) |
| ニボルマブ | 10.9ヶ月 | 8.4-13.9 | |
| 化学療法 | 9.3ヶ月 | 7.2-12.0 |
| PD-L1≥1% | 中央値 | 95%信頼区間 | HR 0.69 (95%C.I. 0.51-0.94) |
| ニボルマブ | 10.9ヶ月 | 8.0-14.2 | |
| 化学療法 | 8.1ヶ月 | 6.0-9.9 |
9. 後治療
・ニボルマブ群の57%(210例中119例)、化学療法群の55%(209例中115例)が後治療を受けた。
| N(%) | タキサン系 | フッ化ピリミジン系 | 白金製剤 |
|---|---|---|---|
| ニボルマブ | 100 (48) | 24 (11) | 20 (10) |
| 化学療法 | 43 (21) | 39 (19) | 22 (11) |
結語
本試験において、ニボルマブはPD-L1の発現に関わらず、化学療法群に比して有意に全生存期間を延長した。認容性も良好であり、食道扁平上皮癌の二次治療における新たな標準治療となり得る。
執筆:釧路ろうさい病院 腫瘍内科 部長 原田 一顕 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生