| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 食道扁平上皮癌 | 一次治療 | 第2相 | 奏効割合 | 国内 | あり |
試験名 :JCOG 9905-DI
レジメン:5-FU+ネダプラチン
登録期間:1999年12月〜2002年6月
背景
進行食道扁平上皮癌に対する一次化学療法として、5-FU+シスプラチンによる全身化学療法が最も一般的に使用されている。シスプラチンベースの化学療法はしばしば悪心、嘔吐、腎機能障害などの有害事象を引き起こし、用量調整や治療の延期を要することが多い。一般的に食道癌患者は他の癌腫と比較して、全身状態が不良で栄養状態が悪く、有効性を向上させ、有害事象を軽減させた新しい治療が必要とされていた。
ネダプラチンは第二世代の白金製剤であり、より良好な抗腫瘍効果を示し、腎機能障害が少なく、シスプラチンの10倍の水溶性を示す薬剤である。頭頸部や肺、子宮頸部、食道の扁平上皮癌を対象に単剤の第2相試験が行われ、有望な奏効割合を報告している。5-FU+ネダプラチン療法に関しては第1/2相試験が行われ、推奨用量は5-FU 800mg/m2 Day 1-5, ネダプラチン 90mg/m2 Day 1と決定し、奏効割合は50%と報告された。
本試験は食道扁平上皮癌に対する5-FU+ネダプラチン療法の有効性と安全性を検証するために実施された。
ネダプラチンは第二世代の白金製剤であり、より良好な抗腫瘍効果を示し、腎機能障害が少なく、シスプラチンの10倍の水溶性を示す薬剤である。頭頸部や肺、子宮頸部、食道の扁平上皮癌を対象に単剤の第2相試験が行われ、有望な奏効割合を報告している。5-FU+ネダプラチン療法に関しては第1/2相試験が行われ、推奨用量は5-FU 800mg/m2 Day 1-5, ネダプラチン 90mg/m2 Day 1と決定し、奏効割合は50%と報告された。
本試験は食道扁平上皮癌に対する5-FU+ネダプラチン療法の有効性と安全性を検証するために実施された。
シェーマ
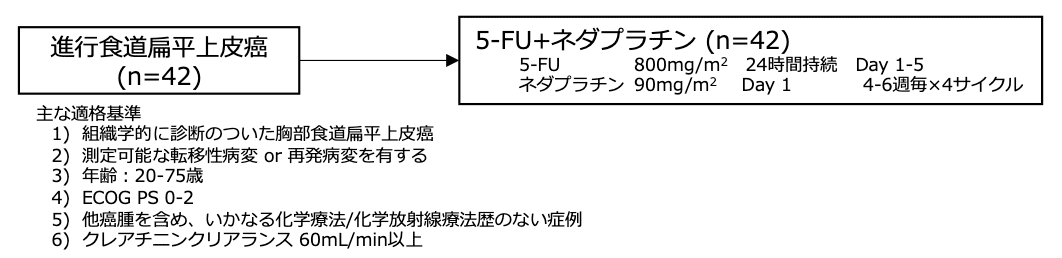
統計学的事項
主要評価項目:奏効割合
転移/再発食道癌を対象とした5-FU+シスプラチン療法の第2相試験であるJCOG9407試験では奏効割合 33.3%と報告された。以上の結果より、本試験の期待奏効割合を40%とし、閾値奏効割合を20%、α=0.1、検出力90%とした場合、36例の登録が必要であると算出された。若干の不適格例などを考慮し、本試験の目標登録症例数は40例と設定された。試験結果:
- 1999年12月から2002年6月の間に42例が症例登録された。
- 原発切除後の肺病変で登録した1例が、登録後に病変が肺結核であることが判明し、予定の治療を受けなかった。よって、安全性解析集団は41例となった。
- 更に不適格の3例(遠隔転移なし 2例/組織診断 1例)を除いた38例で有効性解析を実施した。
1. 患者背景:登録された全42例
- 年齢中央値(範囲) :59歳(44-70)
- ECOG PS:0/1/2 :21(50%)/21(50%)/0
- 前治療:外科的切除/放射線照射/術後補助化学療法/なし:23/6/3/18
- 転移臓器:リンパ節/肺/肝 :34/24/21
2. 奏効割合(WHO規準)(主要評価項目)
| N=38 | N (%) |
|---|---|
| CR PR SD PD NE |
1 (2.6) 14 (36.8) 13 (34.2) 9 (23.7) 1 (2.6) |
| 奏効割合 (95%信頼区間) |
39.5% (24.0-56.6) |
3. 全生存期間
| 中央値 | 95%信頼区間 | 1年生存割合 | |
|---|---|---|---|
| 5-FU+ネダプラチン | 8.8ヶ月 | 7.4-10.2 | 32.9% |
4. 無増悪生存期間
| 中央値 | 95%信頼区間 | 1年無増悪生存割合 | |
|---|---|---|---|
| 5-FU+ネダプラチン | 2.5ヶ月 | 1.6-3.5 | 18.4% |
5. 投与状況
- 投与期間中央値(範囲):2.0ヶ月(0.7-8.8)
- 投与サイクル中央値(範囲):2サイクル(1-11)
- 4サイクル完遂:12例、4サイクル完遂前の中止:26例(病勢進行 20例、有害事象 5例、治療中の死亡 1例)
- 後治療を受けたのは31例(78.0%)であった。
主な治療の内訳:タキサンベースの化学療法 10例、ビンデシンベースの化学療法 6例、イリノテカンベースの化学療法 4例、緩和的放射線照射 6例、緩和的手術 2例
6. 有害事象 (NCI-CTC ver.2.0)
| Grade | 1 | 2 | 3 | 4 | 全Grade (%) | Grade 3以上 (%) | |
|---|---|---|---|---|---|---|---|
| 白血球減少 | 8 | 9 | 1 | 2 | 48.8 | 7.3 | |
| 好中球数減少 | 7 | 9 | 5 | 3 | 58.5 | 19.5 | |
| 貧血 | 22 | 13 | 1 | 1 | 90.2 | 4.9 | |
| 血小板数減少 | 1 | 1 | 1 | 1 | 9.8 | 4.9 | |
| 悪心 | 13 | 7 | 6 | 0 | 63.4 | 14.6 | |
| 嘔吐 | 2 | 1 | 0 | 0 | 7.3 | 0 | |
| 下痢 | 6 | 2 | 1 | 0 | 22.0 | 2.4 | |
| 口腔粘膜炎 | 11 | 8 | 1 | 0 | 48.8 | 2.4 | |
| AST/ALT増加 | 17 | 2 | 0 | 0 | 46.3 | 0 | |
| クレアチニン増加 | 3 | 1 | 0 | 0 | 9.8 | 0 | |
| アレルギー反応 | 2 | 0 | 0 | 0 | 4.9 | 0 |
- 治療関連死亡:1例(発熱性好中球減少症後の敗血症性ショック)
結語
5-FU+ネダプラチン療法は切除不能進行/再発食道扁平上皮癌に高い有効性と良好な安全性を示した。
5-FU+ネダプラチン療法は食道扁平上皮癌に対する一次化学療法のオプションになり得ると考えられる。
5-FU+ネダプラチン療法は食道扁平上皮癌に対する一次化学療法のオプションになり得ると考えられる。
執筆:香川大学医学部附属病院 腫瘍内科 助教 大北 仁裕 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生