肝細胞癌 Asian SHARP
Efficacy and safety of sorafenib in patients in the Asia-Pacific region with advanced hepatocellular carcinoma: a phase III randomized, double-blind, placebo-controlled trial.
Cheng AL, Kang YK, Chen Z, et al. Lancet Oncol. 2009 ; 10: 25-34. [PubMed]
| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 肝細胞癌 | 一次治療 | 第3相 | 事前の設定なし | 国際 (中国、韓国、台湾) |
なし |
試験名 :Asian SHARP
レジメン:Sorafenib vs プラセボ
登録期間:2005年9月〜2007年1月
背景
欧米を中心に行われた大規模無作為化第3相プラセボ対照二重盲検試験(SHARP試験)により、ソラフェニブ単独投与は初めて全生存期間(OS)を有意に延長することが示され、また忍容性も高いという結果であった。しかしアジア人患者における肝細胞癌のほとんどは慢性B型肝炎に由来しており、欧米の状況とは異なるため、新規治療薬の効果と安全性をアジア人患者で検討することは重要である。そこで今回、アジア人患者を対象とした多施設無作為化第3相プラセボ対照二重盲検試験(Asian SHARP試験)を実施した。
シェーマ
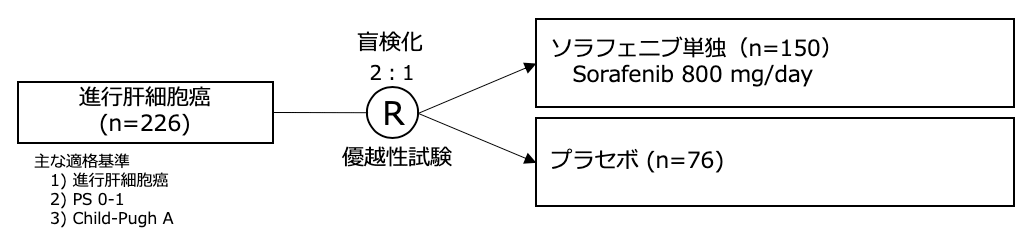
統計学的事項
主要評価項目:事前の設定なし
(評価項目は、全生存期間、増悪までの期間、症状増悪までの期間、病勢制御割合、安全性)
本試験は全生存期間、増悪までの期間、症状増悪までの期間、病勢制御割合、安全性を評価項目としたが、主要評価項目の事前設定は行わなかった。全生存期間については期待値40%、閾値20%、片側α=0.14として、165イベント・222例(ソラフェニブ群 148例、プラセボ群 74例)の登録を必要とした。試験結果:
- 2005年9月から2007年1月の間に、中国、韓国、台湾の23施設から271例が登録された。そのうち適格であった226例が2:1にソラフェニブ群とプラセボ群に割り付けられた。
- ITT集団および安全性解析対象は下記のとおり。
ITT集団:ソラフェニブ群 150例、プラセボ群 76例
安全性解析対象:ソラフェニブ群 149例、プラセボ群 75例 - 患者背景に大きな隔たりはなかった。
1. 全生存期間
| 中央値 | 95%信頼区間 | HR 0.68 (95%C.I. 0.50-0.93) P = 0.014 |
|
| ソラフェニブ(n=150) | 6.5ヶ月 | 5.56-7.56 | |
| プラセボ(n=76) | 4.2ヶ月 | 3.75-5.46 |
2. 増悪までの期間
| 中央値 | 95%信頼区間 | HR 0.57 (95%C.I. 0.42-0.79 P = 0.0005 |
|
| ソラフェニブ(n=150) | 2.8ヶ月 | 2.63-3.58 | |
| プラセボ(n=76) | 1.4ヶ月 | 1.35–1.55 |
3. 症状増悪までの期間
| 中央値 | 95%信頼区間 | HR 0.90 (95%C.I. 0.67-1.22 P = 0.50 |
|
| ソラフェニブ(n=150) | 3.5ヶ月 | 2.80-4.24 | |
| プラセボ(n=76) | 3.4ヶ月 | 2.40-4.08 |
4. 病勢制御割合
| 病勢制御割合 | P=0.0019 | |
| ソラフェニブ(n=150) | 35.3%(PR 5例、SD 81例) | |
| プラセボ(n=76) | 15.8%(PR 1例、SD 21例) |
5. 有害事象
| ソラフェニブ(n=149) | プラセボ(n=75) | |||
|---|---|---|---|---|
| 全Grade | Grade 3/4 | 全Grade | Grade 3/4 | |
| 手足皮膚反応 | 45.0% | 10.7% | 2.7% | 0% |
| 下痢 | 25.5% | 6.0% | 5.3% | 0% |
| 脱毛 | 24.8% | - | 1.3% | - |
| 疲労 | 20.1% | 3.4% | 8.0% | 1.3% |
| 皮疹/落屑 | 20.1% | 0.7% | 6.7% | 0% |
| 高血圧 | 18.8% | 2.0% | 1.3% | 0% |
| 食欲不振 | 12.8% | 0% | 2.7% | 0% |
| 悪心 | 11.4% | 0.7% | 10.7% | 1.3% |
結語
ソラフェニブは、進行肝細胞癌を対象とした第3相試験においてプラセボに対して欧米を中心に行われたSHAPR試験のみならず、アジア人においても全生存期間を有意に延長することを示し、また高い忍容性も示した。
執筆:千葉大学病院 臨床試験部 特任助教 小笠原 定久 先生
監修:神奈川県立がんセンター 消化器内科(肝胆膵) 部長 上野 誠 先生
監修:神奈川県立がんセンター 消化器内科(肝胆膵) 部長 上野 誠 先生