| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 進行肝細胞癌 | 二次治療 | 第3相 | 全生存期間 無増悪生存期間 |
国際 | あり |
試験名 :KEYNOTE-240
レジメン:ペムブロリズマブ
登録期間:2016年3月31日〜2017年11月23日
背景
第2相試験「KEYNOTE-224」において、進行肝細胞癌における免疫チェックポイント阻害薬であるペムブロリズマブ(Pembro)の抗腫瘍活性と安全性が示された。今回標準治療であるソラフェニブ不耐、不応となった進行肝細胞癌においてPembroの有用性を検討する第3相試験が実施された。
シェーマ
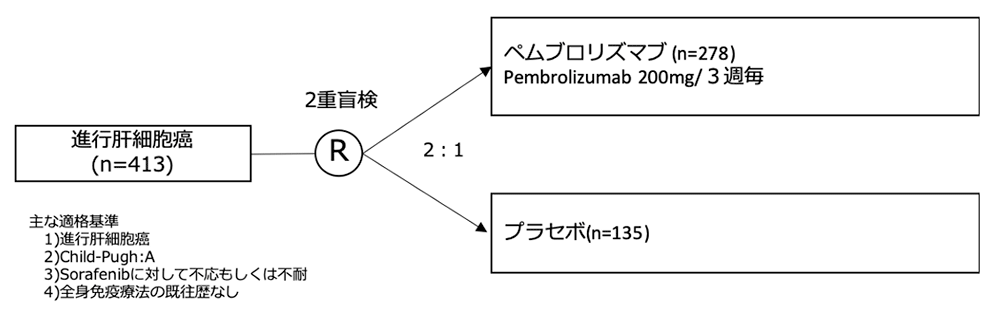
統計学的事項
主要評価項目:全生存期間および無増悪生存期間
本試験はプラセボ群を対照としてPembro群の全生存期間と無増悪生存期間のハザード比が0.65、0.60となることを検証する優越性試験として設計され、全生存期間は検出力92%、片側α=0.025として、408例の登録・273イベント、無増悪生存期間は検出力94%、片側α=0.025として、408例の登録・331イベントが必要とされた。各々事前設定されたP値は全生存期間:0.0174、無増悪生存期間:0.002であった。試験結果:
- 2016年3月31日から2017年11月23日の間に27ヶ国から413例が登録された。
- データカットオフは2019年1月に行われた。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR0.781 (95信頼区間 0.611-0.998) p=0.0238 |
|
| Pembro群 n=278 | 13.9ヶ月 | 11.6-16.0ヶ月 | |
| プラセボ群 n=135 | 10.6ヶ月 | 8.3-13.5ヶ月 |
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR0.718 (95信頼区間 0.570-0.904) p=0.0022 |
|
| Pembro群 n=278 | 3.0ヶ月 | 2.8-4.1ヶ月 | |
| プラセボ群 n=135 | 2.8ヶ月 | 1.6-3.0ヶ月 |
3. 奏効割合
| 奏効割合 | p=0.00007 | |
| Pembro群 n=278 | 18.3%(CR 6例/2.2%、PR 45例/16.2%) | |
| プラセボ群 n=135 | 4.4%(CR 0例/0%、PR 6例/4.4%) |
4. 有害事象
| PEMBRO群(N=278) | プラセボ群 (N=135) | |||
|---|---|---|---|---|
| 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | |
| AST上昇 | 63 (22.6%) | 37 (13.3%) | 22 (16.4%) | 10 (7.5%) |
| ビリルビン上昇 | 52 (18.6%) | 21 (7.5%) | 17 (12.7%) | 7 (5.2%) |
| 疲労 | 52 (18.6%) | 7 (2.5%) | 31 (23.1%) | 2 (1.5%) |
| 掻痒感 | 51 (18.3%) | 1 (0.4%) | 16 (11.9%) | 0 (0%) |
| ALT上昇 | 49 (17.6%) | 17 (6.1%) | 13 (9.7%) | 4 (3.0%) |
| 食欲低下 | 48 (17.2%) | 3 (1.1%) | 21 (15.7%) | 0 (0%) |
| 下痢 | 48 (17.2%) | 4 (1.4%) | 21 (15.7%) | 3 (2.2%) |
結語
本試験は、進行肝細胞癌において免疫チェックポイント阻害薬を用いた初の第3相試験である。免疫チェックポイント阻害薬であるPembro群では、プラセボ群と比べて全生存期間と無増悪生存期間において事前に規定された統計学的有意差を示すことはできなかった。
執筆:国立がん研究センター東病院 肝胆膵内科 がん専門修練医 大鶴 徹 先生
監修:監修:国立がん研究センター東病院 肝胆膵内科 科長 池田 公史 先生
監修:監修:国立がん研究センター東病院 肝胆膵内科 科長 池田 公史 先生