| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 肝細胞癌 | 二次治療 | 第3相 | 全生存期間 | 国際 | あり |
試験名 :REACH
レジメン:ラムシルマブ vs プラセボ
登録期間:2010年11月〜2013年4月
背景
進行肝細胞癌に対しては、唯一ソラフェニブが全生存期間の延長を示した薬剤として承認されているが、有効性及び忍容性には限界がある。
VEGF及びVEGFR-2を介したシグナル伝達は肝細胞癌における血管新生や腫瘍増殖に重要な役割を果たしており、VEGFR-2のIgG1モノクローナル抗体であるラムシルマブは、進行肝細胞癌に対する第2相試験やソラフェニブを含むチロシンキナーゼ阻害薬投与歴のある腎細胞癌において良好な抗腫瘍効果を示しており、今回の国際共同プラセボ対照二重盲検比較第3相試験(REACH試験)の実施に至った。
[ClinicalTrials.gov Identifier:NCT01140347]
VEGF及びVEGFR-2を介したシグナル伝達は肝細胞癌における血管新生や腫瘍増殖に重要な役割を果たしており、VEGFR-2のIgG1モノクローナル抗体であるラムシルマブは、進行肝細胞癌に対する第2相試験やソラフェニブを含むチロシンキナーゼ阻害薬投与歴のある腎細胞癌において良好な抗腫瘍効果を示しており、今回の国際共同プラセボ対照二重盲検比較第3相試験(REACH試験)の実施に至った。
[ClinicalTrials.gov Identifier:NCT01140347]
シェーマ
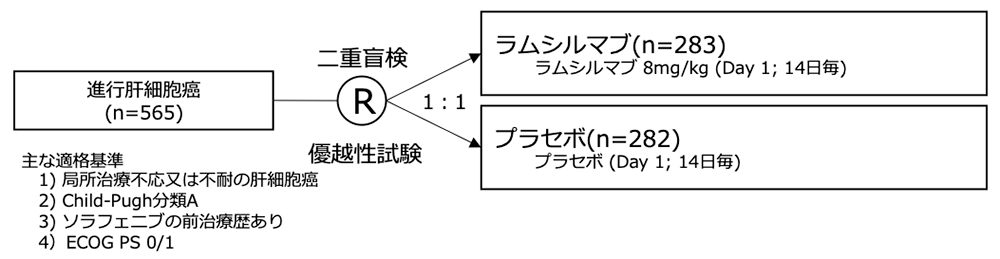
統計学的事項
主要評価項目:全生存期間
本試験はプラセボ群を対照としてラムシルマブ群の全生存期間のハザード比が0.75となることを検証する優越性試験として設計され、検出力85%、片側α=0.025として、544人の登録・438イベントが必要と設定された。試験結果:
- 2010年11月から2013年4月の間に、27ヵ国154施設から565例が登録された。
- データカットオフは、2014年3月18日に行われた。
- 患者背景に大きな隔たりは認められなかった。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.87 (95%C.I. 0.72-1.05) p=0.14 |
|
| ラムシルマブ(n=283) | 9.2ヶ月 | 8.1-10.6 | |
| プラセボ(n=282) | 7.6ヶ月 | 6.0-9.3 |
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 0.63 (95%C.I. 0.52-0.75) p<0.0001 |
|
| ラムシルマブ(n=283) | 2.8ヶ月 | 2.7-3.9 | |
| プラセボ(n=282) | 2.1ヶ月 | 1.6-2.7 |
3. 最良効果
| 完全奏効 | 部分奏効 | 安定 | 進行 | 評価不能 | |
|---|---|---|---|---|---|
| ラムシルマブ(n=283) | 1 (<1%) | 19 (7%) | 139 (49%) | 97 (34%) | 27 (10%) |
| プラセボ(n=282) | 0 | 2 (<1%) | 127 (45%) | 129 (46%) | 24 (9%) |
4. 全生存期間(部分集団解析 - AFP≥400ng/mL)
| 中央値 | 95%信頼区間 | HR 0.67 (95%C.I. 0.51-0.90) p=0.006 |
|
| ラムシルマブ(n=119) | 7.8ヶ月 | 5.8-9.3 | |
| プラセボ(n=131) | 4.2ヶ月 | 3.7-4.8 |
5. 有害事象
| ラムシルマブ (n=277) | プラセボ (n=276) | |||
|---|---|---|---|---|
| Grade 1/2 | Grade 3以上 | Grade 1/2 | Grade 3以上 | |
| 四肢浮腫 | 100 (36%) | 1 (<1%) | 49 (18%) | 1 (<1%) |
| 腹水 | 61 (22%) | 13 (5%) | 29 (11%) | 11 (4%) |
| 疲労 | 58 (21%) | 6 (2%) | 50 (18%) | 8 (3%) |
| 食欲減退 | 56 (20%) | 5 (2%) | 48 (17%) | 2(1%) |
| 嘔気 | 52 (19%) | 0 | 52 (19%) | 0 |
| 頭痛 | 51 (18%) | 2 (1%) | 15 (5%) | 0 |
| 下痢 | 48 (17%) | 3 (1%) | 37 (13%) | 1 (<1%) |
| 発熱 | 45 (16%) | 1 (<1%) | 25 (9%) | 1 (<1%) |
| 腹痛 | 42 (15%) | 5 (2%) | 50 (18%) | 12 (4%) |
| 咳嗽 | 40 (14%) | 1 (<1%) | 24 (9%) | 0 |
| 蛋白尿 | 39 (14%) | 6 (2%) | 13 (5%) | 0 |
| 鼻出血 | 38 (14%) | 0 | 17 (6%) | 0 |
| 便秘 | 36 (13%) | 0 | 34 (12%) | 0 |
| 無力症 | 37 (13%) | 14 (5%) | 31 (11%) | 5 (2%) |
| 血小板数減少 | 35 (13%) | 13 (5%) | 11 (4%) | 1 (<1%) |
| 低アルブミン血症 | 30 (11%) | 3 (1%) | 13 (5%) | 0 |
| そう痒症 | 28 (10%) | 0 | 28 (10%) | 1 (<1%) |
| 嘔吐 | 28 (10%) | 2 (1%) | 38 (14%) | 2 (1%) |
結語
ソラフェニブ治療歴のある進行肝細胞癌に対するラムシルマブの二次治療は、主要評価項目である全生存期間を延長させなかった。ただし、AFP≥400ng/mLの部分集団における有用性は更なる検討が必要である。
執筆:金沢大学 消化器内科 寺島 健志 先生
監修:神奈川県立がんセンター 消化器内科・外科(肝胆膵) 部長 上野 誠 先生
監修:神奈川県立がんセンター 消化器内科・外科(肝胆膵) 部長 上野 誠 先生