| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 非小細胞肺癌 | 二次治療 | 第3相 | 無増悪生存期間 | 国際 | あり |
試験名 :AURA3
レジメン:オシメルチニブvsカルボプラチンorシスプラチン+ペメトレキセド
登録期間:2014年8月〜2015年9月
背景
EGFRチロシンキナーゼ阻害薬 (EGFR-TKI)はEGFR 遺伝子変異陽性非小細胞肺癌 (NSCLC)に対して優れた有効性を示すものの、その後治療抵抗性 (耐性)を獲得する。そのEGFR-TKI耐性例の約60%にEGFR T790M変異が認められる。
オシメルチニブ(OSI)は、EGFR 活性型変異およびEGFR T790M変異に対して選択的かつ不可逆的に作用するEGFR-TKIである。EGFR-TKI耐性後の進行NSCLCを対象としたOSIの第I相試験 (AURA試験)では、T790M陽性患者における奏効割合が61%、無増悪生存期間 (PFS)中央値が9.6ヶ月と良好な抗腫瘍効果を認めた。T790M変異陽性NSCLCに対してOSIの有効性を検討した2つの第2相試験の統合解析でも、奏効割合66%、PFS 11.0ヶ月と良好な結果であった。そこで、EGFR-TKI耐性後にT790M変異を認める進行NSCLCを対象として、OSI群とプラチナ併用化学療法群(CBDCA or CDDP+PEM群)を比較する国際共同無作為化非盲検第3相試験であるAURA3試験が実施された。
オシメルチニブ(OSI)は、EGFR 活性型変異およびEGFR T790M変異に対して選択的かつ不可逆的に作用するEGFR-TKIである。EGFR-TKI耐性後の進行NSCLCを対象としたOSIの第I相試験 (AURA試験)では、T790M陽性患者における奏効割合が61%、無増悪生存期間 (PFS)中央値が9.6ヶ月と良好な抗腫瘍効果を認めた。T790M変異陽性NSCLCに対してOSIの有効性を検討した2つの第2相試験の統合解析でも、奏効割合66%、PFS 11.0ヶ月と良好な結果であった。そこで、EGFR-TKI耐性後にT790M変異を認める進行NSCLCを対象として、OSI群とプラチナ併用化学療法群(CBDCA or CDDP+PEM群)を比較する国際共同無作為化非盲検第3相試験であるAURA3試験が実施された。
シェーマ
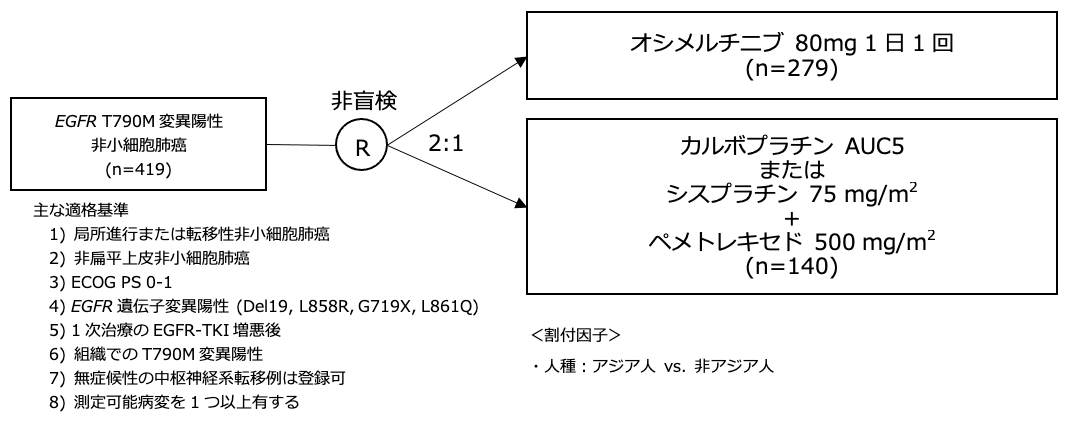
統計学的事項
主要評価項目:PFS(担当医による評価)
副次的評価項目:奏効割合、奏効期間、病勢コントロール率、全生存期間 (OS)、患者報告アウトカム、安全性
本試験は、OSI群がCBDCA or CDDP+PEM群と比較して、PFSが3ヶ月改善する (HR 0.67)と仮定 (プラチナ併用化学療法のPFS中央値が6か月と仮定)し、αエラー0.05 (両側)において、検出力80%を確保するための必要症例数は両群で400例と設定された。試験結果:
- 2014年8月から2015年9月の間に419例が登録された。両群間で患者背景に偏りはなかった。
- 2016年8月15日のデータカットオフ時点で、CBDCA or CDDP+PEM群において、60%の患者が後治療としてOSIによる治療を受けた。
- OSI群はCBDCA or CDDP+PEM群と比較して、PFSが有意に延長していた (10.1ヶ月 vs 4.4ヶ月、HR 0.30、95%CI 0.23-0.41、P < 0.001)。
- 中枢神経系転移を含む全てのサブグループにおいて、OSI群はCBDCA or CDDP+PEM群と比較して良好なPFSであった。
- 奏効割合はOSI群がCBDCA or CDDP+PEM群と比較して有意に良好であった (71% vs 31%、P < 0.001)。
- 病勢コントロール率はOSI群が93% (95%CI 90-96)で、CBDCA or CDDP+PEM群が74% (95%CI 66-81)であった。
- 奏効期間はOSI群が9.7ヶ月 (95%CI 8.3-11.6)で、CBDCA or CDDP+PEM群が4.1ヶ月 (95%CI 3.0-5.6)であった。
- 本試験のOSはデータカットオフ時点では未成熟であった。
- 患者報告アウトカムは、食欲不振、咳嗽、胸痛、呼吸困難、疲労の5つの症状において、OSI群はCBDCA or CDDP+PEM群より改善していた。
- Grade 3以上の有害事象はOSI群がCBDCA or CDDP+PEM群より少なかった (23% vs 47%)。OSI群で最もよく見られた有害事象は下痢 (41%)、皮疹 (34%)、皮膚乾燥 (23%)、爪囲炎 (22%)であった。CBDCA or CDDP+PEM群で最もよく見られた有害事象は悪心 (49%)、食欲不振 (36%)、便秘 (35%)、貧血 (30%)であった。治療関連死はOSI群で4例 (2例が呼吸不全、1例が肺炎、1例が虚血性脳卒中)、CBDCA or CDDP+PEM群で1例 (循環血液量減少性ショック)に認めた。間質性肺疾患はOSI群が4%、CBDCA or CDDP+PEM群が1%であった。QT延長はOSI群が4%、CBDCA or CDDP+PEM群が1%であった。
1. 無増悪生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.30 (0.23-0.41) P < 0.001 |
|
| OSI群 | 10.1ヶ月 | 8.3-12.3 | |
| CBDCA or CDDP+PEM群 | 4.4ヶ月 | 4.2-5.6 |
2. 無増悪生存期間のサブグループ解析
| N | HR (95%CI) | |
|---|---|---|
| EGFR変異 | ||
| Del 19 | 279 | 0.34 (0.24-0.46) |
| L858R | 128 | 0.46 (0.30-0.71) |
| 中枢神経系転移 | ||
| あり | 144 | 0.32 (0.21-0.49) |
| なし | 275 | 0.40 (0.29-0.55) |
3. 奏効割合
| 奏効割合 | 95%信頼区間 | P < 0.001 | |
| OSI群 | 71% | 65-76 | |
| CBDCA or CDDP+PEM群 | 31% | 24-40 |
4. 有害事象
| OSI群 (N=279) | CBDCA or CDDP+PEM群 (N=136) | |||
|---|---|---|---|---|
| Any Grade | Grade≧3 | Any Grade | Grade≧3 | |
| 下痢 | 41% | 1% | 11% | 1% |
| 皮疹 | 34% | 1% | 6% | 0% |
| 皮膚乾燥 | 23% | 0% | 4% | 0% |
| 爪囲炎 | 22% | 0% | 1% | 0% |
| 悪心 | 16% | 1% | 49% | 4% |
| 食欲不振 | 18% | 1% | 36% | 3% |
| 便秘 | 14% | 0% | 35% | 0% |
| 貧血 | 8% | 1% | 30% | 12% |
結語
1次治療のEGFR-TKI増悪後にT790M変異を有するNSCLC患者において、OSIはプラチナ併用化学療法(CBDCA or CDDP+PEM)より有効であった。
関連論文
・ Papadimitrakopoulou VA, Mok TS, Han JY, et al. Osimertinib versus platinum-pemetrexed for patients with EGFR T790M advanced NSCLC and progression on a prior EGFR-tyrosine kinase inhibitor: AURA3 overall survival analysis. Ann Oncol. 2020 Aug 27. Online ahead of print. [Pubmed]
・ Ahn MJ, Chiu CH, Cheng Y, et al. Osimertinib for Patients With Leptomeningeal Metastases Associated With EGFR T790M-Positive Advanced NSCLC: The AURA Leptomeningeal Metastases Analysis. J Thorac Oncol. 2020;15(4):637-648. [Pubmed]
・ Papadimitrakopoulou VA, Han JY, Ahn MJ, et al. Epidermal growth factor receptor mutation analysis in tissue and plasma from the AURA3 trial: Osimertinib versus platinum-pemetrexed for T790M mutation-positive advanced non-small cell lung cancer. Cancer. 2020;126(2):373-380. [Pubmed]
・ John T, Akamatsu H, Delmonte A, et al. EGFR mutation analysis for prospective patient selection in AURA3 phase III trial of osimertinib versus platinum-pemetrexed in patients with EGFR T790M-positive advanced non-small-cell lung cancer. Lung Cancer. 2018;126:133-138. [Pubmed]
・ Wu YL, Ahn MJ, Garassino MC, et al. CNS Efficacy of Osimertinib in Patients With T790M-Positive Advanced Non-Small-Cell Lung Cancer: Data From a Randomized Phase III Trial (AURA3). J Clin Oncol. 2018;36(26):2702-2709. [Pubmed]
・ Sebastian M, Rydén A, Walding A, et al. Patient-reported symptoms possibly related to treatment with osimertinib or chemotherapy for advanced non-small cell lung cancer. Lung Cancer. 2018;122:100-106. [Pubmed]
・ Lee CK, Novello S, Rydén A, et al. Patient-Reported Symptoms and Impact of Treatment With Osimertinib Versus Chemotherapy in Advanced Non-Small-Cell Lung Cancer: The AURA3 Trial. J Clin Oncol. 2018;36(18):1853-1860. [Pubmed]
・ Akamatsu H, Katakami N, Okamoto I, et al. Osimertinib in Japanese patients with EGFR T790M mutation-positive advanced non-small-cell lung cancer: AURA3 trial. Cancer Sci. 2018;109(6):1930-1938. [Pubmed]
執筆:近畿大学医学部 内科学教室 腫瘍内科部門 助教 加藤 了資 先生
監修:市立岸和田市民病院 腫瘍内科 医長 谷崎 潤子 先生
監修:市立岸和田市民病院 腫瘍内科 医長 谷崎 潤子 先生