| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 非小細胞肺癌 | 二次治療、三次治療 | 第3相 | 全生存期間 | 東アジア | あり |
試験名 :非小細胞肺癌におけるS-1のDTXに対するランダム化非劣性試験(EAST-LC試験)
レジメン:S-1 vs DTX
登録期間:2010年7月~2014年6月
背景
進行非小細胞肺癌において、プラチナ併用化学療法 (±免疫チェックポイント阻害剤) による一次治療増悪後の現在の標準治療はドセタキセル (DTX) (±ラムシルマブ) やペメトレキセドである。しかし、DTXはGrade 3/4の好中球減少や発熱性好中球減少の頻度が高い。
エスワン(S-1)は経口細胞傷害性抗癌剤であり、テガフール(5-FUのプロドラッグ)、ギメラシル(5-FU濃度を高める)、オテラシルカリウム(5-FUの消化管毒性を軽減する)を1:0.4:1の割合で含む合剤である。先行する第2相試験でS-1の有望な成績が示されたことから、本試験は、既治療の進行非小細胞肺癌におけるS-1のDTXに対する生存期間の非劣性を検証するために実施された。
エスワン(S-1)は経口細胞傷害性抗癌剤であり、テガフール(5-FUのプロドラッグ)、ギメラシル(5-FU濃度を高める)、オテラシルカリウム(5-FUの消化管毒性を軽減する)を1:0.4:1の割合で含む合剤である。先行する第2相試験でS-1の有望な成績が示されたことから、本試験は、既治療の進行非小細胞肺癌におけるS-1のDTXに対する生存期間の非劣性を検証するために実施された。
シェーマ
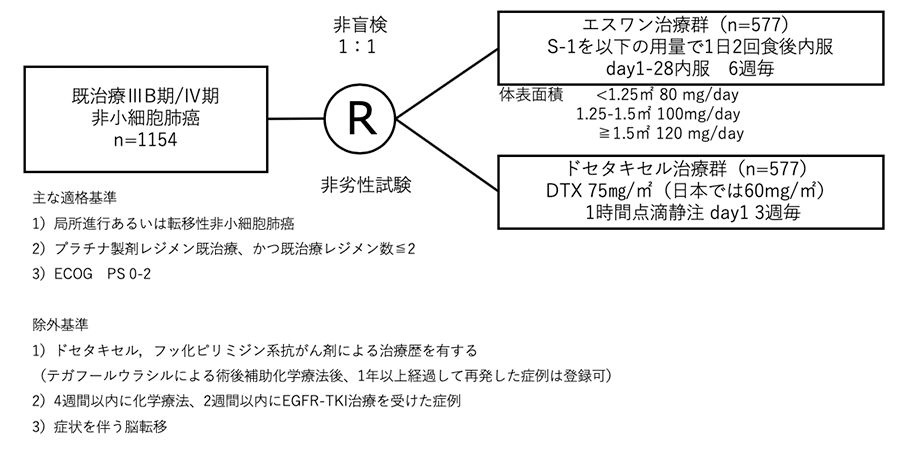
※層別化因子:治療群、PS、前治療レジメン数、EGFR-TKI治療の有無、EGFR遺伝子変異の状況、性別、組織型、喫煙歴
統計学的事項
本試験の主要評価項目は全生存期間(OS)、副次評価項目は有害事象、奏効割合(RR)、無増悪生存期間(PFS)、などであった。
OSにおけるS-1のDTXに対する非劣性を示すため、ランダム化1.5年後における両群の生存期間中央値を12ヶ月と仮定し、ハザード比 (HR) の非劣性マージンを1.2とすると、片側α0.025、検出力80%で非劣性を示すためには両群で944イベント、各群568名が必要とされた。既治療非小細胞肺癌を対象とした第3相試験において、DTXのBSCに対するHRは0.61と報告されており、本試験ではS-1が、BSCに対してDTXが有するベネフィット(効果)の60%程度を保持すれば許容されると考え、非劣性マージンをHR 1.2と算出した。
OSにおけるS-1のDTXに対する非劣性を示すため、ランダム化1.5年後における両群の生存期間中央値を12ヶ月と仮定し、ハザード比 (HR) の非劣性マージンを1.2とすると、片側α0.025、検出力80%で非劣性を示すためには両群で944イベント、各群568名が必要とされた。既治療非小細胞肺癌を対象とした第3相試験において、DTXのBSCに対するHRは0.61と報告されており、本試験ではS-1が、BSCに対してDTXが有するベネフィット(効果)の60%程度を保持すれば許容されると考え、非劣性マージンをHR 1.2と算出した。
試験結果:
- 1154名が登録されランダム化によって各群577名が割り当てられた。
最大解析集団(FAS)はS-1群577名、DTX群570名(6名同意撤回、1名書類不備)となり、両群の患者背景は均衡がとれていた。 - 主要評価項目であるOS中央値は、S-1群で12.75ヵ月、DTX群で12.52ヵ月であった。HR 0.945(95%CI 0.833-1.073; P=0.3818)と95%信頼区間の上限が非劣性マージン1.2を下回ったことから、S-1のDTXに対する非劣性が示された。OSのサブグループ解析では特徴的なサブグループは同定できなかった。
- PFS、RRには両群間に有意差を認めなかった。
- PFSのサブグループ解析では、EGFR遺伝子変異陽性, 女性, 腺癌ではDTXのほうが有効である可能性が示唆された。
- 有害事象に関して、S-1群では食欲低下、悪心、下痢が多く、DTX群では好中球減少、脱毛症、食欲低下が多かった。発熱性好中球減少症は0.9% vs 13.6%とDTX群で多かった。
- EORTC QLQ-C30(がん患者のQOLスコア)において、S-1群は4つの機能スケール(身体機能、役割機能、情緒機能、社会的機能)と、症状スケール(疲労感)で優れていた。
また、EORT CQLQ-LC13(肺癌患者における症状スコア)において、S-1群は胸部痛、呼吸困難、末梢神経障害、脱毛症で、DTX群は嚥下障害のスコアで優れた結果だった。
1. 全生存期間(主要評価項目)
| 中央値 | HR 0.945 (95%CI, 0.833-1.073,P=0.3818) |
|
| S-1 (n=577) | 12.75ヵ月 | |
| DTX(n=570) | 12.52ヵ月 |
| N | ||||
|---|---|---|---|---|
| S-1 | DTX | HR | P値 | |
| Japan | 361 | 359 | 0.905 | 0.2141 |
| non-Japan | 216 | 211 | 1.058 | 0.6071 |
2. 無増悪生存期間
| 中央値 | HR 1.033 (95%CI, 0.913-1.168,P=0.6080) |
|
| S-1 (n=577) | 2.86ヵ月 | |
| DTX(n=570) | 2.89ヵ月 |
3. 奏効割合
| 奏効割合 | 病勢制御割合 | 奏効割合 P=0.3761 |
|
| S-1 (n=570) | 8.3% | 45.4% | |
| DTX(n=577) | 9.9% | 44.7% |
4. 有害事象(Grade3/4血液毒性 NCI-CTCAE ver4.0)
| S-1(n=569) | DTX(n=560) | |||
|---|---|---|---|---|
| 全グレード | グレード3/4 | 全グレード | グレード3/4 | |
| 食欲低下 | 50.4% | 6.5% | 36.4% | 2.7% |
| 悪心 | 36.4% | 0.9% | 26.6% | 1.4% |
| 下痢 | 35.9% | 6.3% | 16.4% | 1.1% |
| 皮膚色素過剰 | 31.3% | 0.0% | 2.0% | 0.0% |
| 口内炎 | 23.4% | 2.5% | 14.3% | 0.9% |
| 嘔吐 | 18.6% | 1.6% | 11.4% | 0.7% |
| 倦怠感 | 18.5% | 0.2% | 23.4% | 0.7% |
| 疲労 | 16.7% | 1.2% | 18.9% | 0.9% |
| 好中球減少 | 14.9% | 5.4% | 54.8% | 47.7% |
| 便秘 | 12.3% | 0.2% | 16.4% | 0.2% |
| 貧血 | 12.1% | 2.6% | 9.5% | 1.4% |
| 体重減少 | 12.1% | 0.5% | 3.6% | 0.0% |
| 血小板減少 | 11.1% | 1.2% | 2.3% | 0.2% |
| 斑状丘疹状皮疹 | 10.4% | 0.9% | 8.0% | 0.2% |
| 白血球減少 | 9.5% | 1.2% | 43.9% | 29.1% |
| 末梢性感覚ニューロパチー | 4.0% | 0.2% | 15.5% | 0.7% |
| 末梢性浮腫 | 2.3% | 0.0% | 15.7% | 0.9% |
| 脱毛症 | 1.9% | 0.0% | 46.6% | 0.0% |
| 発熱性好中球減少症 | 0.9% | 0.9% | 13.4% | 13.4% |
結語
本試験は既治療非小細胞肺癌において、S-1がDTXに対して全生存期間において非劣性であることを証明した第3相試験である。無増悪生存期間、奏効割合はほぼ同様で、有害事象の毒性プロファイルが異なっていた。
S-1はDTXと比較して脱毛がなく、好中球減少も軽度かつ内服治療という特徴を持っており、DTX単剤治療に代わる治療の選択肢の一つになり得る。
S-1はDTXと比較して脱毛がなく、好中球減少も軽度かつ内服治療という特徴を持っており、DTX単剤治療に代わる治療の選択肢の一つになり得る。
執筆:横浜市立大学附属病院 呼吸器内科学 堂下 皓世 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 朝尾 哲彦 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 朝尾 哲彦 先生