| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 肺癌 | 一次治療 | 第3相 | 全生存期間 | 日本 | あり |
試験名 :JCOG0803/WJOG4307L
レジメン:Weekly DOC+CDDP vs DOC
登録期間:2008年8月〜2010年9月
背景
進行非小細胞肺癌のプラチナ併用化学療法に関する第3相試験のサブグループ解析にて、若年者と同様に高齢者にもプラチナ併用療法の有効性が認められたと報告されている(Belani CP, et al. Cancer. 2005;104(12):2766-74. Langer CJ, et al. J Natl Cancer Inst. 2002;94(3):173-81.)。しかし、一般に加齢に伴い薬物排泄や代謝能は低下しており、高齢者の化学療法は、抗癌剤の投与量や投与スケジュールを調整することが推奨されている。
日本では、70歳以上の進行非小細胞肺癌患者を対象に、ドセタキセル(DOC)+シスプラチン(CDDP)の週1回投与(DOC 20 mg/m2, Day 1, 8, 15, 4週毎+CDDP 25 mg/m2, Day 1, 8, 15, 4週毎)とDOCの週1回投与(DOC 25 mg/m2, Day 1, 8, 15, 4週毎)を比較する第3相試験であるJCOG0207が実施された(Tsukada H, et al. Jpn J Clin Oncol. 2015;45(1):88-95.)。2回目の中間解析にて、全生存期間はDOC+CDDP群で良好であったが、74歳以下の患者において、75歳以上においては有意な差が認められていなかったものの、DOC+CDDP群とDOC群で著しい差が認められたため、試験は早期終了となった。最終解析の全生存期間は、74歳以下においてはHR 0.508(95%CI 0.259-0.997)、75歳以上においてはHR 0.822(95%CI 0.483-1.400)であった。このため、当時の高齢非小細胞肺癌の標準療法であったDOCの3週毎投与法( DOC 60 mg/m2, Day 1, 3週毎)を対象群として、DOC+CDDPの週1回投与法を比較する第3相試験が行われた。
日本では、70歳以上の進行非小細胞肺癌患者を対象に、ドセタキセル(DOC)+シスプラチン(CDDP)の週1回投与(DOC 20 mg/m2, Day 1, 8, 15, 4週毎+CDDP 25 mg/m2, Day 1, 8, 15, 4週毎)とDOCの週1回投与(DOC 25 mg/m2, Day 1, 8, 15, 4週毎)を比較する第3相試験であるJCOG0207が実施された(Tsukada H, et al. Jpn J Clin Oncol. 2015;45(1):88-95.)。2回目の中間解析にて、全生存期間はDOC+CDDP群で良好であったが、74歳以下の患者において、75歳以上においては有意な差が認められていなかったものの、DOC+CDDP群とDOC群で著しい差が認められたため、試験は早期終了となった。最終解析の全生存期間は、74歳以下においてはHR 0.508(95%CI 0.259-0.997)、75歳以上においてはHR 0.822(95%CI 0.483-1.400)であった。このため、当時の高齢非小細胞肺癌の標準療法であったDOCの3週毎投与法( DOC 60 mg/m2, Day 1, 3週毎)を対象群として、DOC+CDDPの週1回投与法を比較する第3相試験が行われた。
シェーマ
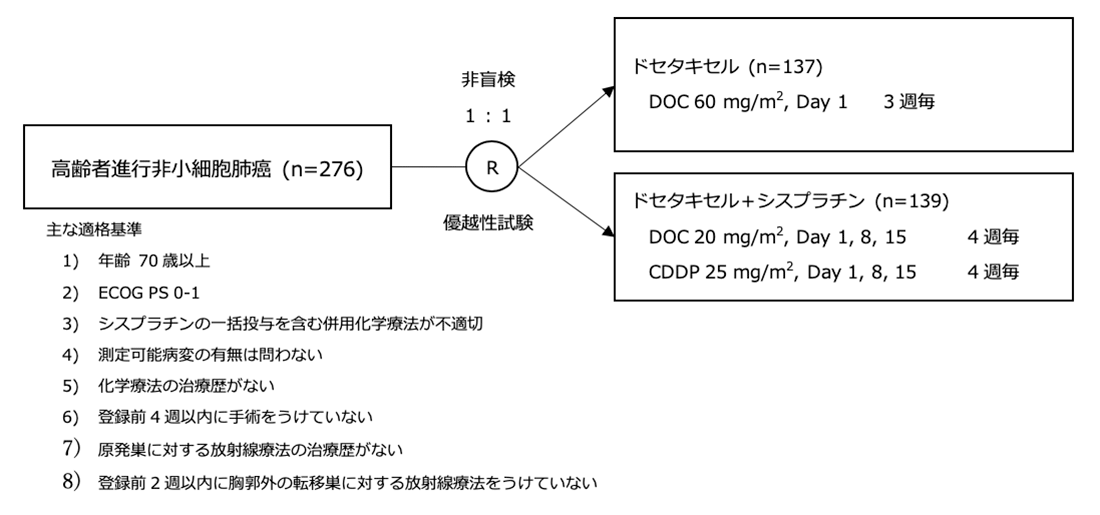
統計学的事項
主要評価項目:全生存期間
本試験の主要評価項目は全生存期間であった。全生存期間中央値が10ヵ月から13.3ヵ月へと33%改善すると仮定し、検出力 80%、片側α=0.05にて、364人の患者が必要と算出された。不適格例および脱落例の割合を5%と仮定し、本試験のサンプルサイズは380例と設定された。2回の中間解析が計画され、1回目は患者の50%が登録された後、2回目は登録が完了した後に実施することとされた。試験結果:
- 1回目の中間解析が2010年9月に実施され、221人の患者が対象であった。全生存期間はDOC+CDDP群がドセタキセル群よりも劣っており(HR 1.56、95%CI 0.98-2.49、片側p=0.97、p=0.06(両側検定))、最終解析でDOC+CDDP群がDOC群よりも統計学的に優越性を検証する確率は0.996%と予測された。この結果から、試験は早期無効中止とされた。
- 2008年10月~2010年9月の期間に56施設より276例が登録され、DOC群には137例、DOC+CDDP群には139例が割り付けられた。
- 276例で安全性解析が行われた。
- コントロール不良の糖尿病のために、DOC群の3例、DOC+CDDP群の1例が除外され、DOC群の134例、DOC+CDDP群の138例、合計272例で生存期間解析が行われた。
- 年齢中央値は両群ともに76歳であった。
- データカットオフは2010年11月であった。追跡期間中央値は9.6ヵ月であった。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 1.18 (95% CI 0.83-1.69) |
|
| DOC | 14.8ヵ月 | 11.9-24.1 | |
| DOC+CDDP | 13.3ヵ月 | 10.8-19.4 |
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 0.92 (95% CI 0.71-1.20) |
|
| DOC | 4.4ヵ月 | 3.4-5.1 | |
| DOC+CDDP | 4.7ヵ月 | 4.1-5.8 |
3. 奏効割合
| 奏効割合 | 95%信頼区間 | p=0.10 | |
| DOC | 24.6% | 17.4%-33.1% | |
| DOC+CDDP | 34.4% | 26.3%-43.2% |
4. 有害事象
| DOC | DOC+CDDP | |||
|---|---|---|---|---|
| Grade 3 or 4(%) | Grade 4 (%) | Grade 3 or 4(%) | Grade 4 (%) | |
| 血液毒性 | ||||
| 白血球減少 | 62.7 | 8.2 | 5.4 | 0 |
| 好中球数減少 | 88.8 | 67.9 | 10.1 | 0.8 |
| 貧血 | 3.7 | 0.7 | 16.3 | 0.8 |
| 血小板数減少 | 0 | 0 | 0.8 | 0 |
| 非血液毒性 | ||||
| 発熱性好中球減少 | 15.2 | 0 | 0 | 0 |
| 低ナトリウム血症 | 5.2 | 0.7 | 14.7 | 0.8 |
| 低アルブミン血症 | 1.5 | - | 4.7 | - |
| 感染 | 7.6 | 0 | 8.4 | 0.8 |
| 食欲不振 | 1.5 | 0 | 10.7 | 0 |
| 悪心 | 0.8 | 0 | 3.8 | 0 |
| 下痢 | 3.8 | 0 | 0.8 | 0 |
| 疲労 | 3.0 | 0 | 5.3 | 0 |
| 肺臓炎 | 5.3 | 0 | 2.3 | 0.8 |
5. サブ解析
年齢、病期、性別、ECOG PS、喫煙歴、組織型、EGFR変異、いずれのサブグループも統計学的に有意差を認めなかった。
結語
70歳以上のCDDP一括投与に不適な高齢進行非小細胞肺癌に対する一次療法として、weekly DOC+CDDP療法は3週毎投与のDOC療法と比較して、優越性を示すことはできなかった。この結果、引き続き、3週毎投与のDOC療法が標準療法とみなされた。
執筆:厚木市立病院 呼吸器内科 医長 田村 休応 先生
監修:国立がん研究センター中央病院 呼吸器内科 医員 大熊 裕介 先生
監修:国立がん研究センター中央病院 呼吸器内科 医員 大熊 裕介 先生