| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 肺癌 | 一次治療 | 第3相 | 全生存期間 | 日本 | あり |
試験名 :JCOG1210
レジメン:DOC vs CBDCA+PEM(導入療法+PEM維持療法)
登録期間:2013年8月12日〜2017年2月20日
背景
75歳以上の高齢者進行非小細胞肺癌に対するシスプラチン(CDDP)併用療法に関しては、CDDPの投与量や投与スケジュールの変更が検討されてきたが、臨床的な有益性は証明されてこなかった。IFCT-0501試験(Quoix E, et al. Lancet. 2011;378(9796):1079-88.)では、70-89歳(PS 0-2)の高齢の進行非小細胞肺癌患者を対象に、4週間毎に4コースまでのカルボプラチン(CBDCA)(AUC 6, day 1)+weekly-パクリタキセル(PTX)(90mg/m2, day 1, 8, 15)併用療法(4コースまで)とゲムシタビン(GEM)またはビノレルビン(VNR)単剤療法(5コースまで)を比較し、全生存期間、無増悪生存期間、奏効割合においてCBDCA+ weekly-PAC併用療法の優越性が検証されたが、有害事象の発現割合も高く、治療関連死は4.4%であり、本邦では受け入れられなかった。高齢者進行非小細胞肺癌患者を対象としたドセタキセル(DOC)とVNRを比較したWJTOG9904試験(Kudoh S, et al. J Clin Oncol. 2006;24(22):3657-63.)では、統計学的有意差は認めなかったものの、無増悪生存期間および奏効割合ではDOCの方が良好であったことから、我が国ではDOC 単剤療法がみなし標準治療とされ実地臨床では用いられてきた。その後、75 歳以上の進行非扁平上皮非小細胞肺癌患者を対象に、CBDCA+ペメトレキセド(PEM)(導入療法+PEM維持療法を含む)の有効性と忍容性が単群第2相試験(Tamiya M, et al. Med Oncol. 2016 Jan;33(1):2.)で示された(全生存期間中央値 20.5ヵ月、無増悪生存期間中央値 5.7ヵ月)。この結果に基づき、DOC を対象群とし、CBDCA+PEMの非劣性および有効性を検証する第3相試験が行われた。
シェーマ
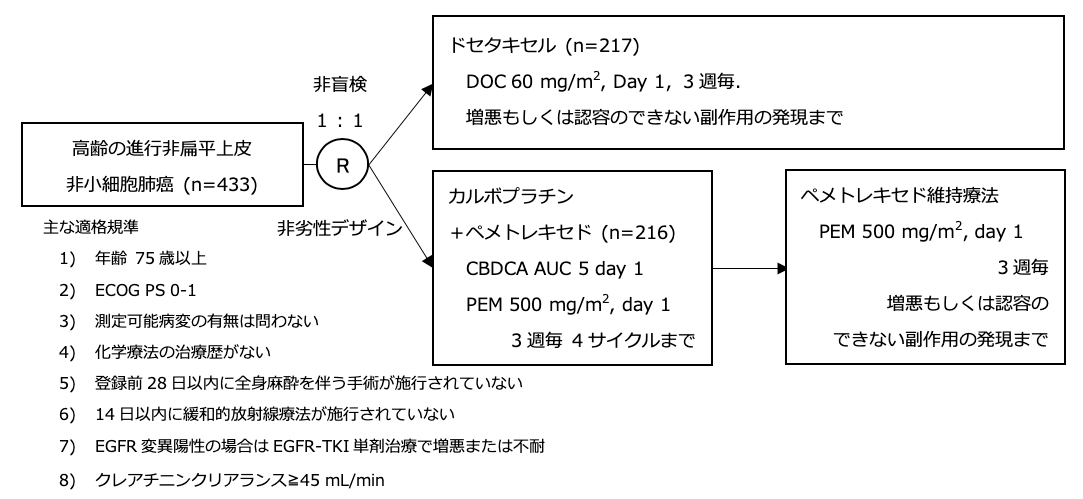
統計学的事項
主要評価項目:全生存期間
本試験の主要評価項目は全生存期間であった。全生存期間中央値をDOC群で15ヵ月、CBDCA+PEM群で18ヵ月と仮定し、DOCと比較しCBDCA+PEMの全生存期間が2ヵ月以上短縮(HR 1.154 [非劣性マージン])していない場合、非劣性が証明されることとすると、検出力 80%、片側α=0.05として、320例の登録(233例のイベント)を必要と算出された。予想よりも症例集積が早かったため、検出力をあげるために2015年8月14日、検出力 85%、片側α=0.025に変更し、目標症例数を430例に再設定された。また、主たる解析で全生存期間における非劣性が証明された場合に限り、優越性の検定を行うこととし、HRの信頼区間の上限が1未満であれば優越性が証明されたと判断することとした。
試験結果:
- 2013年8月12日~2017年2月20日の期間に79施設より433例が登録され、DOC群には217例、CBDCA+PEM群には216例が割り付けられた。
- 95例がEGFR遺伝子変異を有していた。
- 433例が有効性解析に含められたが、DOC群の3例、CBDCA+PEM群の2例がプロトコル治療を受けなかったため、428例で安全性解析が行われた。
- 年齢中央値は両群ともに78歳であった。
- 治療サイクル中央値はDOC群 4サイクル、CBDCA+PEM群 6サイクルであった。
- 減量はDOC群 61.3%、CBDCA+PEM群 22.7%で行われた。
- 追跡期間中央値は17.1ヵ月であった。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | R 0.850 (95%CI 0.684-1.056) p=0.003 (非劣性) p=0.07(優越性) |
|
| DOC | 15.5ヵ月 | 13.6-18.4 | |
| CBDCA+PEM | 18.7ヵ月 | 16.0-21.9 |
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 0.739 (95%CI 0.609-0.896) P<0.001 |
|
| DOC | 4.3ヵ月 | 4.0-4.9 | |
| CBDCA+PEM | 6.4ヵ月 | 5.4-7.7 |
3. 奏効割合
| 奏効割合 | 95%信頼区間 | P=0.07 | |
| DOC | 28.2% | 22.2%-34.9% | |
| CBDCA+PEM | 36.8% | 30.1%-43.8% |
4. 有害事象
| DOC(N=214) | CBDCA+PEM(N=214) | |||||
|---|---|---|---|---|---|---|
| Grade 1 or 2 | Grade 3 | Grade 4 | Grade 1 or 2 | Grade 3 | Grade 4 | |
| 白血球減少 | 24.8% | 60.3% | 8.4% | 44.9% | 25.2% | 2.8% |
| 好中球数減少 | 8.9% | 15.4% | 70.6% | 41.1% | 29.4% | 16.8% |
| 貧血 | 89.7% | 1.4% | 0.5% | 69.2% | 24.8% | 4.7% |
| 血小板数減少 | 35.5% | 0.5% | 0.9% | 65.0 | 16.3% | 9.3% |
| 発熱性好中球減少 | - | 16.8% | 0.9% | - | 4.2% | 0% |
| 疲労 | 56.5% | 4.7% | - | 52.3% | 6.1% | - |
| 食欲不振 | 54.8% | 5.1% | 0% | 56.5% | 7.5% | 0% |
| 低ナトリウム血症 | 61.7% | 7.0 | 0% | 61.2% | 8.4% | 0% |
| 感染 | 7.9% | 7.5% | 0% | 9.3% | 6.5% | 0% |
結語
75歳以上の化学療法未治療の進行非扁平上皮非小細胞肺癌に対するCBDCA+PEM療法(導入療法+PEM維持療法)は、有効性と忍容性において臨床的に有用であり、高齢の未治療非扁平上皮非小細胞肺癌の標準療法のひとつとして検討されるべきである。
執筆:厚木市立病院 呼吸器内科 医長 田村 休応 先生
監修:国立がん研究センター中央病院 呼吸器内科 医員 大熊 裕介 先生
監修:国立がん研究センター中央病院 呼吸器内科 医員 大熊 裕介 先生