| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 非小細胞肺癌 | 二次治療 | 第3相 | 全生存期間 | 国際 | なし |
試験名 :既治療非小細胞肺癌におけるペメトレキセドvsドセタキセルの第3相ランダム化比較試験(JMEI試験)
レジメン:PEM vs DTX
登録期間:2001年3月~2002年2月
背景
ドセタキセル (DTX) はプラチナ併用化学療法増悪後の2次治療以降で、イフォスファミドやビノレルビン、ベストサポーティブケア (BSC) などと比較して生存を延長し、QOLを改善することが示された薬剤であり、非小細胞肺癌(NSCLC)の二次治療の標準治療として確立された薬剤である。しかしその有効性は未だ十分ではなく、新規治療が求められていた。
ペメトレキセド (PEM) は主に非小細胞肺癌や悪性胸膜中皮腫に対する治療薬として開発された葉酸代謝拮抗薬である。葉酸とビタミンB12の補充により有害事象が減少することが明らかになってから毒性管理が容易となった。先行する第2相試験で有望な成績を示し、DTXと比較して毒性も低いことが期待されたことから、既治療非小細胞肺癌においてDTXとPEMの有効性を比較する第3相非劣性試験が行われた。
ペメトレキセド (PEM) は主に非小細胞肺癌や悪性胸膜中皮腫に対する治療薬として開発された葉酸代謝拮抗薬である。葉酸とビタミンB12の補充により有害事象が減少することが明らかになってから毒性管理が容易となった。先行する第2相試験で有望な成績を示し、DTXと比較して毒性も低いことが期待されたことから、既治療非小細胞肺癌においてDTXとPEMの有効性を比較する第3相非劣性試験が行われた。
シェーマ
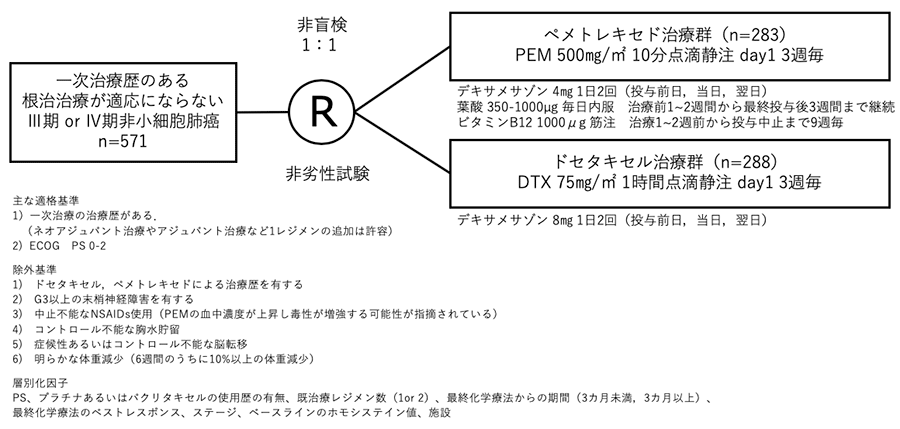
統計学的事項
本試験の主要評価項目は生存期間、副次的評価項目は有害事象、奏効割合 (RR)、無増悪生存期間(PFS)、などとした。本試験は、DTXに対するPEMの真のハザード比を0.83と(PEMの方がやや優れていると仮定)し、αエラー 5%, 検出力81%で生存期間の非劣性を示すようデザインされ、あらかじめ2つの非劣性マージンが設定された。
当初、PEMの生存期間がDTXと比較して劣っていてもその割合が10%以内であれば許容し、ハザード比の95%信頼区間 [CI] 上限が1.11未満であれば非劣性とするようデザインされた(非劣性マージン①)。
また、もう一つの非劣性マージンとして、DTXとBSCを比較した第3相試験におけるハザード比が0.56と報告されていることを根拠に、PEMが、BSCに対してDTXが有するベネフィット(効果)の50%程度を保持すると仮定し、算出されるハザード比の95% CI上限1.21未満であれば非劣性とするよう設定された (Percent retention method; 非劣性マージン②)。
当初、PEMの生存期間がDTXと比較して劣っていてもその割合が10%以内であれば許容し、ハザード比の95%信頼区間 [CI] 上限が1.11未満であれば非劣性とするようデザインされた(非劣性マージン①)。
また、もう一つの非劣性マージンとして、DTXとBSCを比較した第3相試験におけるハザード比が0.56と報告されていることを根拠に、PEMが、BSCに対してDTXが有するベネフィット(効果)の50%程度を保持すると仮定し、算出されるハザード比の95% CI上限1.21未満であれば非劣性とするよう設定された (Percent retention method; 非劣性マージン②)。
試験結果:
- 2001年3月から2002年2月の期間に571例が登録され、PEM群には283例、DTX群には288例が割り付けられた。フォローアップ期間中央値は7.5ヶ月であった。
- 主要評価項目である生存期間は、生存期間中央値PEM群 8.3ヶ月、DTX群 7.9ヶ月 (HR 0.99, 95%信頼区間 0.82-1.2; 非劣性P = 0.226) で非劣性は示されなかった(非劣性マージン①)。一方、Percent retention methodを用いると、PEMが、BSCに対してDTXが有する有効性の102%(95%信頼区間下限 52%)を保持していた (P=0.047) (非劣性マージン②)。
- 奏効割合、無増悪生存期間も有意差はなかった。
- PEM群はDTX群と比較して、好中球減少、発熱性好中球減少、有害事象による入院、G-CSF製剤使用が有意に少なかった。また、DTX群では脱毛症、下痢が、PEM群ではALT上昇が多かった。
1. 全生存期間(主要評価項目)
| 中央値 | HR 0.99 (95%CI, 0.82-1.2,P=0.226) |
|
| PEM(n=283) | 8.3ヵ月 | |
| DTX(n=288) | 7.9ヵ月 |
2. 無増悪生存期間
| 中央値 | HR 0.97 (95%CI, 0.82-1.16,P=0.759) |
|
| PEM(n=283) | 2.9ヵ月 | |
| DTX(n=288) | 2.9ヵ月 |
3. 奏効割合
| 奏効割合 | SD | 病勢制御割合 | P=0.105 | |
| PEM(n=283) | 9.1% | 45.8% | 54.9% | |
| DTX(n=288) | 8.8% | 46.4% | 55.2% |
4. 有害事象(Grade3/4血液毒性 NCI-CTACE ver2.0)
| PEM(n=283) | DTX(n=288) | P値 | |
|---|---|---|---|
| 好中球減少 | 5.3% | 40.2% | <0.001 |
| 発熱性好中球減少症 | 1.9% | 12.7% | <0.001 |
| 感染を伴う好中球減少 | 0.0% | 3.3% | 0.004 |
| 貧血 | 4.2% | 4.3% | 0.99 |
| 血小板減少症 | 1.9% | 0.4% | 0.116 |
5. 有害事象(非血液毒性 NCI-CTACE ver2.0)
| PEM(n=283) | DOC(n=288) | ||||
|---|---|---|---|---|---|
| 全グレード | グレード3/4 | 全グレード | グレード3/4 | P値 | |
| 疲労 | 34.0% | 5.3% | 35.9% | 5.4% | 0.99 |
| 悪心 | 30.9% | 2.6% | 16.7% | 1.8% | 0.57 |
| 嘔吐 | 16.2% | 1.5% | 12.0% | 1.1% | 0.72 |
| 肺 | 0.8% | 0.0% | 2.1% | 1.4% | NA |
| 感覚障害 | 4.9% | 0.0% | 15.9% | 1.1% | NA |
| 口内炎 | 14.7% | 1.1% | 17.4% | 1.1% | 0.99 |
| 脱毛症 | 6.4% | - | 37.7% | - | <0.001 |
| 下痢 | 12.8% | 0.4% | 24.3% | 2.5% | 0.069 |
| 皮疹 | 14.0% | 0.8% | 6.2% | 0.7% | 1.00 |
| 体重減少 | 1.1% | 0.0% | 1.8% | 0.0% | NA |
| 浮腫 | 4.5% | 0.0% | 8.3% | 0.0% | NA |
| ALT上昇 | 7.9% | 1.9% | 1.4% | 0.0% | 0.028 |
6. 生存期間を改善する要素(サブグループ解析)
| PEM生存期間 | DTX生存期間 | P値 | |
|---|---|---|---|
| PS | |||
| 0/1 | 9.4ヵ月 | 9.1ヵ月 | 0.996 |
| 2 | 3.6ヵ月 | 2.2ヵ月 | 0.264 |
| 臨床病期 | |||
| Ⅲ | 9.3ヵ月 | 10.3ヵ月 | 0.948 |
| Ⅳ | 7.9ヵ月 | 7.2ヵ月 | 0.896 |
| 前治療からの時間 | |||
| 3ヵ月未満 | 7.0ヵ月 | 6.2ヵ月 | 0.670 |
| 3ヵ月以上 | 9.3ヵ月 | 9.2ヵ月 | 0.588 |
結語
本試験は、既治療非小細胞肺癌に対する二次治療としてのPEMのDTXに対する非劣性試験であったが、非劣性は示されなかった (非劣性マージン①)。
一方、生存曲線はほぼ重なっていること、Percent retention methodにより、PEMが、DTXのBSCに対する効果の少なくとも50%を保持していることが示された (非劣性マージン②) ことから、ある程度の有効性は担保されているものと考えられた。
コントロールが容易なPEMの毒性の低さは魅力的であり、既治療の非小細胞肺癌の二次治療以降の選択肢の一つとして一考の余地があるものと考える。
一方、生存曲線はほぼ重なっていること、Percent retention methodにより、PEMが、DTXのBSCに対する効果の少なくとも50%を保持していることが示された (非劣性マージン②) ことから、ある程度の有効性は担保されているものと考えられた。
コントロールが容易なPEMの毒性の低さは魅力的であり、既治療の非小細胞肺癌の二次治療以降の選択肢の一つとして一考の余地があるものと考える。
執筆:横浜市立大学附属病院 呼吸器内科学 堂下 皓世 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 朝尾 哲彦 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 朝尾 哲彦 先生