| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 非小細胞肺癌 | 既治療 | 第2/3相 | 無増悪生存期間/全生存期間 | 国際 | あり |
試験名 :KEYNOTE-010
レジメン:ペムブロリズマブ vs ドセタキセル
登録期間:2013年8月23日〜 2015年2月27日
背景
非小細胞肺癌の治療では分子標的薬が進歩してきているが、標的になる遺伝子変異を有する症例は限られている。ドライバー変異陰性非小細胞肺癌におけるプラチナ併用化学療法増悪後の2次治療の標準治療は長らくドセタキセル(DOC)単剤であった。ペムブロリズマブ(Pemb)はヒト化IgG4抗PD-1抗体で、PD-1を阻害することで抗腫瘍免疫効果を発揮する免疫チェックポイント阻害薬である。非小細胞肺癌を対象とした第1b相試験であるKEYNOTE-001を受け、プラチナ併用化学療法増悪後の非小細胞肺癌の2次治療においてPemb単剤とDOC単剤を比較する第2/3相試験である本試験(KEYNOTE-010)が行われた。
シェーマ
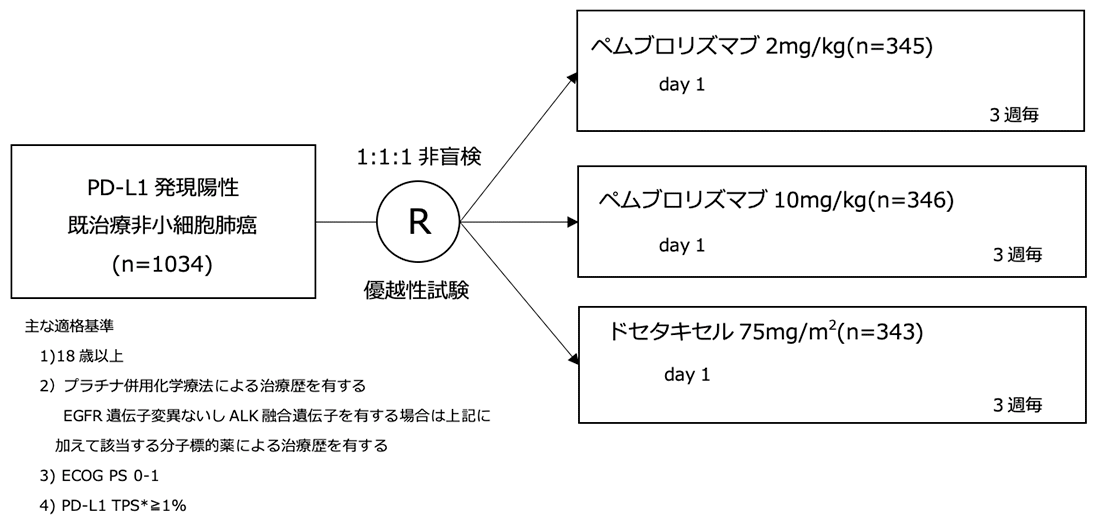
層別化因子:ECOG PS (0 vs 1), 地域 (東アジア vs それ以外)
* TPS (tumor proportion score): PD-L1を発現している腫瘍細胞の割合
** PembからDOCへのクロスオーバーは認められない
統計学的事項
主要評価項目:
本試験の主要評価項目は、全体集団 (PD-L1発現陽性; TPS≧1%) およびPD-L1発現強陽性集団 (TPS≧50%) それぞれにおける、全生存期間(OS)および無増悪生存期間(PFS)とした。本試験はDOC群を対照群とし、全体集団におけるPemb群のOSのハザード比 (HR) が0.7、TPS≧50%集団におけるPemb群のOSのHRが0.55となることを検証する優越性試験として設計された。検出力を80%、片側α=0.00825と設定すると、550イベントが必要と見込まれ、16か月の登録期間、8か月のフォローアップ期間から920例が必要と計算された。登録数はイベント数に応じて変更され、TPS≧50%の集団で3群合計200イベントが発生するまで登録が行われた。試験全体のαを片側2.5% (PFSに0.35%、OSに2.15%が割り当てられた) とし、それぞれのエンドポイントに対して多重性の調整 (Hochberg法, Bonferroni法, ゲートキーピング法) が行われた。ゲートキーピング法を用いて、PD-L1発現強陽性集団 (TPS≧50%) の解析で統計的有意差がついた場合、その有意水準は全体集団 (TPS≧1%) に対する解析に再分配された。OSの最終解析については、PFSの解析結果 (中間解析および最終解析) に応じて、TPS≧50%と全体集団のそれぞれで0.825-1%の有意水準を用いて検定が行われた。試験結果:
- 2013年8月~2015年2月の期間に202施設から1034例が登録され、Pemb2mg/kg群に345例、Pemb10mg/kg群に346例、DOC群に343例が割付けられた。
- 患者背景は各群で差を認めなかった。
- フォローアップ期間中央値は全群で13.1か月であった。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.71 (95%CI 0.58-0.88) p=0.0008 |
|
| Pemb 2mg/kg (n=345) | 10.4ヶ月 | 9.4-11.9 | |
| DOC (n=343) | 8.5ヶ月 | 7.5-9.8 |
| 中央値 | 95%信頼区間 | HR 0.61 (95%CI 0.49-0.75) p<0.0001 |
|
| Pemb 10mg/kg (n=346) | 12.7ヶ月 | 10.0-17.3 | |
| DOC (n=343) | 8.5ヶ月 | 7.5-9.8 |
- 全体集団(TPS≧1%)において、Pemb2mg/kg、Pemb10mg/kgのいずれの用量でもDOC群と比較して有意にOSの延長を認めた。
- TPS≧50%の集団において、Pemb2mg/kg (14.9ヶ月 vs 8.2ヶ月; HR 0.54[95%CI 0.38-0.77]; p=0.0002), 10mg/kg (17.3ヶ月 vs 8.2ヶ月; HR 0.5 [95%CI 0.36-0.70]; p<0.0001) のいずれの用量でもDOC群と比較してOSを有意に延長した。
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 0.88 (95%CI 0.74-1.05) P=0.07 |
|
| Pemb 2mg/kg (n=345) | 3.9ヶ月 | 3.1-4.1 | |
| DOC (n=343) | 4.0ヶ月 | 3.1-4.2 |
| 中央値 | 95%信頼区間 | HR 0.79 (95%CI 0.66-0.94) P=0.004 |
|
| Pemb 10mg/kg (n=346) | 4.0ヶ月 | 2.7-4.3 | |
| DOC (n=343) | 4.0ヶ月 | 3.1-4.2 |
- 全体集団(TPS≧1%)において、PFSはいずれも有意差をみとめなかった。
- TPS≧50%の集団において、Pemb2mg/kg (5.0ヶ月 vs 4.1ヶ月; HR 0.59[95%CI 0.44-0.78]; p=0.0001), 10mg/kg (5.2ヶ月 vs 4.1ヶ月; HR 0.59 [95%CI 0.45-0.78]; p<0.0001) のいずれの用量でもDOC群と比較してPFSを有意に延長した。
3. 奏効割合
| 奏効割合 | ||
|---|---|---|
| Pemb 2mg/kg | 18% | p=0.0005 |
| Pemb 10mg/kg | 18% | p=0.0002 |
| DOC | 9% |
- 全体集団(TPS≧1%)において、Pemb2mg/kg、Pemb10mg/kgのいずれの用量でもDOCと比較して奏効割合が有意に高かった。
4. 有害事象
| PEMB 2MG/KG (N=339) | PEMB 10MG/KG (N=343) | DOC (N=309) | ||||
|---|---|---|---|---|---|---|
| Any grade | Grade 3-5 | Any grade | Grade 3-5 | Any grade | Grade 3-5 | |
| 全有害事象 | 215(63%) | 43(13%) | 226(66%) | 55(16%) | 251(81%) | 109(35%) |
| いずれかの群で≧10%で起こる有害事象 | ||||||
| 食思不振 | 46(14%) | 3(1%) | 33(10%) | 1(<1%) | 49(16%) | 3(1%) |
| 疲労 | 46(14%) | 4(1%) | 49(14%) | 6(2%) | 76(25%) | 11(4%) |
| 悪心 | 37(11%) | 1(<1%) | 31(9%) | 2(1%) | 45(15%) | 1(<1%) |
| 皮疹 | 29(9%) | 1(<1%) | 44(13%) | 1(<1%) | 14(5%) | 0(0%) |
| 下痢 | 24(7%) | 2(1%) | 22(6%) | 0(0%) | 56(18%) | 7(2%) |
| 無力症 | 20(6%) | 1(<1%) | 19(6%) | 2(1%) | 35(11%) | 6(2%) |
| 口内炎 | 13(4%) | 0(0%) | 7(2%) | 1(<1%) | 43(14%) | 3(1%) |
| 貧血 | 10(3%) | 3(1%) | 14(4%) | 1(<1%) | 40(13%) | 5(2%) |
| 脱毛 | 3(1%) | 0(0%) | 2(1%) | 0(0%) | 101(33%) | 2(1%) |
| 好中球減少症 | 1(<1%) | 0(0%) | 1(<1%) | 0(0%) | 44(14%) | 38(12%) |
| PEMB群で2例以上に発生した注目すべき有害事象 | ||||||
| 甲状腺機能低下症 | 28(8%) | 0(0%) | 28(8%) | 0(0%) | 1(<1%) | 0(0%) |
| 肺臓炎 | 16(5%) | 7(2%) | 15(4%) | 7(2%) | 6(2%) | 2(1%) |
| 甲状腺機能亢進症 | 12(4%) | 0(0%) | 20(6%) | 1(<1%) | 3(1%) | 0(0%) |
| 大腸炎 | 4(1%) | 3(1%) | 2(1%) | 1(<1%) | 0(0%) | 0(0%) |
| 皮膚障害 | 4(1%) | 3(1%) | 7(2%) | 6(2%) | 2(1%) | 2(1%) |
| 膵炎 | 3(1%) | 2(1%) | 0(0%) | 0(0%) | 0(0%) | 0(0%) |
| 副腎不全 | 2(1%) | 0(0%) | 3(1%) | 1(<1%) | 0(0%) | 0(0%) |
| 筋炎 | 2(1%) | 0(0%) | 1(<1%) | 0(0%) | 1(<1%) | 0(0%) |
| 甲状腺炎 | 2(1%) | 0(0%) | 0(0%) | 0(0%) | 0(0%) | 0(0%) |
| 自己免疫性肝炎 | 1(<1%) | 1(<1%) | 2(1%) | 0(0%) | 0(0%) | 0(0%) |
| 下垂体機能低下症 | 1(<1%) | 1(<1%) | 1(<1%) | 1(<1%) | 0(0%) | 0(0%) |
| 1型糖尿病 | 1(<1%) | 1(<1%) | 2(1%) | 1(<1%) | 0(0%) | 0(0%) |
5. サブ解析
- サブグループ解析では、性別や年齢、PSなどにかかわらずPemb群でOSが良好な傾向を示した。
- EGFR遺伝子陽性サブグループではOSはHR0.88 (95%CI 0.45-1.70) であったが、PFSはHR 1.79 (95%CI 0.94-3.42) とDOC群で良好であった。
結語
PD-L1陽性の既治療進行非小細胞肺癌において、Pembは2mg/kg群、10mg/kg群のいずれにおいてもDOC群と比較し全生存期間を延長した。Pembの有害事象としては、免疫関連有害事象が特徴的であったが、毒性は許容される範囲であった。
執筆:慶應義塾大学病院 呼吸器内科 助教 堀内 康平 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 助教 朝尾 哲彦 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 助教 朝尾 哲彦 先生