| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 非小細胞肺癌 | 一次治療 | 第3相 | 全生存期間 | 国際 | あり |
試験名 :KEYNOTE-042
レジメン:ペムブロリズマブ vs 化学療法
登録期間:2014年12月9日〜2017年3月6日
背景
ペムブロリズマブ(Pemb)は、ヒト化IgG4モノクローナル抗PD-1抗体である。進行非小細胞肺がんに対するPembの有効性と、腫瘍細胞表面のPD-L1発現量の上昇との間には相関関係がある。KEYNOTE-024試験において、腫瘍細胞表面のPD-L1発現スコア(TPS)が50%以上の進行非小細胞肺癌305例に対して、一次治療としてのPembは化学療法よりも有意に無増悪生存期間と全生存期間を延長させた。本試験は、PD-L1 TPSが1%以上の進行非小細胞肺がんを対象に、一次治療としてPembとプラチナ製剤を用いた化学療法を比較・検討するランダム化第3相試験である。
シェーマ
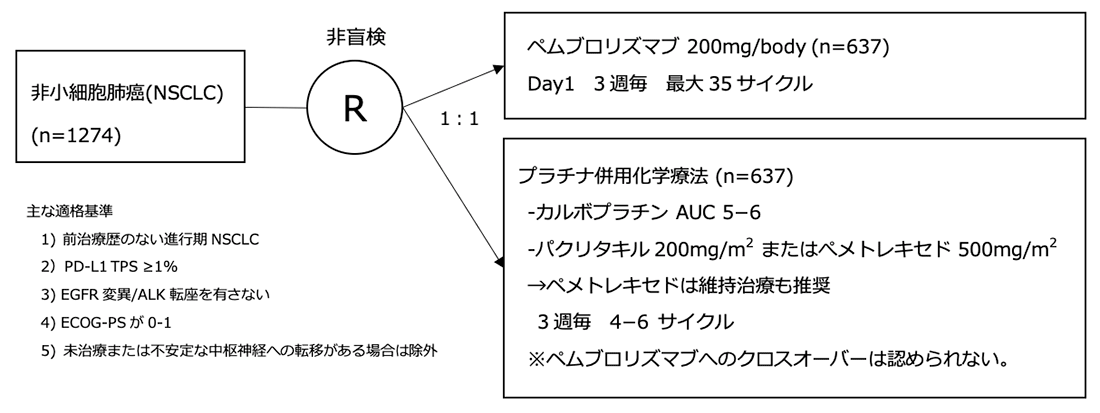
統計学的事項
主要評価項目:PD-L1 TPS 50%以上、20%以上、1%以上の集団の全生存期間
2014年当初、本試験の主要評価項目はPD-L1 TPSが50%以上の患者群での全生存期間(OS)であったが、KEYNOTE−010試験とCheckMate−026試験の結果に基づき、患者登録終了後の2017年4月に、主要評価項目をPD-L1 TPSが50%以上、20%以上、1%以上のそれぞれの患者群でのOSへ変更した。50%以上、20%以上、1%以上の順に評価を行い、先行する仮説での優越性が確立された場合にのみ次の検定を行なうこととした。Pembと化学療法のOSを比較した場合、非比例ハザードとなる可能性を考慮してピースワイズハザード比(HR)を使用した。登録期間が約26ヵ月、最小フォローアップ期間は19ヵ月、試験脱落率が0.003/月と仮定し、片側αが0.025としてPembのTPS 50%以上におけるHR 0.65を見込むと、約1240例の症例数に対して、398例の死亡イベントが確認されたときに、検出力は99%と計算された。またTPS 20%以上において、治療期間0−6ヵ月間のHR 0.80、および治期期間6ヵ月後のHR 0.64を見込むと557例の死亡イベントで検出力は98%と計算された。TPS 1%以上において、治療期間0−6ヵ月間のHR 0.92、および治期期間6ヵ月後のHR 0.73を見込むと900例の死亡イベントで検出力は91%と計算された。最初の中間解析は、最後の患者が登録されてから約6カ月後に計画され、2回目の中間解析は、最初の患者の登録から38.3ヶ月後に実施された。本論文は2回目の中間解析の結果に基づくものである。
試験結果:
- 2014年12月9日〜2017年3月6日の期間に1275例をPemb群(638例)と化学療法群(637例)に無作為に割り付けた。Pemb群で1例が治療前に死亡し、ITT集団には1274例が含まれた。
- TPSが50%以上の患者は599例(47%)、TPSが20%以上の患者は818例(64%)であった。
- 患者背景の特徴は、両群間およびTPS集団間で偏りは認められなかった。
- 有効性解析のデータカットオフは2018年2月26日。フォローアップ期間の中央値は12.8ヶ月であった。
- Pemb群で240例(38%)、化学療法群で282例(44%)が1レジメン以上の後治療を受け、そのうち免疫チェックポイント阻害剤はそれぞれ19例(3%)、126例(20%)で投与された。
1. 全生存期間:主要評価項目
| PD-L1≧50% | 中央値 | 95%信頼区間(CI) | HR 0.69 (0.56−0.85) p=0.0003 |
| Pemb群 | 20.0ヶ月 | 15.4−24.9 | |
| 化学療法群 | 12.2ヶ月 | 10.4−14.2 |
| PD-L1≧20% | 中央値 | 95%信頼区間(CI) | HR 0.77 (0.64−0.92) p=0.002 |
| Pemb群 | 17.7ヶ月 | 15.3−22.1 | |
| 化学療法群 | 13.0ヶ月 | 11.6−15.3 |
| PD-L1≧1% | 中央値 | 95%信頼区間(CI) | HR 0.81 (0.71−0.93) p=0.0018 |
| Pemb群 | 16.7ヶ月 | 13.9−19.7 | |
| 化学療法群 | 12.1ヶ月 | 11.3−13.3 |
- PD-L1 TPSが50%以上の集団で356例、TPS20%以上の集団で496例、TPS1%以上の集団で809例が死亡した。
- 24ヵ月生存割合は、 Pemb群と化学療法群でそれぞれ、TPS50%以上で45%と30%、TPS20%以上で41%と30%、TPS1%以上で39%と28%であった。
- 探索的評価項目として、PD-L1 TPSが1-49%の集団では、生存期間中央値はPemb群で13.4ヵ月(95%CI:10.7−18.2)、化学療法群で12.1ヵ月(11.0−14.0)であり、両群のカプランマイヤー曲線はクロスしており、有意差がなかった。
2. 無増悪生存期間
| PD-L1≧50% | 中央値 | 95%信頼区間(CI) | HR 0.81 (0.67−0.99) p=0.0170 |
| Pemb群 | 7.1ヶ月 | 5.9−9.0 | |
| 化学療法群 | 6.4ヶ月 | 6.1−6.9 |
| PD-L1≧20% | 中央値 | 95%信頼区間(CI) | HR 0.94 (0.80−1.11) |
| Pemb群 | 6.2ヶ月 | 5.1−7.8 | |
| 化学療法群 | 6.6ヶ月 | 6.2−7.3 |
| PD-L1≧1% | 中央値 | 95%信頼区間(CI) | HR 1.07 (0.94−1.21) |
| Pemb群 | 5.4ヶ月 | 4.3−6.2 | |
| 化学療法群 | 6.5ヶ月 | 6.3−7.0 |
- TPS50%以上の集団における無増悪生存期間の有意性は、事前に規定された片側p値の境界0.0146に達さなかった。そのためTPS20%以上と1%以上の集団で優越性を検証しなかった。
3. 奏効割合
| PD-L1≧50% | 奏効割合 | 95%信頼区間(CI) |
|---|---|---|
| Pemb群 | 39% | 34−45 |
| 化学療法群 | 32% | 27−38 |
| PD-L1≧20% | 奏効割合 | 95%信頼区間(CI) |
|---|---|---|
| Pemb群 | 33% | 29−38 |
| 化学療法群 | 29% | 25−34 |
| PD-L1≧1% | 奏効割合 | 95%信頼区間(CI) |
|---|---|---|
| Pemb群 | 27% | 24−31 |
| 化学療法群 | 27% | 23−30 |
- 奏効期間の中央値は、Pemb群では全TPS集団において20.2カ月、化学療法群ではTPS50%以上、20%以上、1%以上でそれぞれ10.8カ月、8.3カ月、8.3カ月であった。
4. 有害事象
| 有害事象(AE) | PEMB群(N=636) | 化学療法群(N=615) | ||
|---|---|---|---|---|
| 全Grade | Grade 3-5 | 全Grade | Grade 3-5 | |
| 全有害事象 | 399(63%) | 113(18%) | 553(90%) | 252(41%) |
| 治療中止につながったAE | 57(9%) | 48(8%) | 58(9%) | 43(7%) |
| 死亡につながったAE | 13(%) | 13(2%) | 14(2%) | 14(2%) |
| 5%以上に生じたAE | ||||
| 疲労感 | 50(8%) | 3(<1%) | 102(17%) | 8(1%) |
| 皮膚そう痒 | 46(7%) | 2(<1%) | 15(2%) | 0 |
| 皮疹 | 46(7%) | 3(<1%) | 27(4%) | 0 |
| ALT上昇 | 45(7%) | 9(1%) | 53(9%) | 5(<1%) |
| 肺炎 | 43(7%) | 20(3%) | 0 | 0 |
| AST上昇 | 41(6%) | 4(<1%) | 42(7%) | 2(<1%) |
| 食欲減退 | 40(6%) | 5(<1%) | 109(18%) | 9(1%) |
| 貧血 | 35(6%) | 4(<1%) | 229(37%) | 80(13%) |
| 下痢 | 34(5%) | 5(<1%) | 46(7%) | 1(<1%) |
| 嘔気 | 31(5%) | 0 | 184(30%) | 7(1%) |
| 関節痛 | 27(4%) | 0 | 46(7%) | 0 |
| 無力症 | 27(4%) | 3(<1%) | 60(10%) | 10(2%) |
| 筋痛 | 20(3%) | 1(<1%) | 50(8%) | 0 |
| 嘔吐 | 15(2%) | 0 | 97(16%) | 2(<1%) |
| 白血球減少症 | 10(2%) | 0 | 35(6%) | 10(2%) |
| 便秘 | 8(1%) | 0 | 68(11%) | 0 |
| 口内炎 | 7(1%) | 0 | 31(5%) | 0 |
| 好中球減少症 | 5(<1%) | 1(<1%) | 88(14%) | 46(7%) |
| 末梢感覚神経障害 | 3(<1%) | 0 | 41(7%) | 6(1%) |
| 血小板減少症 | 3(<1%) | 1(<1%) | 56(9%) | 10(2%) |
| 白血球数減少 | 3(<1%) | 0 | 71(12%) | 32(5%) |
| 好中球数減少 | 2(<1%) | 0 | 86(14%) | 54(9%) |
| 血小板数減少 | 2(<1%) | 0 | 64(10%) | 20(3%) |
| 末梢神経障害 | 1(<1%) | 0 | 50(8%) | 5(<1%) |
| 免疫関連有害事象 | 177(28%) | 51(8%) | 44(7%) | 9(%1) |
| 甲状腺機能低下症 | 77(12%) | 1(<1%) | 9(1%) | 0 |
| 肺臓炎 | 53(8%) | 22(3%) | 3(<1%) | 1(<1%) |
| 甲状腺機能亢進症 | 39(6%) | 1(<1%) | 4(<1%) | 0 |
| 重症皮膚反応 | 15(2%) | 11(2%) | 2(<1%) | 1(<1%) |
| インフュージョンリアクション | 10(2%) | 1(<1%) | 26(4%) | 6(1%) |
| 甲状腺炎 | 10(2%) | 0 | 0 | 0 |
| 肝炎 | 9(1%) | 7(1%) | 0 | 0 |
| 腸炎 | 7(1%) | 4(<1%) | 2(<1%) | 1(<1%) |
| 副腎不全 | 4(<1%) | 2(<1%) | 1(<1%) | 0 |
| 下垂体炎 | 3(<1%) | 3(<1%) | 0 | 0 |
| 腎炎 | 3(<1%) | 1(<1%) | 0 | 0 |
| 心筋炎 | 1(<1%) | 1(<1%) | 0 | 0 |
| 膵炎 | 1(<1%) | 0 | 0 | 0 |
- グレード3以上の治療関連有害事象は、Pemb群636例中113例(18%)、化学療法群615例中252例(41%)に発現し、それぞれ13例(2%)、14例(2%)で死亡に至った。治療中止に至った有害事象はそれぞれ57人(9%)、58人(9%)だった。
- 免疫関連有害事象はPemb群で177例(28%)、化学療法群で44例(7%)に発現した。Pemb群で5例以上に発生したGrade3以上の免疫関連有害事象は、肺炎、重症皮膚反応、肝炎であった。
結語
ALK融合またはEGFR変異のない、PD-L1 TPS1%以上の局所進行非小細胞肺がん患者において、Pemb単剤治療は、リスク・ベネフィットを考慮すると一次治療の選択肢の一つになり得る。
執筆:千葉大学医学部附属病院 呼吸器内科 池田 英樹 先生
監修:神奈川県立循環器呼吸器病センター 呼吸器内科 医長 池田 慧 先生
監修:神奈川県立循環器呼吸器病センター 呼吸器内科 医長 池田 慧 先生