| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 扁平上皮非小細胞肺癌 | 一次治療 | 第3相 | 全生存期間 無増悪生存期間 |
国際 | あり |
試験名 :KEYNOTE-407
レジメン:カルボプラチン+パクリタキセル/nab-パクリタキセル+ペムブロリズマブvs カルボプラチン+パクリタキセル/nab-パクリタキセル+プラセボ
登録期間:2016年8月19日〜2017年12月28日
背景
プラチナ併用化学療法もしくは抗PD-1抗体であるペムブロリズマブ(Pemb)単剤療法 (PD-L1発現スコア(TPS)≧50%の場合) が扁平上皮非小細胞肺癌 (NSCLC) の標準初回治療となっている。非扁平上皮NSCLCの一次治療では、Pembとプラチナ併用化学療法の併用が全生存期間を延長させることが示されているが、扁平上皮NSCLCでは、Pembとプラチナ併用化学療法を併用する有効性は示されていない。本試験では、扁平上皮NSCLCに対してPembとプラチナ併用化学療法を併用する有効性を検証した第3相試験である。
シェーマ
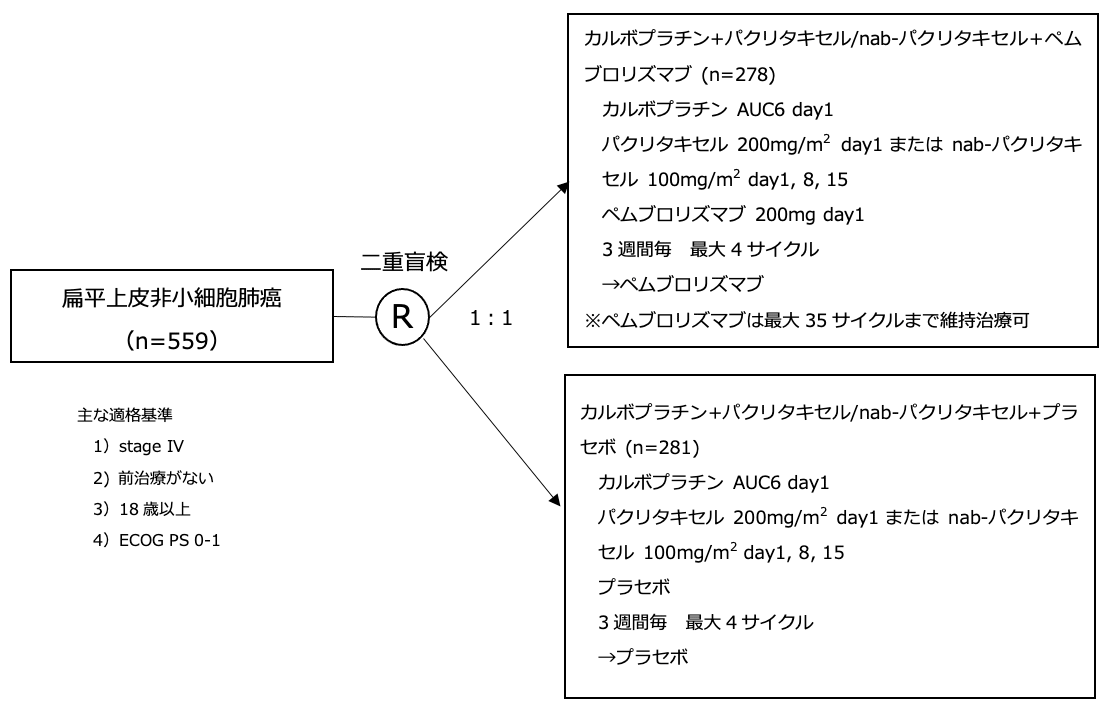
※維持療法としてペムブロリズマブまたはプラセボを病勢進行または有害事象で中止となるまで使用する
※病勢進行後のペムブロリズマブへのクロスオーバー可
層別化因子:PD-L1 TPS (≧1%、<1%)、タキサン系薬剤(パクリタキセル、nab-パクリタキセル)、登録施設の地域(東アジア、東アジア以外)
統計学的事項
主要評価項目:
本試験の主要評価項目は、全生存期間(OS)と無増悪生存期間(PFS)、副次評価項目は、客観的奏効割合、奏効期間、安全性とした。また、PD-L1発現割合に応じたPFSとOS、客観的奏効割合を探索的に評価した。有効性は治療群に割り振られたすべての症例(intention-to treat population)、安全性は少なくとも1回以上割り付けられた治療を受けたすべての症例(as-treated population)で評価した。OS、PFS、奏効期間の推定にKaplan-Meier法を使用し、OSとPFSの比較に層別ログランク検定を使用した。ハザード比の算出には層別化Cox比例ハザードモデルを使用した。本試験では、560例中415例で病勢進行または死亡のイベントが発生した場合、片側α 0.01で病勢進行または死亡のハザード比 0.70を検出力 90%で検出し、361例で死亡のイベントが発生した場合、片側α 0.01で死亡のハザード比 0.70を検出力 85%で検出できるデザインとした。
本試験では、中間解析を2回、最終解析を1回行う予定であったが、長期の治療効果を明らかにするために、中間解析を3回、最終解析を1回行うデザインに変更された。2018年5月21日をカットオフとした2回目の中間解析でOS及びPFSの有効性が示され、本論文は2回目の中間解析の結果である。
試験結果:
- 2016年8月19日~2017年12月28日に125施設の559症例が無作為化され、Pemb併用群に278例、プラセボ併用群に281例が割り付けられた。
- PD-L1発現スコア(TPS)≧1%は63.1%、パクリタキセルを使用した症例は60.1%、東アジア人は19.0%であった。
- 追跡期間の中央値は7.8か月(0.1-19.1か月)であった。
- Pemb併用群とプラセボ併用群において患者背景に違いは認めなかった。
- 後治療として、プラセボ併用群のうち75例がPemb単剤へクロスオーバーされ、14例は本試験外でPD-1/L1抗体が投与された。
1. OS(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.64 (95%信頼区間:0.49-0.85) P<0.001 |
|
| Pemb併用群 | 15.9ヶ月 | 13.2ヵ月-NR* | |
| プラセボ併用群 | 11.3ヶ月 | 9.5-14.8ヵ月 |
*NR: Not Reached
- PD-L1発現スコアのサブグループ解析における12ヵ月生存割合は、PD-L1 TPS≧50%でPemb併用群63.4% vsプラセボ併用群 51.0%(ハザード比0.64(95%信頼区間:0.37-1.10))、1-49%で65.9% vs 50.0%(ハザード比0.57(95%信頼区間:0.36-0.90))、1%未満で64.2% vs 43.3%(ハザード比0.61(95%信頼区間:0.38-0.98))であった。
2. PFS(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.56 (95%信頼区間:0.45-0.70) P<0.001 |
|
| Pemb併用群 | 6.4ヶ月 | 6.2-8.3ヵ月 | |
| プラセボ併用群 | 4.8ヶ月 | 4.3-5.7ヵ月 |
- PD-L1発現スコアのサブグループ解析におけるPFSの中央値は、PD-L1 TPS≧50%でPemb併用群8.0か月 vsプラセボ併用群 4.2か月(ハザード比0.37(95%信頼区間:0.24-0.58))、1-49%の群で7.2か月 vs 5.2か月(ハザード比0.57(95%信頼区間:0.39-0.80))、1%未満で6.3か月 vs 5.3か月(ハザード比0.68(95%信頼区間:0.47-0.98))であった。
3. 客観的奏効割合
| 中央値 | 95%信頼区間 | |
|---|---|---|
| Pemb併用群 | 57.9% | 51.9-63.8% |
| プラセボ併用群 | 38.4% | 32.7-44.4% |
4. 奏効期間
| 奏効期間中央値 | 範囲 | |
|---|---|---|
| Pemb併用群 | 7.7ヶ月 | 1.1+*-14.7+ヵ月 |
| プラセボ併用群 | 4.8ヶ月 | 1.3+-15.8+ヵ月 |
*「+」はデータカットオフの時点で病勢増悪がみられないことを示す
5. 有害事象
| Pemb併用群 (N=278) | プラセボ併用群 (N=280) | |||
|---|---|---|---|---|
| Any Grade | Grade 3-5 | Any Grade | Grade 3-5 | |
| 全ての有害事象 | 273(98.2%) | 194(69.8%) | 274(97.9%) | 191(68.2%) |
| すべての治療薬剤の中止につながった有害事象 | 37(13.3%) | 34(12.2%) | 18 (6.4%) | 18 (6.4%) |
| 治療薬剤の一部が中止になった有害事象 | 65 (23.4%) | 54(19.4%) | 33(11.8%) | 29 (10.4%) |
| ペムブロリズマズまたはプラセボが 中止になった有害事象 |
48 (17.3%) | 44(15.8%) | 22(7.9%) | 21 (7.5%) |
| カルボプラチンが中止になった有害事象 | 31 (11.2%) | 28(10.1%) | 21(7.5%) | 19 (6.8%) |
| パクリタキセルまたはnab-パクリタキセルが 中止になった有害事象 |
44 (15.8%) | 33(11.9%) | 28(10.0%) | 24 (8.6%) |
| 死亡につながった有害事象 | 23(8.3%) | 23(8.3%) | 18(6.4%) | 18(6.4%) |
| 観察者が治療レジメンによって 死亡につながったと判断した有害事象 |
10(3.6%) | 10(3.6%) | 6 (2.1%) | 6 (2.1%) |
| 15%以上に生じた有害事象 | ||||
| 貧血 | 148(53.2%) | 43(15.5%) | 145(51.8%) | 57(20.4%) |
| 脱毛 | 128(46.0) | 1 (0.4%) | 102(36.4%) | 3 (1.1%) |
| 好中球減少症 | 105(37.8%) | 63(22.7%) | 92(32.9%) | 69(24.6%) |
| 悪心 | 99(35.6%) | 3 (1.1%) | 90(32.1%) | 4 (1.4%) |
| 血小板減少症 | 85(30.6%) | 19(6.8%) | 65(23.2%) | 18(6.4%) |
| 下痢 | 83(29.9%) | 11(4.0%) | 65(23.2%) | 6 (2.1%) |
| 食欲不振 | 68(24.5%) | 6 (2.2%) | 82(29.3%) | 5 (1.8%) |
| 便秘 | 64(23.0%) | 2 (0.7%) | 61(21.8%) | 3 (1.1%) |
| 疲労 | 63(22.7%) | 9 (3.2%) | 72(25.7%) | 11(3.9%) |
| 衰弱 | 60(21.6%) | 6 (2.2%) | 59(21.1%) | 10(3.6%) |
| 関節痛 | 57(20.5%) | 4 (1.4%) | 40(14.3%) | 2 (0.7%) |
| 末梢性ニューロパチー | 57(20.5%) | 3 (1.1%) | 45(16.1%) | 2 (0.7%) |
| 嘔吐 | 45(16.2%) | 1 (0.4%) | 33(11.8%) | 6 (2.1%) |
| 咳嗽 | 37(13.3%) | 2 (0.7%) | 47(16.8%) | 3 (1.1%) |
| 呼吸困難 | 36(12.9%) | 4 (1.4%) | 45(16.1%) | 3 (1.1%) |
| 免疫関連有害事象 | Pemb併用 (N=278) | プラセボ併用群 (N=280) | ||
|---|---|---|---|---|
| Any Grade | Grade 3-5 | Any Grade | Grade 3-5 | |
| すべての免疫関連有害事象 | 80(28.8%) | 30(10.8%) | 24(8.6%) | 9 (3.2%) |
| 甲状腺機能低下症 | 22 (7.9%) | 1 (0.4%) | 5 (1.8%) | 0 |
| 甲状腺機能亢進症 | 20 (7.2%) | 1 (0.4%) | 2 (0.7%) | 0 |
| 肺臓炎 | 18 (6.5%) | 7 (2.5%) | 6 (2.1%) | 3 (1.1%) |
| インフュージョン・リアクション | 8 (4.1%) | 4 (1.4%) | 6 (2.1%) | 1 (0.4%) |
| 大腸炎 | 7 (2.5%) | 6 (2.2%) | 4 (1.4%) | 3 (1.1%) |
| 肝炎 | 5 (1.8%) | 5 (1.8%) | 0 | 0 |
| 重症皮膚反応 | 5 (1.8%) | 3 (1.1%) | 1 (0.4%) | 1 (0.4%) |
| 下垂体炎 | 3 (1.1%) | 2 (0.7%) | 0 | 0 |
| 甲状腺炎 | 3 (1.1%) | 1 (0.4%) | 0 | 0 |
| 腎炎 | 2 (0.7%) | 2 (0.7%) | 2 (0.7%) | 2 (0.7%) |
結語
進行期扁平上皮NSCLC患者の一次治療において、カルボプラチン+パクリタキセル/nab-パクリタキセル+Pembは、カルボプラチン+パクリタキセル/nab-パクリタキセル+プラセボと比較してPFS及びOSを有意に延長した。
執筆:横浜市立大学附属病院 呼吸器病学教室 久保 創介 先生
監修:静岡県立静岡がんセンター 呼吸器内科 医長 和久田 一茂 先生
監修:静岡県立静岡がんセンター 呼吸器内科 医長 和久田 一茂 先生