| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| EGFR遺伝子変異陽性非小細胞肺癌 | 一次治療 | 第3相 | 無増悪生存期間 | 東アジア | なし |
試験名 :Lux-Lung 6
レジメン:アファチニブ vs シスプラチン+ゲムシタビン
登録期間:2010年4月27日〜2011年11月16日
背景
非小細胞肺癌(NSCLC)のうち、上皮成長因子受容体(epidermal growth factor receptor:EGFR)遺伝子変異陽性例は約30-50%を占める。EGFR遺伝子変異陽性例に対して、第一世代のEGFRチロシンキナーゼ阻害薬(EGFR-TKI)の有効性が、複数の第3相試験で示された。アファチニブ(AFA)は、ErbBファミリーであるEGFR、HER2 (ErbB2)、HER4 (ErbB4) のATP 結合部位に共有結合して不可逆的にチロシンキナーゼのリン酸化を阻害する第二世代のEGFR-TKIとして開発された。本試験は、未治療EGFR陽性非小細胞肺癌の患者を対象として、第二世代EGFR-TKIのAFAと、従来の標準治療であるプラチナ併用化学療法を比較した多施設共同無作為化非盲検の第3相試験である。
シェーマ
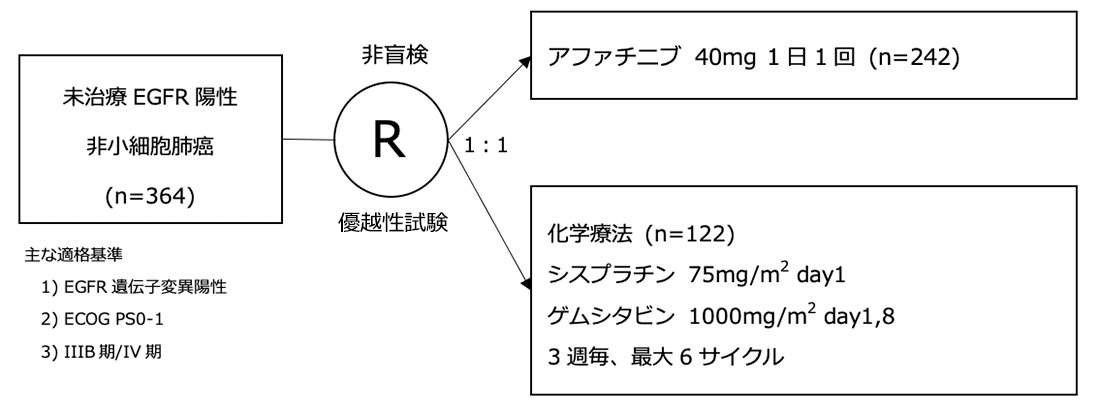
統計学的事項
主要評価項目:無増悪生存期間
本試験はEGFR遺伝子変異陽性例において、シスプラチン+ゲムシタビン併用療法(化学療法)を対照群としてAFA単剤群の優越性を検証した第3相試験である。過去の試験結果から、AFA群と化学療法群の無増悪生存期間(PFS)のハザード比が0.64となると仮定し、両側α=0.05、検出力=90%と設定し、必要なPFSのイベント数は計217、必要症例数は計330例となった。試験結果:
- 2010年4月27日〜2011年11月16日の期間に、東アジアの36施設より364例が登録され、AFA群に242例、化学療法群に122例が割り付けられた。
- データカットオフは2012年10月29日で、221のPFSイベントが確認された。
- PFSの追跡期間中央値は16.6ヵ月であった。
- ECOG PS0の症例の割合が、化学療法群で33.6%、AFA群で19.8%と、化学療法群で高かった。その他、両群間で患者背景に明らかな差は認められなかった。
1. 独立判定委員会判定による無増悪生存期間(主要評価項目)
| 中央値 | 95%信頼区間 (CI) | HR 0.28 (95%CI: 0.20-0.39) p < 0.0001 |
|
| AFA群 | 11.0月 | 9.7-13.7ヵ月 | |
| 化学療法群 | 5.6ヶ月 | 5.1-6.7ヵ月 |
2. 全生存期間
| 中央値 | 95%CI | HR 0.95 (95%CI: 0.68-1.33) p = 0.76 |
|
| AFA群 | 22.1ヶ月 | 20.0ヵ月-NA | |
| 化学療法群 | 22.2ヶ月 | 18.0ヵ月-NA |
3. 奏効割合
| 中央値 | OR 7.28 (95%CI 4.36-12.18) p < 0.0001 |
|
| AFA群 | 66.9% | |
| 化学療法群 | 23.0% |
4. 有害事象
| AFA群 (N=239) | 化学療法群 (N=113) | |||||
|---|---|---|---|---|---|---|
| Grade 1-2 | Grade 3 | Grade 4 | Grade 1-2 | Grade 3 | Grade 4 | |
| 皮疹 | 158 (66%) | 34 (14%) | 1 (<1%) | 10 (9%) | 0 | 0 |
| 爪囲炎 | 78 (33%) | 0 | 0 | 0 | 0 | 0 |
| 下痢 | 198 (83%) | 13 (5%) | 0 | 12 (11%) | 0 | 0 |
| ALT上昇 | 44 (18%) | 4 (2%) | 0 | 15 (13%) | 2 (2%) | 1 (1%) |
| AST上昇 | 35 (15%) | 1 (<1%) | 0 | 10 (9%) | 2 (2%) | 0 |
| 肺臓炎 | 0 | 0 | 1 (<1%) | 0 | 0 | 0 |
| 食欲不振 | 21 (9%) | 3 (1%) | 0 | 44 (39%) | 2 (2%) | 0 |
| 疲労 | 23 (10%) | 1 (<1%) | 0 | 40 (35%) | 1 (1%) | 0 |
| 好中球数減少 | 4 (2%) | 1 (<1%) | 0 | 31 (27%) | 20 (18%) | 10 (9%) |
| 貧血 | 12 (5%) | 1 (<1%) | 0 | 21 (19%) | 8 (7%) | 2 (2%) |
| 血小板減少 | 1 (<1%) | 1 (<1%) | 0 | 10 (9%) | 8 (7%) | 3 (3%) |
治療と関連したGrade3以上の有害事象はAFA群 86例 (36%)、化学療法群 68例 (60%) で認められた。
多く認めた有害事象は、AFA群で下痢、皮疹、粘膜炎、化学療法群で嘔吐、悪心、好中球数減少、白血球減少であった。
治療関連死亡は両群でそれぞれ1例に認められた。
5. サブ解析:無増悪生存期間(AFA群 vs 化学療法群)
| 症例数 | ハザード比 | 95%信頼区間 | ||
|---|---|---|---|---|
| 全体 | 364 | 0.28 | 0.20-0.39 | |
| 性別 | 男性 | 126 | 0.36 | 0.21-0.63 |
| 女性 | 238 | 0.24 | 0.16–0.35 | |
| 年齢 | <65歳 | 278 | 0.30 | 0.21-0.43 |
| ≥65歳 | 86 | 0.16 | 0.07-0.40 | |
| ECOG PS | 0 | 89 | 0.22 | 0.12-0.41 |
| 1 | 275 | 0.29 | 0.20-0.43 | |
| 遺伝子変異 | Del19 | 186 | 0.20 | 0.13–0.33 |
| L858R | 138 | 0.32 | 0.19–0.52 | |
| その他 | 40 | 0.55 | 0.22-1.43 |
結語
未治療EGFR遺伝子変異陽性NSCLC患者において、AFAはプラチナ併用化学療法と比較して無増悪生存期間の有意な延長を示した。本試験の結果により、AFAはEGFR遺伝子変異陽性NSCLCの標準治療の一つとなり得ることが示された。
執筆:静岡県立静岡がんセンター 呼吸器内科 レジデント 宮脇 太一 先生
監修:静岡県立静岡がんセンター 呼吸器内科 医長 和久田 一茂 先生
監修:静岡県立静岡がんセンター 呼吸器内科 医長 和久田 一茂 先生