| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 非小細胞肺癌 | 二次治療 三次治療 |
第3相 | 全生存期間 | 国際 | あり |
試験名 :OAK
レジメン:アテゾリズマブ vs ドセタキセル
登録期間:2014年3月11日〜 2015年4月29日
背景
非小細胞肺癌において、PD-1阻害薬であるニボルマブやペムブロリズマブはドセタキセル(DOC) と比較して全生存期間を延長することが示されてきた。アテゾリズマブ(Atezo)は抗PD-L1抗ヒト化モノクローナル抗体であり、PD-L1だけでなくB7-1 (CD80) も阻害することから、PD-1阻害薬とは異なる効果が得られる可能性があった。第2相試験であるPOPLAR試験でAtezoがDOCに比して全生存期間を延長したことを受けて、今回第3相試験であるOAK試験が行われた。
シェーマ
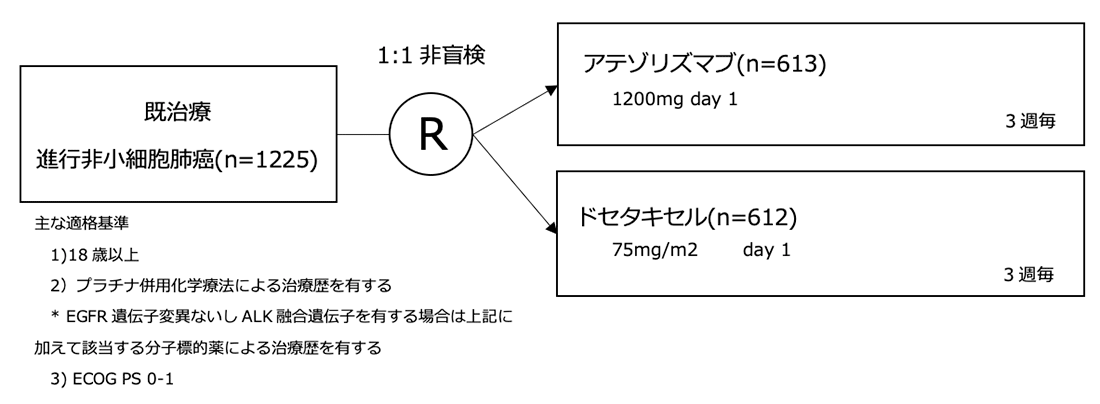
層別化因子:PD-L1発現 (IC0 vs IC1 vs IC2 vs IC3), 前治療レジメン数 (1 vs 2), 組織型 (非扁平上皮 vs 扁平上皮)
統計学的事項
主要評価項目:
本試験の主要評価項目はintention-to-treat (ITT) 集団及びPD-L1 TC1/2/3またはIC1/2/3の集団 (腫瘍細胞または腫瘍浸潤免疫細胞におけるPD-L1 発現≧1%) における全生存期間(OS)とした。ITT集団における、DOCに対するAtezoのOSのハザード比 (HR) を0.73 (OS中央値: DOC群10ヶ月, Atezo群 13.7ヶ月), 両側α 3%, 検出力 95.3%とし、TC1/2/3またはIC1/2/3集団におけるHR を0.63, 両側α 2%, 検出力 98.6%としたところ、850例の登録が必要となると考えられた (全体のαを両側5%に調整)。
当初、予定症例数は850例 (一次解析対象集団)であったが、PD-L1強発現 (TC3またはIC3) 集団における比較を行うために、プロトコール改訂により1300例に変更された。
注:TC: 腫瘍細胞 (tumor cell) におけるPD-L1発現スコア、IC: 腫瘍浸潤免疫細胞 (tumor-infiltrating immune cell) におけるPD-L1発現スコア (PD-L1免疫染色はSP142クローンを用いて行われた)
TC0: PD-L1発現<1%; TC1: PD-L1発現1-5%; TC2: PD-L1発現5-50%; TC3: PD-L1発現≧50%
IC0: PD-L1発現<1%; IC1: PD-L1発現1-5%; IC2: PD-L1発現5-10%; IC3: PD-L1発現≧10%
試験結果:
- 2014年3月~2015年4月の期間に194施設から1225例が登録された。このうち一次解析対象集団は850例で、Atezo群に425例、DOC群に425例が割り付けられた。一次解析対象集団のフォローアップ期間中央値は全群で21か月であった。
- 患者背景は各群で差を認めなかった。
- DOC群では、試験治療終了後に17%で後治療として免疫チェックポイント阻害剤が投与された。
1. 全生存期間(主要評価項目)
ITT
| 中央値 | 95%信頼区間 | HR 0.73 (95%CI 0.62-0.87) p=0.0003 |
|
| Atezo (n=425) | 13.8ヶ月 | 11.8-15.7 | |
| DOC (n=425) | 9.6ヶ月 | 8.6-11.2 |
TC1/2/3またはIC1/2/3 (PD-L1発現≧1%)
| 中央値 | 95%信頼区間 | HR 0.74 (95%CI 0.58-0.93) p=0.0102 |
|
| Atezo (n=425) | 15.7ヶ月 | 12.6-18.0 | |
| DOC (n=425) | 10.3ヶ月 | 8.8-12.0 |
TC0かつIC0 (PD-L1発現<1%)
| 中央値 | 95%信頼区間 | HR 0.75 (95%CI 0.59-0.96) p=0.0215 |
|
| Atezo (n=425) | 12.6ヶ月 | 9.6-15.2 | |
| DOC (n=425) | 8.9ヶ月 | 7.7-11.5 |
- 主要評価項目であるOS中央値は、ITT集団, TC1/2/3またはIC1/2/3集団のいずれにおいてもAtezo群で統計学的に有意に延長した。
- PD-L1発現がない (TC0かつIC0) 集団においてもAtezo群でOSを延長した。
2. 無増悪生存期間
ITT
| 中央値 | 95%信頼区間 | HR 0.95 (95%CI 0.82-1.10) P=0.4928 |
|
| Atezo (n=425) | 2.8ヶ月 | 2.6-3.0 | |
| DOC (n=425) | 4.0ヶ月 | 3.3-4.2 |
TC1/2/3またはIC1/2/3 (PD-L1発現≧1%)
| 中央値 | 95%信頼区間 | HR 0.91 (95%CI 0.74-1.12) P=0.3806 |
|
| Atezo (n=425) | 2.8ヶ月 | 2.6-4.0 | |
| DOC (n=425) | 4.1ヶ月 | 2.9-4.3 |
TC0かつIC0 (PD-L1発現<1%)
| 中央値 | 95%信頼区間 | HR 1.00 (95%CI 0.80-1.25) P=0.9924 |
|
| Atezo (n=425) | 2.6ヶ月 | 1.7-2.9 | |
| DOC (n=425) | 4.0ヶ月 | 3.1-4.2 |
- PFSは両群で有意差を認めなかった (ITT集団、TC1/2/3またはIC1/2/3集団)。
- TC3またはIC3集団に限り無増悪生存期間の延長を認めた(HR0.63; 95%CI 0.43-0.91; p=0.0123)。
3. 奏効割合
ITT
| 奏効割合 | |
|---|---|
| Atezo (n=425) | 14% |
| DOC (n=425) | 13% |
TC1/2/3またはIC1/2/3 (PD-L1発現≧1%)
| 奏効割合 | |
|---|---|
| Atezo (n=425) | 18% |
| DOC (n=425) | 16% |
- 奏効割合は両群で同程度であった (ITT集団、TC1/2/3またはIC1/2/3集団)。
4. 有害事象 (安全性解析対象集団)
| ATEZO (N=609) | DOC (N=578) | |||
|---|---|---|---|---|
| Any grade | Grade 3-4 | Any grade | Grade 3-4 | |
| 全治療関連有害事象 | 390(64%) | 90(15%) | 496(86%) | 247(43%) |
| 倦怠感 | 163(26.8%) | 17 (2.8%) | 205 (35.5%) | 23 (4.0%) |
| 食思不振 | 143 (23.5%) | 2 (0.3%) | 136 (23.5%) | 9 (1.6%) |
| 咳嗽 | 141 (23.2%) | 2 (0.3%) | 105 (18.2%) | 1 (0.2%) |
| 悪心 | 108 (17.7%) | 4 (0.7%) | 131 (22.7%) | 2 (0.3%) |
| 下痢 | 94 (15.4%) | 4 (0.7%) | 141 (24.4%) | 11 (1.9%) |
| 疲労 | 116 (19.0%) | 8 (1.3%) | 114 (19.7%) | 13 (2.2%) |
| 息切れ | 118 (19.4%) | 15 (2.5%) | 112 (19.4%) | 14 (2.4%) |
| 貧血 | 70 (11.5%) | 14 (2.3%) | 136 (23.5%) | 33 (5.7%) |
| 脱毛 | 3 (0.5%) | 0 | 202 (34.9%) | 1 (0.2%) |
| 便秘 | 107 (17.6%) | 2 (0.3%) | 82 (14.2%) | 1 (0.2%) |
| 発熱 | 108 (17.7%) | 1 (0.2%) | 76 (13.1%) | 1 (0.2%) |
| 浮腫 | 54 (8.9%) | 1 (0.2%) | 82 (14.2%) | 3 (0.5%) |
| 嘔吐 | 74 (12.2%) | 2 (0.3%) | 62 (10.7%) | 4 (0.7%) |
| 関節痛 | 73 (12.0%) | 3 (0.5%) | 58 (10.0%) | 1 (0.2%) |
| 筋痛 | 39 (6.4%) | 1 (0.2%) | 91 (15.7%) | 4 (0.7%) |
| 背部痛 | 67 (11.0%) | 7 (1.1%) | 42 (7.3%) | 4 (0.7%) |
| 好中球減少症 | 10 (1.6%) | 3 (0.5%) | 90 (15.6%) | 75 (13.0%) |
| 末梢神経障害 | 24 (3.9%) | 0 | 65 (11.2%) | 7 (1.2%) |
| 筋骨格系の疼痛 | 64 (10.5%) | 4 (0.7%) | 25 (4.3%) | 1 (0.2%) |
| 口内炎 | 19 (3.1%) | 1 (0.2%) | 63 (10.9%) | 11 (1.9%) |
| 味覚障害 | 18 (3.0%) | 0 | 58 (10.0%) | 0 |
| 発熱性好中球減少症 | 1 (0.2%) | 1 (0.2%) | 62 (10.7%) | 62 (10.7%) |
- 免疫関連有害事象としては肺臓炎を6例(1%)、肝炎を2例(<1%)、大腸炎を2例(<1%)に認めた。
- 有害事象による中止はAtezo群で8%, DOC群で19%であった。Atezo群では治療関連死亡はなかった。
5. PFSのサブグループ解析
- OSのサブグループ解析では、PD-L1発現レベル、年齢 (65歳以上, 65歳未満)、組織型(非扁平上皮癌, 扁平上皮癌)、脳転移の有無に関わらずAtezo群でOSが良好であった。
- ただし、EGFR変異症例ではDOC群でOSが良好な傾向を示した(HR1.24 [95%CI 0.71-2.18))。
結語
既治療進行非小細胞肺癌において、AtezoはPD-L1の発現量に関わらずDOCより全生存期間を統計学的に有意に延長した。毒性は許容されるものであった。
執筆:慶應義塾大学病院 呼吸器内科 助教 堀内 康平 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 助教 朝尾 哲彦 先生
監修:順天堂大学大学院 医学研究科 呼吸器内科学 助教 朝尾 哲彦 先生