| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| NTRK 融合遺伝子陽性固形癌 | 不問 | 第1, 2相 | 奏効割合 | 米国 | なし |
試験名 :成人第1相試験, SCOUT(小児 第1/2相), NAVIGATE(成人/青年期 第2相バスケット)
レジメン:ラロトレクチニブ
登録期間:2015年5月〜2017年2月
背景
NTRK1/2/3 遺伝子は、トロポミオシン受容体キナーゼ(TRK) A/B/Cをコードしている。TRKの発現は主に神経系に限定され、これらのキナーゼは痛み、固有受容、食欲、記憶の調節に関与している。NTRK融合遺伝子により生じたTRK融合タンパクはキメラタンパクの過剰発現を引き起こし、恒常的に活性化し、リガンド非依存性の下流シグナル伝達をもたらす。これらのTRK融合タンパクは、原発部位に関わらず、がんの広がりや増殖を促進する発がん性ドライバーとして作用する。NTRK融合遺伝子は、小児および成人に発生する様々な癌において同定され、全固形腫瘍の最大1%に関与しているとされている。
ラロトレクチニブは強い選択性をもってTRKA、TRKB、TRKCを阻害する小分子化合物であり、その有効性はあらゆる年齢・腫瘍タイプの患者を対象とした開発プログラムで評価された。そのプログラムには、成人を対象とした第1相試験、小児を対象とした第1/2相試験、青年期および成人を対象とした第2相バスケット試験の3試験が含まれていた。本研究は、これらの3試験全体でラロトレクチニブの投与を受けたTRK融合タンパク陽性固形癌(最初の連続登録症例 55例)の安全性と有効性を統合解析したものである。
ラロトレクチニブは強い選択性をもってTRKA、TRKB、TRKCを阻害する小分子化合物であり、その有効性はあらゆる年齢・腫瘍タイプの患者を対象とした開発プログラムで評価された。そのプログラムには、成人を対象とした第1相試験、小児を対象とした第1/2相試験、青年期および成人を対象とした第2相バスケット試験の3試験が含まれていた。本研究は、これらの3試験全体でラロトレクチニブの投与を受けたTRK融合タンパク陽性固形癌(最初の連続登録症例 55例)の安全性と有効性を統合解析したものである。
シェーマ
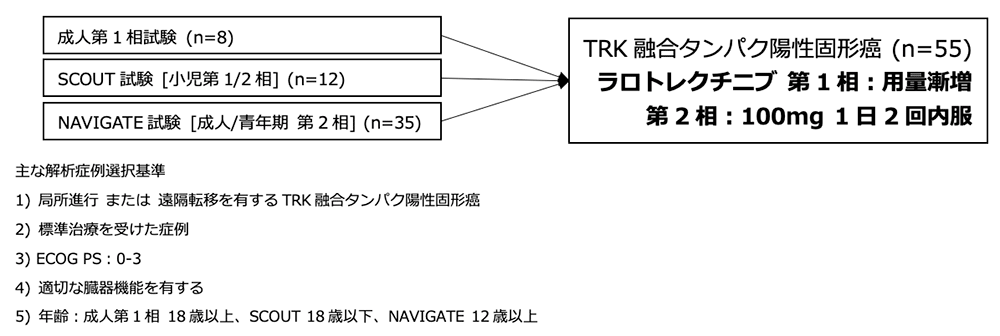
- TRK融合タンパク陽性固形癌の55人目が本プログラムに登録された時点で小児を対象としたSCOUT試験の第2相部分は開始されておらず、SCOUT試験の第2相部分の症例は本解析に含まれていない。
- 体表面積が1m2以上の成人/小児にはラロトレクチニブ 100mg 1日2回内服が選択されたが、体表面積が1m2未満の小児には100mg/m2 1日2回の投与量が選択された。
- 成人第1相試験とSCOUT試験は登録前のTRK融合タンパクの存在は必須ではなかったが、TRK融合タンパクが前向きに特定された症例は本統合解析の有効性評価に含まれた。
統計学的事項
主要評価項目 :奏効割合(中央判定)
副次的評価項目:奏効割合(主治医判定)、奏効期間、無増悪生存期間、安全性
腫瘍縮小効果はRECIST version 1.1にて評価が行われた。統計学的設定は、真の奏効割合を少なくとも50%と仮定し、検出力80%、95%信頼区間(両側)の下限が30%とすると、必要症例数は55例であった。
試験結果:
- 2015年3月から2017年2月までの間に、RECIST version 1.1における評価可能病変を有するTRK融合タンパク陽性固形癌患者 55例が登録された。
1. 患者背景 (n=55)
| N (%) | ||
|---|---|---|
| 年齢 年齢分布 |
中央値 (範囲), 歳 2歳未満 2-5歳 6-14歳 15-39歳 40歳以上 |
45.0 (0.3-76.0) 6 (11) 5 (9) 1 (2) 12 (22) 31 (56) |
| 性別 | 男性 女性 |
29 (53) 26 (47) |
| ECOG PS | 0 1 2 |
24 (44) 27 (49) 4 (7) |
| 前治療レジメン数 | 0-1 2 3 |
27 (49) 9 (16) 19 (35) |
| 癌腫 | 唾液腺 乳腺類似分泌癌 他の軟部肉腫 小児型線維肉腫 甲状腺腫瘍 大腸腫瘍 肺腫瘍 黒色腫 消化管間質腫瘍 胆道癌 虫垂腫瘍 乳腺腫瘍 脳腫瘍 |
12 (22) 11 (20) 7 (13) 5 (9) 4 (7) 4 (7) 4 (7) 3 (5) 2 (4) 1 (2) 1 (2) 1 (2) |
| 中枢神経系への転移 | なし あり |
54 (98) 1 (2) |
| TRK 遺伝子異常 | NTRK1 NTRK2 NTRK3 |
45 (45) 1 (2) 29 (53) |
2. 奏効割合
| % | 主治医判定 (n=55) | 中央判定 (n=55) |
|---|---|---|
| 奏効割合 [95%信頼区間] |
80 [67-90] |
75 [61-85] |
| 最良効果 CR |
16 |
13 |
| PR | 64 | 62 |
| SD | 9 | 13 |
| PD | 11 | 9 |
| 評価不能 | 0 | 4 |
- 2例(4%)は臨床的増悪により早期に治療中止となったため、中央判定では評価不能とされた。
- がん腫、年齢、TRK融合タンパクの状況に関わらず、奏効例が観察された。
3. 奏効までの期間
| 中央値 | 範囲 | |
|---|---|---|
| 奏効までの期間 | 1.8ヶ月 | 0.9-6.4 |
- 観察期間中央値:8.3ヶ月(範囲:0.03-24.9+)の段階で奏効期間は中央値に達していなかった。
4. 奏効期間
| 6ヶ月奏効割合 | 12ヶ月奏効割合 | |
|---|---|---|
| 奏効例 (n=44) | 83% | 71% |
- 観察期間中央値:8.3ヶ月(範囲:0.03-24.9+)の段階で奏効期間は中央値に達していなかった。
5. 無増悪生存期間
| 6ヶ月無増悪生存割合 | 12ヶ月無増悪生存割合 | |
|---|---|---|
| 全症例 (n=55) | 73% | 55% |
- 観察期間中央値:9.9ヶ月(範囲:0.7-25.9+)の段階で無増悪生存期間は中央値に達していなかった。
- 1年後、奏効例の71%は継続中であり、全症例の55%が無増悪を維持していた。
- データカットオフ時点で、奏効した44例中36例(86%)で治療を継続しているか、治癒を目的とした手術が行われていた。
6. 有害事象 (CTCAE v4.0)
| (%) | 原因に関わらないすべての有害事象 | 治療関連有害事象 | ||||||
|---|---|---|---|---|---|---|---|---|
| Grade | 1 | 2 | 3 | 4 | 全 | 3 | 4 | 全 |
| AST or ALT増加 | 31 | 4 | 7 | 0 | 42 | 5 | 0 | 38 |
| 疲労 | 20 | 15 | 2 | 0 | 36 | 0 | 0 | 16 |
| 悪心 | 24 | 9 | 0 | 0 | 33 | 0 | 0 | 11 |
| 浮動性めまい | 25 | 4 | 2 | 0 | 31 | 2 | 0 | 25 |
| 悪心 | 22 | 7 | 2 | 0 | 31 | 2 | 0 | 16 |
| 貧血 | 9 | 9 | 11 | 0 | 29 | 2 | 0 | 9 |
| 下痢 | 15 | 13 | 2 | 0 | 29 | 0 | 0 | 5 |
| 便秘 | 24 | 4 | 0 | 0 | 27 | 0 | 0 | 16 |
| 咳嗽 | 22 | 4 | 0 | 0 | 25 | 0 | 0 | 2 |
| 体重増加 | 11 | 5 | 7 | 0 | 24 | 0 | 0 | 11 |
| 呼吸困難 | 9 | 9 | 0 | 0 | 18 | 0 | 0 | 2 |
| 頭痛 | 13 | 4 | 0 | 0 | 16 | 0 | 0 | 2 |
| 発熱 | 11 | 2 | 2 | 2 | 16 | 0 | 0 | 0 |
| 関節痛 | 15 | 0 | 0 | 0 | 15 | 0 | 0 | 2 |
| 背部痛 | 5 | 9 | 0 | 0 | 15 | 0 | 0 | 0 |
| 好中球数減少 | 0 | 7 | 7 | 0 | 15 | 2 | 0 | 9 |
- 臨床的に重大な有害事象は稀であり、ほとんどの有害事象がGrade 1-2であった(1038件中964件, 93%)。
- 主治医によりGrade 4-5の治療関連有害事象と考えられた事象はなく、5%を超えるGrade 3の治療関連有害事象も存在しなかった。
- 55例中、8例(15%)でラロトレクチニブの減量を要し、その原因はASTまたはALT増加(4例)、浮動性めまい(2例)、好中球数減少(2例)であり、全てGrade 2-3であった。減量を要した症例は全例、減量投与にて最良効果を維持した。
- 有害事象によるラロトレクチニブ投与中止例はいなかった。
7. 一次および獲得耐性
[一次耐性について]
- 全般的に奏効割合が高いにもかかわらず、6例(11%)の一次耐性(最良効果がPDと定義)が観察された。
- 1例は以前に別のTRK阻害剤で治療されており、ラロトレクチニブ投与前のシークエンス評価にてキナーゼドメインのATP結合部位にNTRK3 G623R変異が明らかになった(NTRK3 G623R変異とNTRK1 G595Rパラログは、キナーゼドメインのヌクレオチド結合ループの親水性溶媒曝露部分を変化させ、ラロトレクチニブ結合を立体的に妨害し、ラロトレクチニブの阻害効力を低下させる)。
- 残り5例中3例で腫瘍組織検体が利用可能であり、中央解析が行われた。TRK免疫組織化学検査では3例ともTRK融合タンパクの存在が確認されなかったため、自施設で実施された検査が偽陽性であったが、分子学的に同定された融合がタンパク質レベルで発現しなかった可能性が示された。
[獲得耐性について]
- 獲得耐性は少なくとも奏効または6ヶ月以上のSD維持後、ラロトレクチニブの投与中に増悪することと定義され、該当症例は10例であった。
- 融合に関与するNTRK 遺伝子に影響を与えるキナーゼドメイン変異が、反復検査を受けた9人の患者すべてから増悪後に得られた腫瘍または血漿サンプルで同定された。増悪時に観察されたキナーゼドメイン変異は、薬剤結合部位の入り口(NTRK1 G595RまたはNTRK3 G623R; 7例)、ゲートキーパー位置(NTRK1 F589L; 2例)、およびxDFG位置(NTRK1 G667SまたはNTRK3 G696A; 2例)に見つかった。
- 獲得耐性が発現した 10 例のうち 8人(80%)は、臨床的ベネフィットが持続していることから、病勢進行が認められた後もラロトレクチニブの投与を継続した。
結語
ラロトレクチニブは年齢や癌腫にかかわらず、TRK融合タンパク陽性固形癌に対して高く、持続的な有効性を示した。
執筆:香川大学医学部附属病院 がんセンター/腫瘍内科 病院講師 大北 仁裕 先生
監修:関西医科大学病院 がんセンター 学長特命准教授 佐竹 悠良 先生
監修:関西医科大学病院 がんセンター 学長特命准教授 佐竹 悠良 先生