| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 膵癌 | 補助化学療法 | 第3相 | 無病生存期間 | 国際 | なし |
試験名 :PRODIGE24-CCTG PA6
レジメン:FOLFIRINOX vs Gemcitabine
登録期間:2012年4月〜2016年10月
背景
膵癌は切除が唯一の根治が得られる治療法とされているが、切除のみでは5年生存割合は10%を下回る。これまで、根治切除が行われた患者に対する術後補助化学療法として、Gemcitabineやフッ化ピリミジン系薬剤の有用性が報告されているものの、2年で69~75%の患者で再発する。
遠隔転移を有する膵癌患者に対して5-FU/LV+イリノテカン+オキサリプラチン併用療法(FOLFIRINOX)はゲムシタビンと比較して生存期間を延長させることが示されおり、今回、膵癌の術後補助化学療法として、FOLFIRINOXの有用性をゲムシタビンと比較する国際共同非盲検比較第3相試験(PRODIGE24-CCTG PA6試験)の実施に至った。 [ClinicalTrials.gov Identifier:NCT01526135]
遠隔転移を有する膵癌患者に対して5-FU/LV+イリノテカン+オキサリプラチン併用療法(FOLFIRINOX)はゲムシタビンと比較して生存期間を延長させることが示されおり、今回、膵癌の術後補助化学療法として、FOLFIRINOXの有用性をゲムシタビンと比較する国際共同非盲検比較第3相試験(PRODIGE24-CCTG PA6試験)の実施に至った。 [ClinicalTrials.gov Identifier:NCT01526135]
シェーマ
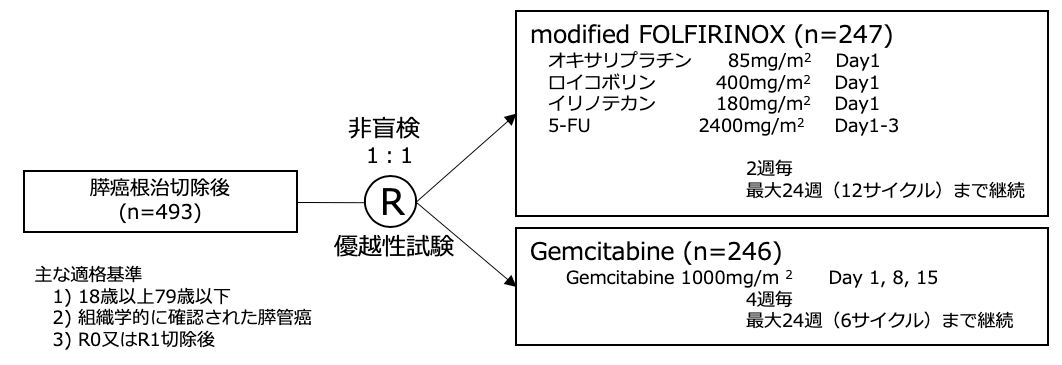
統計学的事項
主要評価項目:無病生存期間
本試験はGemcitabine群を対照として、 modified FOLFIRINOX群の3年無病生存割合が10%改善することを検証する優越性試験として設計され、検出力80%、両側α=0.05と設定し、490人の登録・342イベントが必要とされた。しかし、2018年2月5日に独立モニタリング委員会が早期の解析を勧告したため、314イベントが発生した時点でデータベースが固定され解析が行われた。試験結果:
- 2012年4月から2016年10月、フランスの58施設、カナダの19施設から493例が登録された。
- データカットオフは、観察期間中央値36.6ヶ月で行われた。
- 患者背景に大きな隔たりは認められなかった。
1. 無病生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.58 (95%C.I. 0.46-0.73) p<0.001 |
|
| modified FOLFIRINOX(n=247) | 21.6ヶ月 | 17.7-27.6 | |
| Gemcitabine(n=246) | 12.8ヶ月 | 11.7-15.2 |
2. 全生存期間
| 中央値 | 95%信頼区間 | HR 0.64 (95%C.I. 0.48-0.86) p=0.003 |
|
| modified FOLFIRINOX(n=247) | 54.4ヶ月 | 41.8-NR | |
| Gemcitabine(n=246) | 35.0ヶ月 | 28.7-43.9 | |
| NR: not reached |
3. 無遠隔転移生存期間
| 中央値 | 95%信頼区間 | HR 0.59 (95%C.I. 0.46-0.75) p<0.001 |
|
| modified FOLFIRINOX(n=247) | 30.4ヶ月 | 21.7-NR | |
| Gemcitabine(n=246) | 17.7ヶ月 | 14.2-21.5 |
4. がん特異的生存期間
| 中央値 | 95%信頼区間 | HR 0.63 (95%C.I. 0.47-0.85) p=0.003 |
|
| modified FOLFIRINOX(n=247) | NR | 47.3-NR | |
| Gemcitabine(n=246) | 36.4ヶ月 | 30.9-46.2 |
5. 有害事象
| modified FOLFIRINOX (n=238) | Gemcitabine (n=243) | |||
|---|---|---|---|---|
| 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | |
| 貧血 | 200 (84.7%) | 8 (3.4%) | 216 (89.3%) | 6 (2.5%) |
| 好中球数減少 | 157 (66.5%) | 67 (28.4%) | 154 (63.6%) | 63 (26.0%) |
| 発熱性好中球減少症 | 7 (3.0%) | 7 (3.0%) | 10 (4.1%) | 9 (3.7%) |
| 血小板数減少 | 111 (47.0%) | 3 (1.3%) | 122 (50.4%) | 11 (4.5%) |
| 疲労 | 199 (84.0%) | 26 (11.0%) | 187 (77.6%) | 11 (4.6%) |
| 下痢 | 200 (84.4%) | 44 (18.6%) | 118 (49.0%) | 9 (3.7%) |
| 嘔気 | 187 (78.9%) | 13 (5.5) | 133 (55.2%) | 2 (0.8%) |
| 腹痛 | 111 (46.8%) | 8 (3.4%) | 114 (47.3%) | 1 (0.4%) |
| 嘔吐 | 108 (45.6%) | 12 (5.1%) | 70 (29.0%) | 3 (1.2%) |
| 食欲減退 | 106 (44.7%) | 6 (2.5%) | 60 (24.9%) | 3 (1.2%) |
| 末梢性感覚ニューロパチー | 145 (61.2%) | 22 (9.3%) | 21 (8.7%) | 0 |
| 錯感覚 | 136 (57.4%) | 30 (12.7%) | 13 (5.4%) | 0 |
| 体重減少 | 90 (38.0%) | 3 (1.3%) | 49 (20.3%) | 1 (0.4%) |
| 発熱 | 39 (16.5%) | 1 (0.4%) | 78 (32.4%) | 1 (0.4%) |
| 粘膜炎 | 80 (33.8%) | 6 (2.5%) | 36 (14.9%) | 0 |
| 脱毛 | 64 (27.0%) | 0 | 47 (19.5%) | 0 |
| 便秘 | 49 (20.7%) | 0 | 52 (21.6%) | 0 |
| ALT増加 | 151 (64.0%) | 10 (4.2%) | 178 (73.6%) | 12 (5.0%) |
| AST増加 | 158 (66.9%) | 9 (3.8%) | 167 (69.0%) | 8 (3.3%) |
| ALP増加 | 173 (73.6%) | 5 (2.1%) | 111 (45.9%) | 5 (2.1%) |
| 高血糖 | 59 (24.9%) | 7 (3.0%) | 59 (24.4%) | 5 (2.1%) |
結語
根治切除後の膵癌患者に対するmodified FOLFIRINOXによる術後補助化学療法は、Gemcitabineと比較して、無病生存期間及び全生存期間を統計学的有意に延長させており、有害事象の発現割合は高いものの、新たな標準治療となり得る。
執筆:金沢大学 消化器内科 特任助教 寺島 健志 先生
監修:神奈川県立がんセンター 消化器内科(肝胆膵) 部長 上野 誠 先生
監修:神奈川県立がんセンター 消化器内科(肝胆膵) 部長 上野 誠 先生