| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌/食道胃接合部癌 | 3次治療以降 | 第3相 | 全生存期間 | アジア | あり |
試験名: ATTRACTION-2 [ClinicalTrials.gov Identifier:NCT02267343]
レジメン: ニボルマブ vs プラセボ
登録期間: 2014年11月〜2016年2月
シェーマ
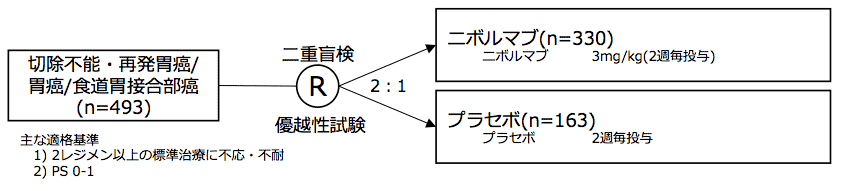
試験結果:
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | |
|---|---|---|
| ニボルマブ | 5.26ヶ月 | 4.60-6.37 |
| プラセボ | 4.14ヶ月 | 3.42-4.86 |
| HR 0.63 (95%C.I. 0.51-0.78) p<0.0001 |
||
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | |
|---|---|---|
| ニボルマブ | 1.61ヶ月 | 1.54-2.30 |
| プラセボ | 1.45ヶ月 | 1.45-1.54 |
| HR 0.60 (95%C.I. 0.49-0.75) p<0.0001 |
||
3. 奏効率
| 奏効率 | 95%信頼区間 | |
|---|---|---|
| ニボルマブ | 11.2% | 7.7-15.6 |
| プラセボ | 0% | 0-2.8 |
| p<0.0001 | ||
4. 病勢制御率
| 病勢制御率 | 95%信頼区間 | |
|---|---|---|
| ニボルマブ | 40.3% | 34.4-46.4 |
| プラセボ | 25% | 18.0-33.5 |
| OR 1.99(95%C.I. 1.24-3.17) p=0.0036 |
||
5. 有害事象
| ニボルマブ | プラセボ | |||
|---|---|---|---|---|
| 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | |
| そう痒症 | 30 (9%) | 0(0%) | 9(6%) | 0(0%) |
| 下痢 | 23(7%) | 2 (1%) | 3(2%) | 0(0%) |
| 皮疹 | 19(6%) | 0(0%) | 5(3%) | 0(0%) |
| 疲労 | 18(5%) | 2(1%) | 9(6%) | 2(1%) |
| 間質性肺疾患 | 6(2%) | 1(<1%) | 0(0%) | 0 (0%) |
| 大腸炎 | 2(1%) | 1(<1%) | 0(0%) | 0 (0%) |
結語
本試験でニボルマブの生存延長効果を示したことから、ニボルマブは既治療の進行胃癌患者に対する新しい治療オプションとなるだろう。現在、進行胃癌患者に対してより早い治療ラインで、非アジア人も含む臨床試験が進行中である。
Reference
Kang YK, et al. Lancet. 2017 Dec 2;390(10111):2461-2471
執筆:国立がん研究センター東病院 消化管内科 レジデント 中島 裕理先生