| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌/食道胃接合部癌 | 二次治療 | 第3相 | 全生存期間 | 国際 | なし |
試験名 :REGARD
レジメン:ラムシルマブ vs プラセボ
登録期間:2009年10月〜2012年1月
背景
進行胃腺癌に対する一次化学療法として標準的な殺細胞性抗癌剤が使用されるが、生存期間中央値は8~10ヶ月である。米国や欧州では、この一次化学療法後に使用する二次化学療法が未だ承認されていないのが現状である。
血管内皮増殖因子(VEGF)とVEGFレセプター2(VEGFR-2)を介したシグナル伝達と血管新生は胃癌の発症に重要な役割を有し、基礎的検討ではVEGFR-2の阻害は腫瘍の増殖や血管新生を抑えることが報告されている。また、胃癌症例においてVEGFの血中/腫瘍内濃度が腫瘍の増殖と生存期間の短縮に関与することも示されている。
ラムシルマブはVEGFR-2の細胞外ドメインに結合するヒト型IgG1モノクローナル抗体であり、VEGFリガンドの結合を遮断し、受容体の活性化を阻害する。
本試験は一次化学療法で不応/不耐となった進行胃癌/食道胃接合部癌患者に対し、ラムシルマブ単剤療法の有効性、安全性を検証することを目的にしたランダム化第3相比較試験である。
血管内皮増殖因子(VEGF)とVEGFレセプター2(VEGFR-2)を介したシグナル伝達と血管新生は胃癌の発症に重要な役割を有し、基礎的検討ではVEGFR-2の阻害は腫瘍の増殖や血管新生を抑えることが報告されている。また、胃癌症例においてVEGFの血中/腫瘍内濃度が腫瘍の増殖と生存期間の短縮に関与することも示されている。
ラムシルマブはVEGFR-2の細胞外ドメインに結合するヒト型IgG1モノクローナル抗体であり、VEGFリガンドの結合を遮断し、受容体の活性化を阻害する。
本試験は一次化学療法で不応/不耐となった進行胃癌/食道胃接合部癌患者に対し、ラムシルマブ単剤療法の有効性、安全性を検証することを目的にしたランダム化第3相比較試験である。
シェーマ
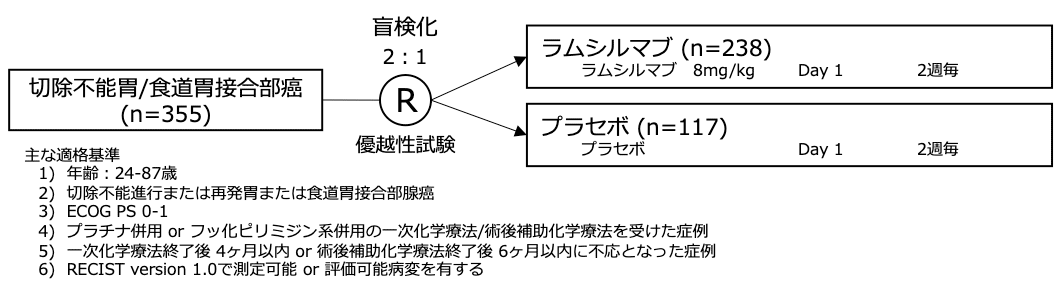
統計学的事項
主要評価項目:全生存期間
本試験は当初、プラセボ群を対照としてラムシルマブ群の全生存期間のハザード比が0.71となることを検証する優越性試験として設計され、検出力90%、両側α=0.05として、615例の登録が必要と設定された。しかし登録が進まず、全生存期間のハザード比が0.69となることを検証する優越性試験として再設計され、検出力80%、両側α=0.05として、348例の登録が必要と最終決定された。試験結果:
- 2009年10月から2012年1月の間に355例が登録され、238例がラムシルマブ群に、117例がプラセボ群に無作為割り付けされた。各群2例で実際の投与が行われず、安全性解析はラムシルマブ群 236例、プラセボ群 115例となった。
- 患者背景は概ねバランスがとれていたが、腹膜播種例はラムシルマブ群でわずかに低頻度だった(ラムシルマブ群 64例/27% vs プラセボ群 45例/38%)。
1. 全生存期間(主要評価項目)
| イベント数 (%) |
中央値 (四分位範囲) |
6ヶ月生存割合 (四分位範囲) |
12ヶ月生存割合 (四分位範囲) |
HR 0.776 (95%C.I. 0.603-0.998) p=0.047 |
|
| ラムシルマブ | 179 (75) |
5.2ヶ月 (2.3-9.9) |
41.8% (35.4-48.1) |
17.6% (11.8-24.3) |
|
| プラセボ | 99 (85) |
3.8ヶ月 (1.7-7.1) |
31.6% (23.2-40.2) |
11.8% (6.0-19.7) |
2. 全生存期間に関するサブ解析
- ECOG PS(1以上 vs 0)、原発部位(胃食道接合部 vs 胃)、腹膜播種(あり vs なし)で調整を行っても、ラムシルマブ群における有意な改善は変わらなかった。
- 割り付け調整因子を含めた項目で多変量解析を行ったが、有意な改善は変わらなかった(HR 0.767, 95%信頼区間 0.598-0.984, p=0.037)。
- 性別による解析では、男性:HR 0.676, 95%信頼区間 0.499-0.916、女性:HR 1.431, 95%信頼区間 0.852-2.405であったが、有意な交互作用はなかった(p=0.063)。
3. 無増悪生存期間
| 中央値 (四分位範囲) |
12週無増悪生存割合 (四分位範囲) |
HR 0.483 (95%C.I. 0.376-0.620) p<0.0001 |
|
| ラムシルマブ | 2.1ヶ月 (1.3-4.2) |
40.1% (33.6-46.4) |
|
| プラセボ | 1.3ヶ月 (1.1-2.1) |
15.8% (9.7-23.3) |
4. 奏効割合/病勢制御割合
| 最良効果 N (%) |
ラムシルマブ (n=238) |
プラセボ (n=117) |
p値 |
|---|---|---|---|
| CR PR SD PD NE |
1 (<1) 7 (3) 108 (45) 78 (33) 44 (18) |
0 (0) 3 (3) 24 (21) 63 (54) 27 (23) |
|
| 奏効割合 | 8 (3) | 3 (3) | 0.76 |
| 病勢制御割合 | 116 (49) | 27 (23) | <0.0001 |
5. 病勢制御期間
| 中央値 | 四分位範囲 | |
|---|---|---|
| ラムシルマブ | 4.2ヶ月 | 2.8-8.1 |
| プラセボ | 2.9ヶ月 | 2.7-4.3 |
p=0.036
6. 投与状況
- データカットオフ(2012年7月25日)の段階で、ラムシルマブ群 222例(93%)、プラセボ群 114例(97%)が治療中止となっていた。
- 治療中止理由で一番頻度が高いのは画像的/臨床的病勢進行で、次に有害事象であった。
- 治療期間中央値(四分位範囲):ラムシルマブ群 8週(6-16)、プラセボ群 6週(4-8)
- 相対用量強度は両群とも高かった(ラムシルマブ群 99.6%/プラセボ群 100%)。
- 試験治療後に後治療を受けた症例はラムシルマブ群よりプラセボ群で多かった。
7. 有害事象 (CTCAE ver.4.02)
| N (%) | ラムシルマブ (n=236) | プラセボ (n=115) | ||
|---|---|---|---|---|
| 全Grade | Grade 3以上 | 全Grade | Grade 3以上 | |
| 疲労 | 84 (36) | 15 (6) | 46 (40) | 11 (10) |
| 食欲不振 | 57 (24) | 8 (3) | 26 (23) | 4 (3) |
| 嘔吐 | 47 (20) | 6 (3) | 29 (25) | 5 (4) |
| 貧血 | 35 (15) | 15 (6) | 17 (15) | 9 (8) |
| 高血圧 | 38 (16) | 18 (8) | 9 (8) | 3 (3) |
| 出血 | 30 (13) | 8 (3) | 13 (11) | 3 (3) |
| 動脈塞栓症 | 4 (2) | 3 (1) | 0 (0) | 0 (0) |
| 静脈塞栓症 | 9 (4) | 3 (1) | 8 (7) | 5 (4) |
| 蛋白尿 | 7 (3) | 1 (<1) | 3 (3) | 0 (0) |
- 高血圧は全Grade、Grade 3以上ともに、ラムシルマブ群で高率であったが、Grade 4は出現しなかった。
- Grade 3以上の動脈塞栓症はラムシルマブ群でわずかに高頻度だったが、有意差はなかった(p=0.55)。
- 出血、静脈塞栓症、蛋白尿、消化管穿孔、瘻孔形成、インフュージョンリアクションの頻度はラムシルマブ群での増加は認めなかった。
- 治療関連死亡:ラムシルマブ群 5例/2%(心筋梗塞、胃出血、消化管穿孔 2例、肺炎)、プラセボ群 2例/2%(消化管穿孔、肺梗塞)
8. QOL
- 本試験では治療開始前、6週後、12週後、18週後の時点で質問票(EORTC QLQ-C13 ver.3.0)を用いてQOL評価を予定していた。
- 治療開始後6週時点でのアンケートはラムシルマブ群 114例(48%)、プラセボ群 29例(25%)しか得ることができなかった。
- 治療開始後6週時点でのQOLアンケートの状況は以下の通りである。
| N (%) | 改善 | 安定 | 悪化 | データなし |
|---|---|---|---|---|
| ラムシルマブ | 23 (30%) | 58 (24%) | 29 (12%) | 128 (54%) |
| プラセボ | 5 (4%) | 11 (9%) | 10 (9%) | 91 (78%) |
9. ECOG PS 2以上まで悪化するまでの期間
| 中央値 | 四分位範囲 | HR 0.586 (95%C.I. 0.414-0.829) p=0.002 |
|
| ラムシルマブ | 5.1ヶ月 | 1.9-16.8 | |
| プラセボ | 2.4ヶ月 | 1.3-未到達 |
結語
ラムシルマブは一次化学療法に不応となった胃/食道胃接合部癌症例に対して、単剤で生存期間の延長を示した最初の分子標的薬剤である。本試験の結果はVEGFR-2を介したシグナル伝達が進行胃癌治療において重要な治療標的となることを確認した。
執筆:香川大学医学部附属病院 腫瘍内科 助教 大北 仁裕 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生