| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌/食道胃接合部癌 | 一次治療 | 第3相 | 全生存期間 | 国際 | あり |
試験名 :ToGA
レジメン:化学療法単独 vs 化学療法+トラスツズマブ
登録期間:2005年9月〜2008年12月
背景
HER2(上皮成長因子受容体2)は胃癌の腫瘍形成に関わる重要なバイオマーカーであり、重要なドライバーであるという報告が増えている。過去の報告では腫瘍の7〜34%で増幅または過剰発現が示されており、一部の研究では胃癌のHER2陽性状態が予後不良および疾患の進行性と関連することが示唆されている。
HER2を標的とするモノクローナル抗体であるトラスツズマブはHER2陽性乳癌の標準治療薬となっているが、HER2過剰発現を有する他癌腫に対しては有効性が確立していない。胃癌の前臨床モデルにおいてトラスツズマブはカペシタビン、シスプラチン、あるいは両者との併用において相加的な抗腫瘍効果が認められていることから、HER2過剰発現を有する胃癌/食道胃接合部癌の一次化学療法におけるトラスツズマブ上乗せの安全性と有効性を検証する目的に本試験が実施された。
HER2を標的とするモノクローナル抗体であるトラスツズマブはHER2陽性乳癌の標準治療薬となっているが、HER2過剰発現を有する他癌腫に対しては有効性が確立していない。胃癌の前臨床モデルにおいてトラスツズマブはカペシタビン、シスプラチン、あるいは両者との併用において相加的な抗腫瘍効果が認められていることから、HER2過剰発現を有する胃癌/食道胃接合部癌の一次化学療法におけるトラスツズマブ上乗せの安全性と有効性を検証する目的に本試験が実施された。
シェーマ
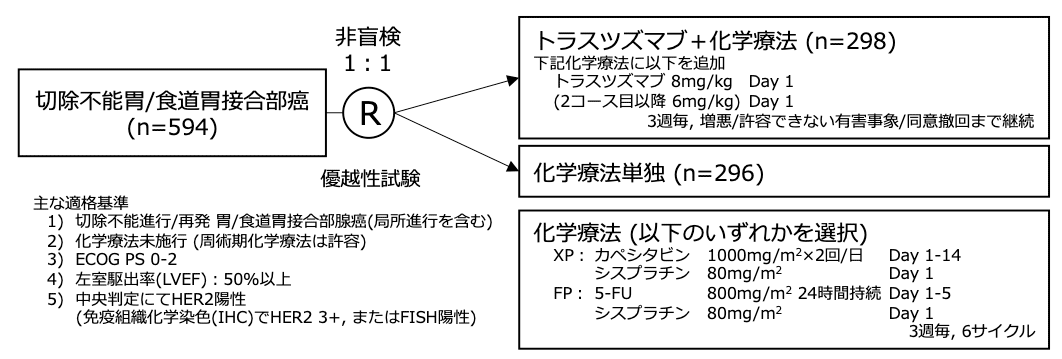
統計学的事項
主要評価項目:全生存期間
本試験は化学療法単独群を対照としてトラスツズマブ+化学療法群の全生存期間のハザード比が0.77となることを検証する優越性試験として設計され、検出力80%、両側α=0.05として、460イベントが必要と設定された。10%の脱落例を考慮し、必要症例数を584例と設定した。試験結果:
- 2005年9月から2008年12月の間に日本を含む24ヶ国、122施設にて3,665例がHER2検査を受け、810例がHER2陽性の診断となった。その内、適格規準を満たした594例が無作為割り付けされた。同意撤回や適格規準違反等にて10例が除外され、最終的な解析対象は化学療法単独群 290例、トラスツズマブ+化学療法群 294例となった。
- 観察期間中央値は化学療法単独群 17.1ヶ月(四分位範囲 9-25)、トラスツズマブ+化学療法群 18.6ヶ月(四分位範囲 11-25)であった。
1. 患者背景
- 化学療法に関して、XPレジメンを選択したのは化学療法単独群 255例(88%)、トラスツズマブ+化学療法群 256例(87%)であった。
- HER2高発現(IHC 3+ or IHC 2+かつFISH陽性)は化学療法単独群 218例(75%)、トラスツズマブ+化学療法群 228例(78%)であった。
- 前化学療法歴のある症例は化学療法単独群 12例(4%)、トラスツズマブ+化学療法群 27例(9%)であり、統計学的有意差を認めた(p<0.0146)。
2. 全生存期間 (主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.74 (95%C.I. 0.60-0.91) p=0.0046 |
|
| トラスツズマブ+化学療法 | 13.8ヶ月 | 12-16 | |
| 化学療法単独 | 11.1ヶ月 | 10-13 |
3. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 0.71 (95%C.I. 0.59-0.85) p=0.0002 |
|
| トラスツズマブ+化学療法 | 6.7ヶ月 | 6-8 | |
| 化学療法単独 | 5.5ヶ月 | 5-6 |
4. 奏効割合
| 奏効割合 | オッズ比 1.70 (95%C.I. 1.22-2.38) p=0.0017 |
|
| トラスツズマブ+化学療法 | 47% | |
| 化学療法単独 | 35% |
5. HER2発現状況による全生存期間
| 症例数 | トラスツズマブ +化学療法 |
化学療法単独 | HR (95%C.I.) | |
|---|---|---|---|---|
| 事前設定の探索的解析 IHC 0/FISH陽性 IHC 1+/FISH陽性 IHC 2+/FISH陽性 IHC 3+/FISH陽性 IHC 3+/FISH陰性 |
61 70 159 256 15 |
10.6ヶ月 8.7ヶ月 12.3ヶ月 17.9ヶ月 17.5ヶ月 |
7.2ヶ月 10.2ヶ月 10.8ヶ月 12.3ヶ月 17.7ヶ月 |
0.92 (0.48-1.76) 1.24 (0.70-2.20) 0.75 (0.51-1.11) 0.58 (0.41-0.81) 0.83 (0.20-3.38) |
| 事後解析 IHC 0 or 1+/FISH陽性 IHC 2+/FISH陽性 or IHC 3+ |
131 446 |
10.0ヶ月 16.0ヶ月 |
8.7ヶ月 11.8ヶ月 |
1.07 (0.70-1.62) 0.65 (0.51-0.83) |
- トラスツズマブ使用の有無と、事後解析で分類した2つのHER2グループの間に有意な交互作用を認めた(p=0.036)。
6. 有害事象 (NCI-CTCAE ver.3.0)
| N (%) | トラスツズマブ+化学療法 (n=294) | 化学療法単独 (n=290) | ||
|---|---|---|---|---|
| 全Grade | Grade 3-4 | 全Grade | Grade 3-4 | |
| 全有害事象 | 292 (99) | 201 (68) | 284 (98) | 198 (68) |
| 悪心 | 197 (67) | 22 (7) | 184 (63) | 21 (7) |
| 嘔吐 | 147 (50) | 18 (6) | 134 (46) | 22 (8) |
| 下痢 | 109 (37) | 27 (9) | 80 (28) | 11 (4) |
| 口腔粘膜炎 | 72 (24) | 2 (1) | 43 (15) | 6 (2) |
| 好中球数減少 | 157 (53) | 79 (27) | 165 (57) | 88 (30) |
| 貧血 | 81 (28) | 36 (12) | 61 (21) | 30 (10) |
| 血小板数減少 | 47 (16) | 14 (5) | 33 (11) | 8 (3) |
| 発熱性好中球数減少 | 15 (5) | 15 (5) | 8 (3) | 8 (3) |
| 食欲不振 | 135 (46) | 19 (6) | 133 (46) | 18 (6) |
| 疲労 | 102 (35) | 12 (4) | 82 (28) | 7 (2) |
| 体重減少 | 69 (23) | 6 (2) | 40 (14) | 7 (2) |
| 発熱 | 54 (18) | 3 (1) | 36 (12) | 0 |
| 粘膜炎 | 37 (13) | 6 (2) | 18 (6) | 2 (1) |
| 鼻咽頭炎 | 37 (13) | 0 | 17 (6) | 0 |
| 悪感 | 23 (8) | 1 (<1) | 0 | 0 |
- 化学療法単独群と比較して、トラスツズマブ+化学療法群では下痢、口腔粘膜炎、貧血、血小板数減少、疲労、悪寒、体重減少、発熱、粘膜炎、鼻咽頭炎がわずかに高頻度であった。
- 重篤な有害事象は、化学療法単独群 81例(28%)、トラスツズマブ+化学療法群 95例(32%)に生じた。
- Grade 3以上の重篤なインフュージョンリアクションはトラスツズマブ+化学療法群の17例(6%)で生じたが、死亡には至らなかった。
- 心臓に関する有害事象は化学療法単独群 18例(6%)、トラスツズマブ+化学療法群 17例(6%)で両群に差はなく、稀であった。
- 心機能障害(LVEFが50%未満へ10%以上低下することと定義)は両群で低頻度だった(化学療法単独群 2例[1%]、トラスツズマブ+化学療法群 11例[5%])。
7. 投与状況
- トラスツズマブ投与サイクル数中央値:8サイクル(範囲:1-49)
- 化学療法の積算量、投与期間、用量強度に関しては、両群で差を認めなかった。
- 用量変更や休薬につながる有害事象を生じた症例:トラスツズマブ+化学療法群 246例(84%)、化学療法単独群 237例(82%)
- 60日以内の死亡:トラスツズマブ+化学療法群 15例(5%)、化学療法単独群 20例(7%)
- 治療関連死亡:トラスツズマブ+化学療法群 10例(3%)、化学療法単独群 3例(1%)
- 病勢進行後の治療は下表のように行われた。
| N (%) | トラスツズマブ+化学療法 | 化学療法単独 |
|---|---|---|
| 後治療あり 化学療法 放射線照射 手術 |
122 (42) 113 (38) 17 (6) 8 (3) |
131 (45) 124 (43) 17 (6) 13 (5) |
結語
本試験の結果より、化学療法へのトラスツズマブ併用は化学療法単独と比較して、HER2陽性進行胃・食道胃接合部癌症例の生存期間を改善した。有効性は主にHER2高発現症例にもたらされた。これらの結果に基づいて、トラスツズマブ+XP(カペシタビン+シスプラチン) or FP(5-FU+シスプラチン)はHER2陽性の進行胃・食道胃接合部癌に対する新しい治療オプションになると考えられる。
執筆:釧路ろうさい病院 腫瘍内科 部長 原田 一顕 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生