Ipilimumab or FOLFOX in combination with Nivolumab and Trastuzumab in previously untreated HER2 positive locally advanced or metastastic EsophagoGastric Adenocarcinoma (EGA) – results of the randomized phase 2 INTEGA trial (AIO STO 0217).
First Author : A. Stein, et al.
HER2陽性進行再発胃または食道胃接合部癌に対するFOLFOX/ニボルマブ/トラスツズマブまたはイピリムマブ/ニボルマブ/トラスツズマブのランダム化第2相試験 (INTEGA試験: AIO STO 0217)
背景
(発表時に口頭でもスライドでも背景について言及がございません。以下については抄録より転載しております。)
HER2陽性進行再発胃または食道胃接合部癌一次治療における免疫チェックポイント阻害薬併用療法
転移再発胃または食道胃接合部癌(Esophagogastric Adenocarcinoma: EGA)の一次治療に従来の化学療法に抗PD-1抗体薬を上乗せすることで一部の患者において予後を改善している。本INTEGA試験ではHER2陽性進行再発EGAの一次治療において異なった免疫療法レジメンを比較した。
対象と方法
12ヶ月全生存期間割合を主要評価項目として免疫チェックポイント併用療法を比較
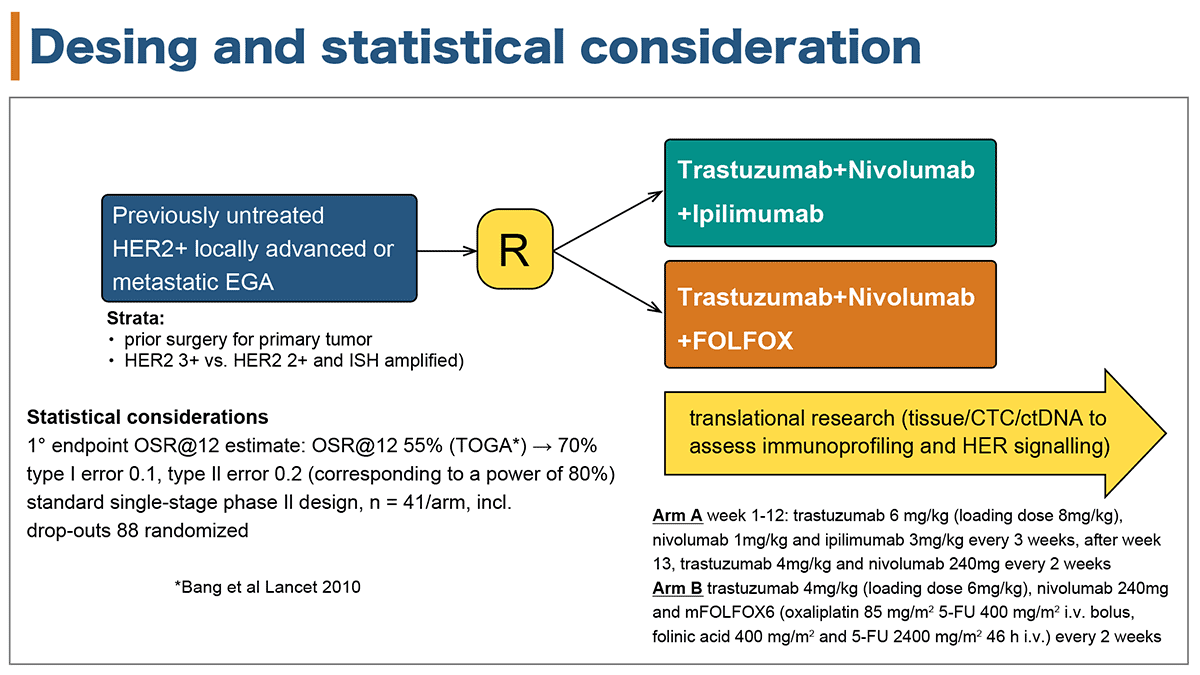
未治療のHER2陽性進行再発EGAを無作為化し、イピリムマブ(Ipi)/ニボルマブ(Nivo)/トラスツズマブ(Tmab)併用療法群(Arm A)とFOLFOX/Nivo/Tmab併用療法群(Arm B)に割り付けた。Arm Aでは12週までTmab: 6mg/kg (初回のみ8mg/kg)、Nivo: 1mg/kg、Ipi: 3mg/kgを3週毎に投与し、以降はTmab: 4mg/kg、Nivo: 240mgを2週毎に投与した。Arm BではTmab: 4mg/kg(初回のみ6mg/kg)、Nivo: 240mg、FOLFOX6(オキサリプラチン: 85mg/m2、レボホリナート 400mg/m2、急速静注5-FU: 400mg/m2、持続静注5-FU 2400mg/m2/46時間)を2週毎に投与した。
TR研究として腫瘍組織、循環腫瘍細胞(CTC)、循環腫瘍DNA(ctDNA)の免疫プロファイリング、HER2発現を評価する。
統計学的事項
図1 INTEGA試験デザイン