Exploratory biomarker analysis of trastuzumab deruxtecan in DESTINY-Gastric01, a randomized, phase 2, multicenter, open-label study in patients with HER2-positive or -low advanced gastric or gastroesophageal junction adenocarcinoma
First Author : Shitara K, et al.
HER2陽性もしくは低発現の進行胃癌および食道胃接合部癌に対する無作為化第2相多施設共同非盲検試験、DESTINY-Gastric01試験におけるトラスツズマブ デルクスカンの探索的バイオマーカー解析
背景
抗HER2療法はHER2陽性胃癌において確立されている。トラスツズマブ デルクスカン(T-DXd)はヒト化抗HER2モノクローナル抗体とリンカー、トポイソメラーゼI阻害剤で構成された抗体薬物複合体である。
DESTINY-Gastric01試験ではT-DXdはHER2陽性胃癌に対して有意な治療成績の向上を示しており、治療効果を予測する追加のバイオマーカーを探索することを目的に同試験の探索的バイオマーカー解析が行われた。
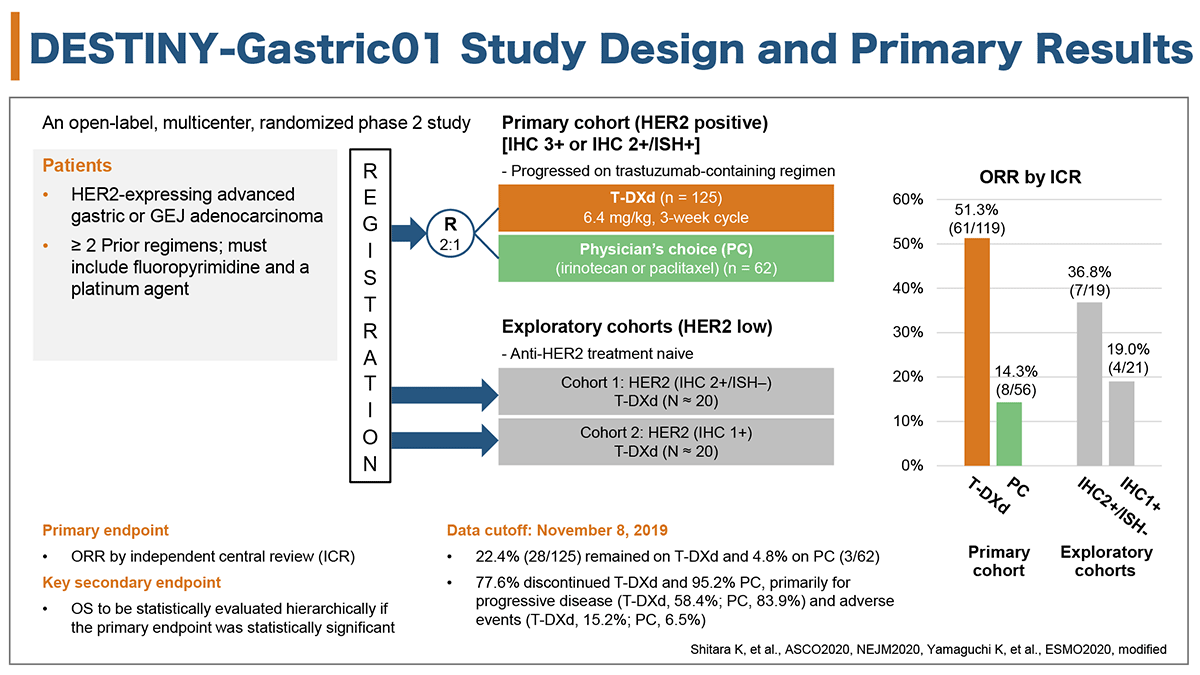
DESTINY-Gastric01試験は日本および韓国で行われたオープンラベル無作為化比較第2相試験である(図1)。
主要コホートにはHER2陽性[IHC 3+ もしくは IHC 2+/ISH+]で、フッ化ピリミジン製剤・白金製剤を含む2レジメン以上が投与され、トラスツズマブ併用レジメンに不応が確認された胃もしくは食道胃接合部癌が登録された。登録例は2:1の割付比でT-DXd群(6.4mg/kg, 3週毎)もしくは化学療法群(イリノテカンもしくはパクリタキセル群)へ割り付けされた。主要コホートの主要評価項目である独立中央判定による客観的奏効割合(ORR)はT-DXd群 51.3%(61/119)、化学療法群 14.3%(8/56)と有意にT-DXd群で良好だった。
探索的コホートには抗HER2療法歴のないHER2弱陽性[Cohort 1:IHC 2+ かつ ISH- (n=19)、Cohort 2:IHC 1+(n=21)]が登録され、T-DXdの投与を受けた。ORRはCohort 1 36.8%(7/19)、Cohort 2 19.0%(4/21)だった。
図1 DESTINY-Gastric01試験の試験デザインと主な結果