| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| KRAS 野生型 切除不能大腸癌 | 三次治療以降 | 第2相 | PFS | 日本 | あり |
試験名 :WJOG6510G
レジメン:パニツムマブ+イリノテカンvsセツキシマブ+イリノテカン
登録期間:2011年12月〜2014年9月
背景
セツキシマブ(CET)、パニツムマブ(PANI)はともに上皮成長因子受容体(EGFR)の細胞外ドメインに結合し、リガンドのEGFRへの結合を阻害することで、その下流のシグナルを抑制し、細胞の分化・増殖を妨げる抗EGFR抗体薬である。両薬剤ともに単剤とBest Supportive Care(BSC)の比較において、生存期間を延長することが報告されている1),2)。既治療のKRAS 野生型切除不能大腸癌に対するPANIとCETを比較する非盲検無作為化第3比較試験であるASPECCT試験において、両薬剤の有効性は同程度であったと報告されている3)。イリノテカン(IRI)に不応のKRAS 野生型切除不能大腸癌に対し、CET単独とCET+IRI併用療法を比較した第3相比較試験であるBOND試験では、IRI併用群で無増悪生存期間、奏効割合が有意に良好であった4)。PANI+IRIは単アームの第2相試験において、BOND試験と同じ対象に対する有効性を示している5)。
IRIとの併用において、PANIとCETを直接比較検討した試験はないことから、本試験ではフッ化ピリミジン、IRI、オキサリプラチンのいずれの薬剤にも不応、または不耐となったKRAS 野生型切除不能大腸癌患者に対し、PANI+IRI併用療法とCET+IRI併用療法を直接比較検討した。
IRIとの併用において、PANIとCETを直接比較検討した試験はないことから、本試験ではフッ化ピリミジン、IRI、オキサリプラチンのいずれの薬剤にも不応、または不耐となったKRAS 野生型切除不能大腸癌患者に対し、PANI+IRI併用療法とCET+IRI併用療法を直接比較検討した。
シェーマ
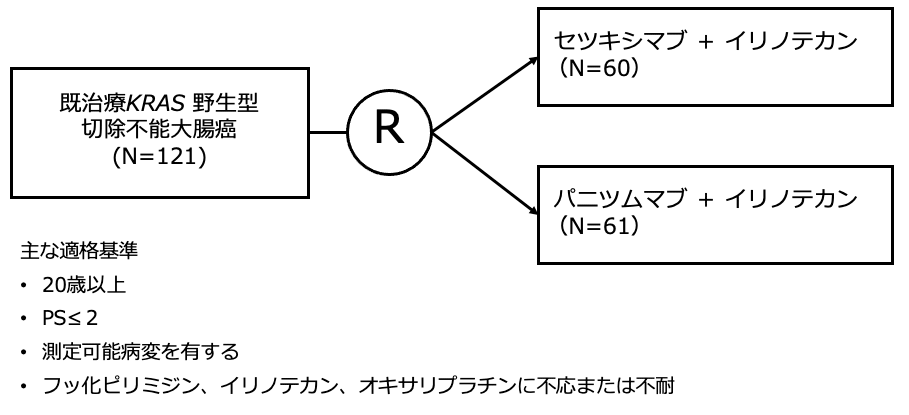
統計学的事項
主要評価項目:full analysis setにおける無増悪生存期間(PFS)
Full analysis set: ランダム化された全登録例からランダム化後に不適格例を除いた集団。
副次的評価項目:全生存期間(OS)、奏効割合(RR)、病勢制御割合(DCR)、安全性
既報から両群のPFSを6.0ヶ月と想定し、片側α:0.2、検出力:0.7とした非劣性マージンのハザード比1.30と設定した場合、サンプルサイズは120例が必要とされた。試験結果:
- データカットオフは2015年12月。
原発巣占居部位、原発巣の切除歴など患者背景に大きな偏りはなく、ベバシズマブ使用歴はPANI併用群:96.7%、CET併用群:96.6%であった。 - 主要評価項目であるPFSはPANI併用群:5.42ヶ月、CET併用群:4.27ヶ月でハザード比は0.64、非劣性の検定ではp<0.001であり、両群の非劣性が示された。事前に設定されていた探索的解析である優越性の検定ではp=0.058とPANI群が良好な傾向を示したが統計学的な有意差は認められなかった。
- OSはPANI併用群:14.85ヶ月、CET併用群:11.53ヶ月、ハザード比:0.66、非劣性の検定ではp<0.001、優越性の検定ではp=0.05でありPFS同様の傾向を示した。
- 奏効割合はPANI併用群:22%、CET併用群:26%、p=0.67であった。
- PFS、OSそれぞれのサブグループ解析では、総じてPANI併用群で良好な傾向を示した。
- 後治療はPANI併用群:48例(79%)、CET併用群:41例(70例)で行われた。レゴラフェニブはPANI併用群:18例(30%)、CET併用群:11例(18%)、トリフルリジンチピラシル塩酸塩はPANI併用群:15例(25%)、CET併用群:7例(12%)で投与された。
1. 無増悪生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.64(0.44-0.94) (非劣性)p<0.001 (優越性)p=0.058 |
|
| PANI+IRI群 | 5.42ヶ月 | 4.14-6.90 | |
| CET+IRI群 | 4.27ヶ月 | 3.48-5.39 |
2. 全生存期間
| 中央値 | 95%信頼区間 | HR 0.66(0.44-1.00) (非劣性)p<0.001 (優越性)p=0.050 |
|
| PANI+IRI群 | 14.85ヶ月 | 12.81-17.54 | |
| CET+IRI群 | 11.53ヶ月 | 10.5-14.13 |
3. 奏効割合
| 中央値 | P=0.67 | |
| PANI+IRI群 | 22% | |
| CET+IRI群 | 26% |
4. 有害事象
| PANI+IRI群 (N=60) | CET+IRI群 (N=58) | |||||||
|---|---|---|---|---|---|---|---|---|
| Any Grade | Grade ≥ 3 | Any Grade | Grade ≥ 3 | |||||
| N | % | N | % | N | % | N | % | |
| 白血球減少 | 27 | 45.0 | 2 | 3.3 | 37 | 63.8 | 11 | 19.0 |
| 好中球減少 | 29 | 48.3 | 5 | 8.3 | 38 | 65.5 | 16 | 27.6 |
| 貧血 | 4 | 6.7 | 1 | 1.7 | 1 | 1.7 | 0 | 0 |
| 血小板減少 | 15 | 25.0 | 4 | 6.7 | 24 | 41.4 | 6 | 10.3 |
| 発熱性好中球減少症 | 1 | 1.7 | 1 | 1.7 | 1 | 1.7 | 1 | 1.7 |
| 低マグネシウム血症 | 49 | 81.7 | 10 | 16.7 | 39 | 67.2 | 4 | 6.9 |
| 低カルシウム血症 | 17 | 28.3 | 2 | 3.3 | 8 | 13.8 | 0 | 0 |
| 注入反応 | 1 | 1.7 | 0 | 0 | 0 | 0 | 0 | 0 |
| 食欲不振 | 30 | 50.0 | 5 | 8.3 | 35 | 60.3 | 4 | 6.9 |
| 口内炎 | 30 | 50.0 | 2 | 3.3 | 22 | 37.9 | 3 | 5.2 |
| 悪心 | 26 | 43.3 | 0 | 0 | 24 | 41.4 | 3 | 5.2 |
| 嘔吐 | 9 | 15.0 | 0 | 0 | 16 | 27.6 | 1 | 1.7 |
| 疲労 | 24 | 40.0 | 2 | 3.3 | 37 | 63.8 | 3 | 5.2 |
| 肺炎 | 1 | 1.7 | 0 | 0 | 0 | 0 | 0 | 0 |
| 感染症 | 4 | 6.7 | 2 | 3.3 | 7 | 12.1 | 3 | 5.2 |
| 下痢 | 32 | 53.3 | 2 | 3.3 | 28 | 48.3 | 5 | 8.6 |
| 皮疹 | 52 | 86.7 | 8 | 13.3 | 51 | 87.9 | 3 | 5.2 |
| 皮膚乾燥 | 41 | 68.3 | 4 | 6.7 | 40 | 69.0 | 2 | 3.4 |
| 爪囲炎 | 36 | 60.0 | 5 | 8.3 | 39 | 67.2 | 8 | 13.8 |
| 他の皮膚毒性 | 12 | 20.0 | 1 | 1.7 | 12 | 20.7 | 1 | 1.7 |
| 死亡 | 0 | 0 | 0 | 0 | 1 | 1.7 | 1 | 1.7 |
結語
フッ化ピリミジン、IRI、オキサリプラチンに不応または不耐となったKRAS エクソン2野生型切除不能大腸癌において、PANI+IRI併用療法のCET+IRI併用療法に対する無増悪生存期間における非劣性が示唆され、PANI+IRI併用療法で無増悪生存期間、全生存期間が良好な傾向にあった。ほとんど全ての患者でベバシズマブの前治療歴があったことから、特にベバシズマブ前治療歴のある患者において、PANI+IRI併用療法はCET+IRI併用療法の代替治療となり得ることが示唆された。
関連論文
1) Jonker DJ, et al. Cetuximab for the treatment of colorectal cancer. N Engl J Med 2007;357:2040-8. [Pubmed]
2) Van Cutsem E, at al. Open-label phase III trial of panitumumab plus best supportive care compared with best supportive care alone in patients with chemotherapy-refractory metastatic colorectal cancer. J Clin Oncol 2007;25-1658-64. [Pubmed]
3) Price TJ, et al. Panitumumab versus cetuximab in patients with chemotherapy-refractory wild-type KRAS exon 2 metastatic colorectal cancer (ASPECCT): a randomised, multicentre, open-label, non-inferiority phase 3 study. Lancet Oncol 2014;15:569-79. [Pubmed]
4) Cunningham D, et al. Cetuximab monotherapy and cetuximab plus irinotecan in irinotecan-refractory metastatic colorectal cancer. N Engl J Med 2004;351:337-45. [Pubmed]
5) Andre T, et al. Panitumumab combined with irinotecan for patients with KRAS wild-type metastatic colorectal cancer refractory to standard chemotherapy: a GERCOR efficacy, tolerance, and translational molecular study. Ann Oncol 2013;24:412-9. [Pubmed]
執筆:香川大学医学部附属病院 腫瘍内科 学内講師 大北 仁裕 先生
監修:愛知県がんセンター病院 薬物療法部 医長 舛石 俊樹 先生
監修:愛知県がんセンター病院 薬物療法部 医長 舛石 俊樹 先生