| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 大腸癌 | 二次治療 | 第3相 | 全生存期間 | 日本・中国・韓国 | あり |
試験名 :AXEPT
レジメン:FOLFIRI±Bevacizumab vs mXELIRI±Bevacizumab
登録期間:2013年12月〜2015年8月
背景
切除不能大腸癌の一次治療においてカペシタビン+オキサリプラチン(XELOX)はFOLFOXと同等の有効性と安全性が示されている。しかしBICC-C試験では、カペシタビン(1000mg/㎡ day1-14)+イリノテカン(250mg/㎡ day1) 3週ごと (XELIRI)は、消化器毒性による治療中止のため無増悪生存期間においてFOLFIRIに劣っていた。そこで両薬剤を減量したmXELIRIはBevacizumab(Bev)との併用で、AIO 0604試験、BIX試験において有効性・安全性が確認された。そのためこれらの試験をもとにmXELIRI±BevのFOLFIRI±Bevに対する有用性を検証するための第3相試験(AXEPT試験)が実施された。
シェーマ
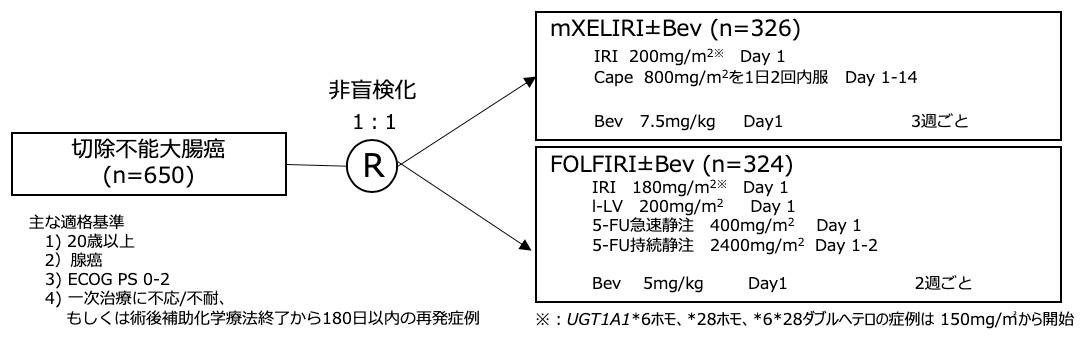
統計学的事項
主要評価項目:全生存期間
本試験はFOLFIRI±Bev群を対照としてmXELIRI±Bev群のOSハザード比の上限が1.30(12.6ヶ月 vs 9.7ヶ月)以下となることを検証する非劣性試験として設計され、検出力80%、片側α=0.025として、464イベント、600例が必要とされた。また上記を満たした場合には、ハザード比の上限を1.25以下とした非劣性、および優越性も検証する設定であった。試験結果:
- 2013年12月から2015年8月までに98施設(日本73、韓国8、中国17)から650例が登録され、mXELIRI±Bev群に326例が、FOLFIRI±Bev群に324例が割付られた(ITT)。そのうちのmXELIRI±Bev群 16例、FOLFIRI±Bev群 14例がプロトコール治療が実施されず、両群ともにper-protocol解析および安全性解析対象集団は310例であった。
- 患者背景に大きな偏りは認められなかった。
- 2017年7月28日のカットオフまでの観察期間中央値は15.8ヶ月であった。
- ベバシズマブを併用したのはmXELIRI±Bev群で269例(83%)、FOLFIRI±Bev群で272例(84%)であった。
- 後治療を受けたのはmXELIRI±Bev群で195例(60%)、FOLFIRI±Bev群で189例(58%)であった。
1. 全生存期間(主要評価項目)
| 中央値 | 95%信頼区間 | HR 0.85(95%C.I. 0.71-1.02) p< 0.0001(非劣性) p=0.088 (優越性) |
|
| mXELIRI±Bev(n=326) | 16.8ヶ月 | 15.3-19.1 | |
| FOLFIRI±Bev(n=324) | 15.4ヶ月 | 13.0-17.7 |
2. 無増悪生存期間
| 中央値 | 95%信頼区間 | HR 0.95 (95%C.I. 0.81-1.11) p=0.51 |
|
| mXELIRI±Bev(n=326) | 8.4ヶ月 | 7.1-9.1 | |
| FOLFIRI±Bev(n=324) | 7.2ヶ月 | 6.6-8.5 |
3. 奏効割合
| 奏効割合 | 95%信頼区間 | |
|---|---|---|
| mXELIRI±Bev(n=310) | 24.2%(CR 13例、PR 62例) | 19.5-29.4 |
| FOLFIRI±Bev(n=310) | 18.4%(CR 2例、PR 55例) | 14.2-23.2 |
4. 有害事象(NCI-CTCAE ver.4.0)
| mXELIRI±Bev(n=310) | FOLFIRI±Bev(n=310) | |||||
|---|---|---|---|---|---|---|
| Grade 1-2 | Grade 3 | Grade 4 | Grade 1-2 | Grade 3 | Grade 4 | |
| 好中球減少症 | 120 (39%) | 46 (15%) | 6 (2%) | 103 (33%) | 84 (27%) | 49 (16%) |
| 貧血 | 207 (67%) | 8 (3%) | 2 (1%) | 236 (76%) | 12 (4%) | 1 (<1%) |
| 血小板減少症 | 105 (34%) | 3 (1%) | 1 (<1%) | 104 (34%) | 1 (<1%) | 0 |
| 発熱性好中球減少症 | 0 | 6 (2%) | 4 (1%) | 0 | 8 (3%) | 5 (2%) |
| 悪心 | 148 (48%) | 13 (4%) | 0 | 156 (50%) | 9 (3%) | 0 |
| 下痢 | 133 (43%) | 22 (7%) | 0 | 122 (39%) | 10 (3%) | 0 |
| 手足症候群 | 100 (32%) | 6 (2%) | 0 | 46 (15%) | 1 (<1%) | 0 |
| 高血圧 | 50 (19%) | 19 (7%) | 0 | 32 (12%) | 27 (10%) | 0 |
| 蛋白尿 | 97 (36%) | 16 (6%) | 0 | 81 (30%) | 26 (10%) | 0 |
| 出血 | 37 (14%) | 2 (1%) | 0 | 37 (14%) | 1 (<1%) | 0 |
| 血栓塞栓症 | 5 (2%) | 2 (1%) | 1 (<1%) | 2 (1%) | 4 (1%) | 0 |
結語
切除不能大腸癌の二次治療において、全生存期間におけるmXELIRI±BevacizumabのFOLFIRI±Bevacizumabに対する非劣性が証明された。mXELIRIは認容性も良好であり、少なくともアジア人患者に対してはFOLFIRIの代替療法となり得る。
執筆:静岡県立静岡がんセンター 消化器内科 レジデント 井上 博登 先生
監修:静岡県立静岡がんセンター 治験管理室 部長、消化器内科 医長 山﨑 健太郎 先生
監修:静岡県立静岡がんセンター 治験管理室 部長、消化器内科 医長 山﨑 健太郎 先生