| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 局所進行食道癌 (cStage I-IVA) (腺癌/腺扁平上皮癌/扁平上皮癌) |
一次治療 | 第2/3相 | 無増悪生存期間 | フランス | なし |
試験名 :PRODIGE5/ACCORD17
レジメン:FOLFOX+放射線療法 vs 5-FU+シスプラチン+放射線療法
登録期間:2004年10月15日〜2011年8月25日
背景
RTOG 85-01試験において、局所進行食道癌に対して放射線単独療法に対する5-FU+シスプラチン(CDDP)併用の根治的化学放射線療法の生存期間延長が示され、その後の試験でこの根治的化学放射線療法の有効性と安全性が確立され、手術不適の食道癌患者に対する標準治療として確立した。しかし、RTOG 85-01試験では5-FU+CDDP併用の根治的化学放射線療法では46%に局所増悪を、20%に重篤な有害事象を認め、41%の患者では計画通りの化学放射線療法ができなかった。
治療の進歩にも関わらず、食道癌患者の予後は依然として不良であり、より効果的な治療計画が必要である。さらにCDDPは大量補液を要するため、より簡便で安全な予後延長につながる治療開発が必要である。食道癌患者に対する小規模な研究では5-FUに対するロイコボリン(LV)の併用が5-FUの活性を修飾し、その併用により治療効果の上昇が期待される結果が得られた。基礎的検討を含めた過去の報告では、オキサリプラチン(OX)はCDDP耐性を克服する放射線増感作用を有する事がしめされ、また、CDDPよりも催吐性が低く、大量補液を要さず、腎毒性もない。
OX+5-FU+LVの併用(FOLFOX)は、いくつかの第1・2相試験において転移性/局所進行食道癌に対してFOLFOX単独、もしくは放射線療法との併用で有望な治療成績を示した。著者らは第1相試験1)において、放射線療法併用時のFOLFOXの最大耐容量を決定し、引き続き、手術不適の食道癌症例を対象としてFOLFOX+放射線療法と5-FU+CDDP+放射線療法(標準的RTOGレジメン)の有効性と安全性を比較する無作為化比較第2/3相試験を実施した。既に第2相部分2)の結果は報告されているが、本論文では第3相部分の有効性と安全性を報告した。
治療の進歩にも関わらず、食道癌患者の予後は依然として不良であり、より効果的な治療計画が必要である。さらにCDDPは大量補液を要するため、より簡便で安全な予後延長につながる治療開発が必要である。食道癌患者に対する小規模な研究では5-FUに対するロイコボリン(LV)の併用が5-FUの活性を修飾し、その併用により治療効果の上昇が期待される結果が得られた。基礎的検討を含めた過去の報告では、オキサリプラチン(OX)はCDDP耐性を克服する放射線増感作用を有する事がしめされ、また、CDDPよりも催吐性が低く、大量補液を要さず、腎毒性もない。
OX+5-FU+LVの併用(FOLFOX)は、いくつかの第1・2相試験において転移性/局所進行食道癌に対してFOLFOX単独、もしくは放射線療法との併用で有望な治療成績を示した。著者らは第1相試験1)において、放射線療法併用時のFOLFOXの最大耐容量を決定し、引き続き、手術不適の食道癌症例を対象としてFOLFOX+放射線療法と5-FU+CDDP+放射線療法(標準的RTOGレジメン)の有効性と安全性を比較する無作為化比較第2/3相試験を実施した。既に第2相部分2)の結果は報告されているが、本論文では第3相部分の有効性と安全性を報告した。
シェーマ
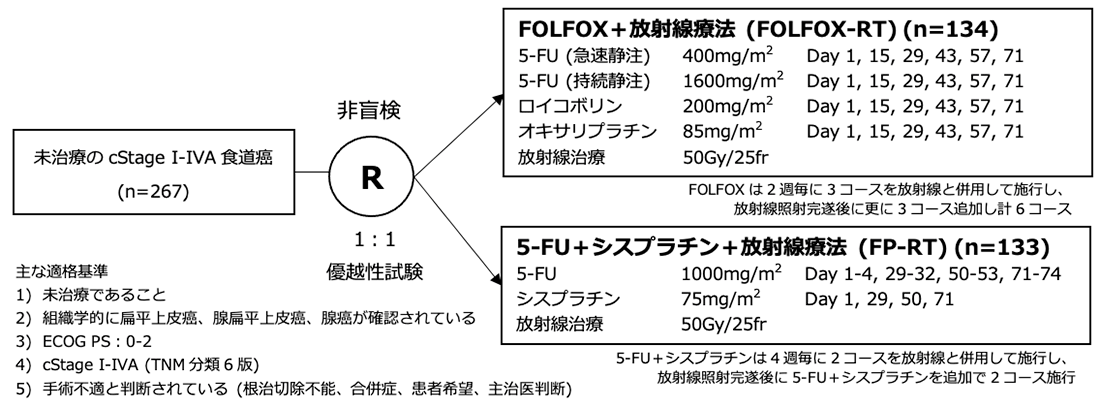
統計学的事項
主要評価項目:無増悪生存期間
第2相パートの結果を元に、FP-RT群/FOLFOX+RT群の3年無増悪生存割合をそれぞれ30%/50%と仮定し、検出力を90%、両側α=0.05、登録期間 48ヶ月(第2相パート 28ヶ月、第3相パート 20ヶ月)、追跡期間 12ヶ月で設定したところ、266例の症例が必要と設定された。72の増悪イベントが観察された時点で、中間解析を計画した。試験結果:
- 2004年10月15日から2011年8月25日までの間に、フランス国内24施設より267例が登録され、FP-RT群に134例、FOLFOX+RT群に133例が割り付けられた(ITT解析集団)。
- FP-RT群の3例(遠隔転移の発覚 n=3)、FOLFOX-RT群の5例(遠隔転移の発覚 n=3、臨床検査値異常 n=1、心筋梗塞の既往 n=1)は試験治療を受けず、安全性解析集団はFP-RT群 128例、FOLFOX-RT群 131例となった。
- 追跡期間中央値はコホート全体で25.3ヶ月(四分位範囲 15.9-36.4)、FOLFOX-RT群で25.5ヶ月(四分位範囲 15.8-35.0)、FP-RT群で25.1ヶ月(四分位範囲 16.1-36.5)であった。
- 各群1例の計2例において、経過観察期間が非常に短かかったが(FOLFOX-RT群 0.1ヶ月、FP-RT群 0.3ヶ月)、ITT解析集団に含まれた。
1. 患者背景
| N (%) | FOLFOX-RT群 (N=134) | FP-RT群 (N=133) | |
|---|---|---|---|
| 年齢 | 中央値 (四分位範囲) | 61 (39-85) | 60 (41-81) |
| 性別 | 男性 女性 |
110 (82) 24 (18) |
107 (80) 26 (20) |
| BMI (kg/m2) | 中央値 (四分位範囲) | 24 (21-27) | 23 (21-27) |
| 3ヶ月以内に10%以上の体重減少 | あり | 32 (24) | 37 (28) |
| ECOG PS | 0 1 2 不明 |
71 (53) 62 (47) 0 1 |
68 (51) 62 (47) 3 (2) 0 |
| 組織診断 | 扁平上皮癌 腺癌 腺扁平上皮癌 |
114 (85) 19 (14) 1 (1) |
115 (86) 18 (14) 0 |
| 分化度 | 低分化 中分化 高分化 不明 |
27 (20) 35 (26) 57 (43) 15 (11) |
18 (14) 48 (36) 50 (38) 17 (13) |
| 診断時の病期 | I IIA IIB III IVA IVB 不明 |
0 31 (26) 10 (8) 67 (56) 8 (7) 5 (3) 14 |
1 (1) 31 (25) 7 (6) 72 (59) 8 (7) 4 (3) 10 |
| 手術不適の理由 | 局所の広がり 手術禁忌 患者拒否 主治医判断 不明 |
75 (61) 15 (12) 1 (1) 31 (25) 12 |
67 (56) 23 (19) 2 (2) 28 (23) 13 |
| 腫瘍径 (mm) | 中央値 (四分位範囲) | 58 (40-72) | 60 (40-70) |
| 原発部位 | 頚部 胸部上部 胸部中部 胸部下部 |
8 (6) 35 (26) 54 (40) 37 (28) |
4 (3) 40 (30) 59 (44) 30 (23) |
- 患者背景は両群間でバランスが取れていた。
2. 放射線照射/薬剤投与状況
- 放射線照射:治療を完全に中止した各群2例(FOLFOX-RT群:死亡[自殺] 1例、重篤な有害事象[食道炎] 1例、FP-RT群:化学療法開始前の突然死 n=1、プロトコールからの離脱 n=1)を除いて、全ての症例が予定の90%以上の放射線照射を達成した。
- 相対用量強度が80%以上の症例:FOLFOX-RT群:5-FU 70%(92/131)/OX 75%(98/127)、FP-RT群:5-FU 69%(87/127)、CDDP 71%(90/126)
- 化学療法延期:FOLFOX-RT群:15%(104/701サイクル)、FP-RT群 16%(73/454サイクル), p=0.56
- 有害事象による減量:FOLFOX-RT群:34%(45/131)、FP-RT群 27%(34/127), p=0.19
- 化学放射線療法はFP-RT群の97%(124/128)、FOLFOX-RTの93%(122/131)で計画通りに実施された。
- 全ての化学療法の完了はFP-RT群の76%(97/128)、FOLFOX-RTの71%(93/131)で達成された。
3. 無増悪生存期間(主要評価項目)
| N | 中央値 | 95%信頼区間 | 3年無増悪生存割合 | 95%信頼区間 | |
|---|---|---|---|---|---|
| FOLFOX+RT群 | 134 | 9.7ヶ月 | 8.1-14.5 | 18.2% | 10.6-27.4 |
| FP-RT群 | 133 | 9.4ヶ月 | 8.1-10.6 | 17.4% | 9.9-26.8 |
HR 0.93 (95%信頼区間 0.70-1.24), p=0.64
- 無増悪生存期間に関して、患者背景による効果予測因子の探索的な解析が実施されたが、有意差を示す因子はなかった。
4. 治療成功期間
| N | 中央値 | 95%信頼区間 | |
|---|---|---|---|
| FOLFOX+RT群 | 134 | 8.0ヶ月 | 6.0-9.5 |
| FP-RT群 | 133 | 8.3ヶ月 | 6.6-9.8 |
HR 1.0 (95%信頼区間 0.8-1.3), p=0.98
5. 全生存期間 (全症例)
| N | 中央値 | 95%信頼区間 | 3年生存割合 | 95%信頼区間 | |
|---|---|---|---|---|---|
| FOLFOX+RT群 | 134 | 20.2ヶ月 | 14.7-25.6 | 19.9% | 10.8-31.0 |
| FP-RT群 | 133 | 17.5ヶ月 | 13.9-19.4 | 26.9% | 16.9-37.8 |
HR 0.94 (95%信頼区間 0.68-1.29), p=0.70
- 全生存期間に関して、患者背景による効果予測因子の探索的な解析が実施されたが、有意差を示す因子はなかった。
6. 全生存期間 (遠隔転移例を除いた症例)
| N | 中央値 | 95%信頼区間 | |
|---|---|---|---|
| FOLFOX+RT群 | 129 | 23.5ヶ月 | 14.3-27.4 |
| FP-RT群 | 129 | 17.4ヶ月 | 13.1-19.4 |
7. 奏効割合/内視鏡的完全奏効割合
| N (%, 95%信頼区間) | FOLFOX+RT 群(n=134) | FP+RT 群(n=133) |
|---|---|---|
| 奏効割合 (RECIST) CR PR SD PD NE 未評価 不明 |
86 (67%, 58-75) 57 (44%, 35-53) 29 (22%, 16-31) 14 (11%, 6-18) 11 (9%, 4-15) 6 (5%, 2-10) 12 (9%, 5-16) 5 |
83 (65%, 56-74) 55 (43%, 34-52) 28 (22%, 15-30) 10 (8%, 4-14) 12 (9%, 5-16) 7 (6%, 2-11) 15 (12%, 7-19) 6 |
8. 奏効割合/内視鏡的完全奏効割合
| N (%, 95%信頼区間) | FOLFOX+RT群 (n=115) | FP+RT 群(n=120) |
|---|---|---|
| 内視鏡的奏効 (主治医判定) 完全奏効 非完全奏効 評価不能 未評価 不明 |
61 (53%, 44-62) 45 (39%, 30-49) 2 (2%, 0-6) 7 (6%, 2-12) 19 |
57 (48%, 38-57) 46 (38%, 30-48) 4 (3%, 1-8) 13 (11%, 6-18) 13 |
9. 有害事象 (CTCAE v3.0)
| N (%) | FOLFOX-RT群 (n=131) | FP-RT群 (n=128) | ||||
|---|---|---|---|---|---|---|
| Grade 1-2 | Grade 3 | Grade 4 | Grade 1-2 | Grade 3 | Grade 4 | |
| 血液毒性 好中球数減少 発熱性好中球減少症 感染を伴う好中球減少症 リンパ球減少症 白血球減少 貧血 血小板数減少 低ナトリウム血症 高カリウム血症 低カリウム血症 |
30 (23) 0 (0) 1 (1) 4 (3) 38 (29) 68 (52) 52 (40) 14 (11) 11 (8) 14 (11) |
29 (22) 5 (4) 2 (2) 14 (11) 25 (19) 6 (5) 6 (5) 3 (2) 1 (1) 0 (0) |
9 (7) 2 (2) 0 (0) 7 (5) 3 (2) 1 (1) 3 (2) 0 (0) 0 (0) 0 (0) |
32 (25) 1 (1) 0 (0) 4 (3) 41 (32) 69 (54) 53 (41) 22 (17) 20 (16) 13 (10) |
26 (20) 6 (5) 1 (1) 11 (9) 20 (16) 12 (9) 2 (2) 5 (4) 1 (1) 1 (1) |
11 (9) 3 (2) 2 (2) 11 (9) 11 (9) 2 (2) 8 (6) 0 (0) 0 (0) 0 (0) |
| 非血液毒性 嚥下不能/嚥下障害 無力症 食道炎 紅斑/皮膚炎 体重減少 食欲不振 粘膜炎 嘔吐 悪心 嚥下痛 栄養障害 心疾患 下痢 便秘 胸骨後面痛 食道痛/心窩部痛 知覚異常 敗血症 血栓症 腎不全 |
16 (12) 47 (36) 19 (15) 9 (7) 42 (32) 25 (19) 20 (15) 28 (21) 62 (47) 17 (13) 0 (0) 1 (1) 18 (14) 16 (12) 5 (4) 16 (12) 61 (47) 1 (1) 6 (5) 1 (1) |
32 (24) 23 (18) 8 (6) 0 (0) 5 (4) 6 (5) 6 (5) 4 (3) 3 (2) 2 (2) 2 (2) 1 (1) 2 (2) 0 (0) 0 (0) 4 (3) 0 (0) 1 (1) 0 (0) 0 (0) |
6 (5) 0 (0) 1 (1) 1 (1) 0 (0) 0 (0) 1 (1) 1 (1) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) |
12 (9) 47 (37) 18 (14) 17 (13) 40 (31) 19 (15) 30 (23) 39 (31) 74 (58) 8 (6) 0 (0) 0 (0) 18 (14) 15 (12) 2 (2) 13 (10) 2 (2) 0 (0) 2 (2) 4 (3) |
31 (24) 12 (9) 11 (9) 1 (1) 5 (4) 4 (3) 2 (2) 3 (2) 4 (3) 3 (2) 2 (2) 1 (1) 1 (1) 0 (0) 3 (2) 2 (2) 1 (1) 0 (0) 2 (2) 1 (1) |
0 (0) 1 (1) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 1(1) 0 (0) 0 (0) 0 (0) 0 (0) 0 (0) 2 (2) 0 (0) 1 (1) |
- 両群間で高頻度に発症したGrade 3-4の有害事象として、好中球数減少、白血球減少、嚥下障害、無力症の発生に有意差は認めなかった。
- 5%以上の症例に発症した全Gradeの有害事象の内、知覚異常(FOLFOX-RT 47%(61/131) vs FP-RT 2%(3/128), p<0.0001)、感覚神経障害(18%(24/131) vs 1%(1/128), p<0.0001)、AST増加(11%(14/131) vs 2%(2/128), p=0.002)、ALT増加(8%(11/131) vs 2%(2/128), p=0.012)はFOLFOX-RT群で有意に高率であったが、クレアチニン増加(3%(4/131) vs 12%(15/128), p=0.007)、粘膜炎(27%(35/131) vs 32%(41/128), p=0.011)、脱毛症(2%(2/131) vs 9%(12/128), p=0.005)はFP-RT群で有意に高率であった。
- Grade 3の末梢運動神経障害の1例はFP-RT群で発生した。
10. 試験治療中止理由
| N (%) | FOLFOX+RT群 (n=94) | FP+RT群 (n=93) |
|---|---|---|
| 原発巣の増悪 | 24 (26) | 23 (25) |
| リンパ節増大 | 12 (13) | 16 (17) |
| 遠隔転移の出現 | 30 (32) | 25 (27) |
| 病勢進行 (詳細不明) | 3 (3) | 4 (4) |
| 有害事象による死亡 | 1 (1) | 6 (6) |
| 突然死 | 2 (2) | 3 (3) |
| 他疾患による死亡 | 12 (13) | 8 (9) |
| 二次性食道癌の出現 | 2 (2) | 1 (1) |
| 二次癌の出現 | 8 (9) | 7 (8) |
- 治療関連死亡:FOLFOX-RT群 1例(病勢進行に関連する肺炎/栄養障害)、FP-RT群 6例(好中球減少性敗血症 5例、虚血性心疾患 1例)、p=0.066
- 5例が突然死した(FOLFOX-RT群 2例、FP-RT 3例)。致命的な虚血性心疾患または脳血管障害が原因の可能性があり(剖検は行われなかった)、治療薬の最終投与後30日以内に発生した。
結語
FOLFOX-RTは、FP-RTと比較して無増悪生存期間を延長することはできなかったが、FOLFOXレジメンは数日で完結する外来で可能な治療で、FP-RTよりも投与が簡便である可能性があるため、FOLFOX-RTは、局所進行食道癌患者におけるFP-RTの代替として使用される可能性がある。
References
1) Conroy T, et al. Br J Cancer. 2008 Nov 4;99(9):1395-401.
2) Conroy T, et al. Br J Cancer. 2010 Oct 26;103(9):1349-55.
執筆:愛知県がんセンター病院 薬物療法部 レジデント 松原 裕樹 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生
監修:北海道大学病院 消化器内科 助教 結城 敏志 先生