| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 切除不能大腸癌 | 一次治療 | 第2相 | 奏効割合(中央判定) | 日本 | あり |
試験名 :JACCRO CC-11
レジメン:modified-FOLFOXIRI+ベバシズマブ(BEV)併用療法
登録期間:2014年10月〜2016年8月
背景
- 複数のランダム化試験(TRIBE試験、STEAM試験、CHARTA試験)において、二剤併用療法に比較して三剤併用療法は、高い有効性が示されている。ESMOコンセンサスガイドラインにおいても、腫瘍縮小を要するRAS/BRAF 変異型切除不能大腸癌患者に対して三剤併用療法を行うことを推奨している。しかしランダム化試験の探索的なサブ解析ではRAS変異例に対する有効性は一貫してない。
- 国内ではTRIBE試験と同じ用量のFOLFOXIRI+BEV療法による第2相試験(QUATTRO試験)行われ、Grade 3以上の好中球減少が72.5%、Grade 3の発熱性好中球減少症が21.7%と骨髄毒性を強く認めることが報告されている。一方、国内第1相試験において、modified-FOLFOXIRI療法は抗腫瘍効果を損なうことなく、忍容可能であることが報告されているが、日本人に対する三剤併用療法の至適用量は不明である。
シェーマ
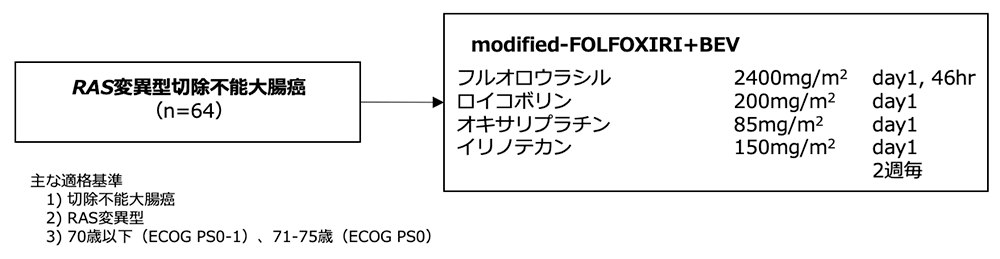
統計学的事項
主要評価項目:奏効割合
TRIBE試験とGONO試験におけるFOLFOXIRI+BEV併用療法の奏効割合:65-77%より、期待奏効割合を70%、閾値奏効割合を40%とし、αエラー0.05、βエラー0.10とし、不適格例を加味して60例の登録が必要と設定された。95%信頼区間の下限値が40%を超えた場合、治療が有望であると判断することとした。試験結果:
- 2014年10月から2016年8月までに国内の28施設から、計64例が本試験に登録された。2例が適格性を満たさなかったためFull analysis setには62例が組み込まれ、1例は不適格症例であったが試験治療を実施したためSafety populationには63例が組み込まれた。
- 年齢中央値は62.5歳(範囲:36-75歳)、右側原発は27%、ECOG PS0は92%であった。
- 導入化学療法投与サイクル中央値は12サイクル(範囲:1-17)であった。
- 66%が主に好中球数減少による毒性のために2サイクル目の投与延期を要し、30%で2週間以上の投与延期を要した。
- 39%において、2サイクル目のイリノテカン、オキサリプラチンもしくは両薬剤の減量を要した。
- 主要評価項目である中央判定による奏効割合は75.8% (95% CI, 65.1-86.5)、病勢制御割合は96.8% (95% CI, 92.4-100)であった。
- 原発占居部位別の奏効割合は左側 vs. 右側=82.2% vs 58.8%であった。
- 早期腫瘍縮小(ETS)を73.8%の症例で認め、最大腫瘍縮小は中央値22週で得られ、最大腫瘍縮小率(DpR)は49.2%であった。
- 解析時点において、無増悪生存期間(PFS)中央値は11.5ヶ月(95% CI, 9.5-14.0)、生存期間(OS)中央値は未達であり、18%において遠隔転移巣に対する外科的切除がなされた。
1. 奏効割合(主要評価項目)
奏効割合95%信頼区間
| 75.8% | 65.1-86.5% |
2. 無増悪生存期間
中央値95%信頼区間
| 11.5ヶ月 | 9.5-14.0ヶ月 |
3. 有害事象
| (N=63) | |||||
|---|---|---|---|---|---|
| Grade 1 | Grade 2 | Grade 3 | Grade 4 | ≥Grade 3 | |
| 白血球数減少 | 11 | 35 | 24 | 5 | 29 |
| 好中球数減少 | 3 | 27 | 25 | 29 | 54 |
| 貧血 | 24 | 21 | 6 | 0 | 6 |
| 血小板数減少 | 32 | 3 | 0 | 2 | 2 |
| 悪心 | 44 | 22 | 8 | 0 | 8 |
| 口腔粘膜炎 | 38 | 11 | 3 | 0 | 3 |
| 下痢 | 41 | 19 | 13 | 0 | 13 |
| 倦怠感 | 35 | 10 | 3 | 0 | 3 |
| 爪囲炎 | 2 | 0 | 0 | ||
| AST上昇 | 37 | 5 | 0 | 0 | 0 |
| ALT上昇 | 41 | 8 | 0 | 0 | 0 |
| 低ナトリウム血症 | 29 | 0 | 3 | 0 | 3 |
| 低カリウム血症 | 10 | 0 | 5 | 2 | 6 |
| タンパク尿 | 32 | 14 | 3 | 3 | |
| 末梢性感覚ニューロパチー | 54 | 35 | 2 | 0 | 2 |
| 高血圧 | 13 | 33 | 32 | 0 | 32 |
| 発熱性好中球減少症 | 2 | 3 | 5 | ||
| 注入に伴う反応 | 0 | 2 | 0 | 0 | 0 |
- サブ解析では71歳以上では70歳以下に比較し、Grade3以上の有害事象の発現頻度が高かった(好中球数減少:75% vs 51%)。
4. 探索的解析
- UGT1A1遺伝子多型と有害事象について、重篤な好中球数減少の発現割合は野生型、シングルヘテロ、ホモ・ダブルヘテロにおいて有意差は認めなかったが、ホモ・ダブルヘテロにおいて多い傾向であった。
| UGT1A1 status | |||
|---|---|---|---|
| *1/*1 (n=27) | *1/*28 or *1/*6 (n=18) | *28/*28, *6/*6, or *28/*6 (n=5) | |
| 好中球数減少 | |||
| Any Grade | 21 (78%) | 15 (83%) | 5 (100%) |
| P value | 0.72 | 0.55 | |
| Grade 3-4 | 12 (44%) | 9 (50%) | 4 (80%) |
| P value | 0.77 | 0.33 | |
| 発熱性好中球減少症 | |||
| Grade 3-4 | 0 (0%) | 2 (11%) | 0 (0%) |
| P value | 0.15 | 0 | |
| 下痢 | |||
| Any Grade | 20 (74%) | 12 (67%) | 4 (80%) |
| P value | 0.74 | 1.00 | |
| Grade 3-4 | 5 (19%) | 2 (11%) | 2 (11%) |
| P value | 0.68 | 0.56 | |
結語
- 一次治療におけるmodified-FOLFOXIRI+BEV併用療法は、RAS 変異型切除不能大腸癌に対して有効であることが示された。
- modified-FOLFOXIRI+BEV併用療法は、日本における三剤併用療法の代替レジメンに成り得る。
関連論文
・ Clin Colorectal Cancer. 2018 Jun;17(2):147-155. doi: 10.1016/j.clcc.2018.01.011. Epub 2018 Feb 9.PMID: 29530335
執筆:国立がん研究センター東病院 消化管内科 中島 裕理 先生
監修:関西医科大学病院 がんセンター 学長特命准教授 佐竹 悠良 先生
監修:関西医科大学病院 がんセンター 学長特命准教授 佐竹 悠良 先生