| 対象疾患 | 治療ライン | 研究の相 | 主要評価項目 | 実施地域 | 日本の参加 |
|---|---|---|---|---|---|
| 胃癌 | 一次治療 | 第2相試験 | 全奏効割合 | 日本 | あり |
試験名 :KSCC/HGCSG/CCOG/PerSeUS 1501B
レジメン:トラスツズマブ+S-1+オキサリプラチン
登録期間:2015年6月〜2016年5月
背景
ToGA試験の結果、トラスツズマブ(T-mab)+FP(フルオロウラシル+シスプラチン)またはXP(カペシタビン+シスプラチン)併用療法はHER2陽性胃癌に対する標準的な一次治療として認識されている。オキサリプラチン(OX)は、胃癌を対象とした複数の臨床試験によってシスプラチン(CDDP)に対する非劣性が示されており、CDDPよりも安全性において優れている。
経口フッ化ピリミジン製剤であるS-1とOXの併用療法(SOX)は、胃癌を対象にSOX(OX 130mg/m2)とカペシタビン+OX(CAPOX)を比較する無作為化比較第2相試験1)において、CAPOXと同等の安全性と有効性を示したことより東アジア諸国の標準治療の一つとなった。本試験は、HER2陽性胃癌に対するT-mab+SOX(OX 130mg/m2)療法(T-SOX130)の有効性と安全性を検討する第2相試験として実施された。
経口フッ化ピリミジン製剤であるS-1とOXの併用療法(SOX)は、胃癌を対象にSOX(OX 130mg/m2)とカペシタビン+OX(CAPOX)を比較する無作為化比較第2相試験1)において、CAPOXと同等の安全性と有効性を示したことより東アジア諸国の標準治療の一つとなった。本試験は、HER2陽性胃癌に対するT-mab+SOX(OX 130mg/m2)療法(T-SOX130)の有効性と安全性を検討する第2相試験として実施された。
シェーマ
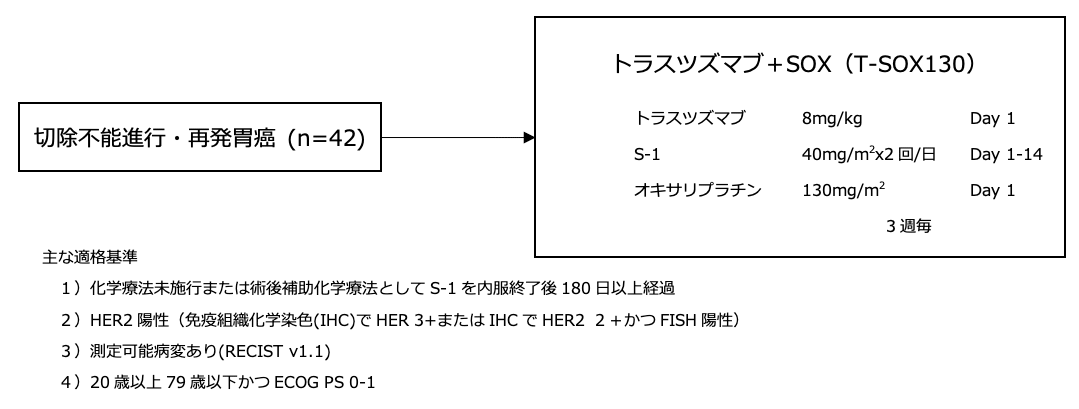
統計学的事項
主要評価項目:全奏効割合
G-SOX試験におけるSOX療法(OX 100mg/m2)の奏効割合が50%であったことから、閾値奏効割合を50%と推定した。T-mabの上乗せにより20%の奏効割合の改善を期待して、期待奏効割合を70%と推定した。片側α=0.05、検出力80%の条件で二項分布の正規近似に基づいて37例が必要症例数として算出された。さらに10%の不適格例と脱落例を見込み、40例が予定登録数として設定された。試験結果:
- 2015年6月から2016年5月にかけて日本国内の27施設より42例が登録された。
- 3例が登録後に不適格例として除外され、39例を解析対象とした。
- 患者背景:年齢中央値 66.0歳、性別:男/女 31(79.5%)/8(20.5%)、胃切除既往:有/無 5(12.8%)/34(87.2%)
- HER2発現状況:IHC 3+/IHC 2+かつFISH陽性 34(87.9%)/5(12.8%)
- 観察期間中央値は22.4か月だった。
1. 全奏効割合(主要評価項目)
| 症例数 | % | |
|---|---|---|
| CR | 9 | 23.1 |
| PR | 23 | 59.0 |
| SD | 2 | 5.1 |
| PD | 5 | 12.8 |
| NE | 0 | 0 |
| 全奏効割合 | 32 | 82.1(90%信頼区間 70.0-90.0) |
| 病態制御割合 | 34 | 87.2(95%信頼区間 73.3-94.4) |
2. 全生存期間
| イベント数 | 中央値 | 95%信頼区間 | 1年生存割合 | 2年生存割合 |
|---|---|---|---|---|
| 20/39 (51.3%) | 27.6ヶ月 | 15.6-未到達 | 74.4% | 57.9% |
3. 無増悪生存期間
| イベント数 | 中央値 | 95%信頼区間 |
|---|---|---|
| 32/39 (82.1%) | 7.0ヶ月 | 5.5-14.1 |
4. 治療成功期間
| 中央値 | 95%信頼区間 |
|---|---|
| 5.7ヶ月 | 4.6-7.0 |
- 35例(89.7%)は二次化学療法へ移行できた。
5. 有害事象(CTCAE ver.4.0)
| N (%) | 全Grade | GRADE 3-4 |
|---|---|---|
| 白血球数減少 | 18 (46.2) | 1 (2.6) |
| 好中球数減少 | 29 (74.4) | 4 (10.3) |
| 貧血 | 38 (97.4) | 5 (12.8) |
| 血小板減少 | 37 (94.9) | 7 (19.9) |
| AST高値 | 36 (92.3) | 2 (5.1) |
| 低ナトリウム血症 | 23 (59.0) | 4 (10.3) |
| 悪心 | 23 (59.0) | 3 (7.7) |
| 食欲不振 | 32 (82.1) | 7 (17.9) |
| 倦怠感 | 24 (61.5) | 2 (5.1) |
| 下痢 | 20 (51.3) | 3 (7.7) |
| 口内炎 | 19 (48.7) | 0 (0.0) |
| 末梢性感覚ニューロパチー | 32 (82.1) | 2 (5.1) |
- 治療関連死亡なし。
6. 投与状況
- 治療コースの中央値:8コース(範囲:1-33)
- 相対用量強度:S-1 87.1%、OX 80.1%、T-mab 73.8%
- 治療中止理由: 病勢進行 22例、有害事象 6例、根治切除へ移行 9例、その他 1例
結語
HER2陽性進行胃癌症例において、T-SOX130療法は十分な忍容性を有しており、その有効性はXP or SP+T-mab療法と同等であることが示された。本試験の結果より、T-SOX130療法はHER2陽性進行胃癌に対する標準的な一次治療になり得ると考える。
関連論文
1) Kim GM et al. A randomized phase II trial of S-1-oxaliplatin versus capecitabine–oxaliplatin in advanced gastric cancer. Eur J Cancer. 2017;48(4):518–526. [PubMed]
執筆:九州がんセンター 消化管外科 中島 雄一郎 先生
監修:近畿大学医学部 内科学教室 腫瘍内科部門 医学部講師 川上 尚人 先生
監修:近畿大学医学部 内科学教室 腫瘍内科部門 医学部講師 川上 尚人 先生